6 دقیقه
پژوهشگران دانشگاه کالیفرنیا، ارواین گزارش میدهند که یک آنتیاکسیدان طبیعی در چای سبز، وقتی با یک شکل رایج از ویتامین B3 ترکیب شود، میتواند یک مولکول کلیدی انرژی سلولی را در نورونها بازسازی کرده و دستگاه پاکسازی ضایعات مغزی را تحریک کند. در نورونهای کشتشده از موش، این ترکیب سطوح گوانوزین تریفسفات (GTP) را افزایش داد، عملکردهای مرتبط با اتوفاژی را باززنده کرد و تجمعهای آمیلوئید بتا — از نشانگان مرتبط با بیماری آلزایمر — را کاهش داد. از آنجا که هر دو ترکیب از طریق تغذیه و بهعنوان مکملهای غذایی در دسترساند، این یافتهها مسیر قابلباوری و کمخطر برای توسعه درمانی بیشتر را نشان میدهند.
پیشینه علمی: EGCG، نیکوتینامید و انرژی سلولی
اپیگالوکاتچین گالات (EGCG) یک پلیفنول فراوان در چای سبز است که خواص آنتیاکسیدانی و نورومحافظتی به آن نسبت داده شده است. نیکوتینامید شکلی از ویتامین B3 (متابولیت نیاسین) است که در غلات، ماهی، آجیل، حبوبات و تخممرغ یافت میشود و در فرایندهای متابولیسم سلولی تولید میشود. تیم UC Irvine این دو مولکول را همزمان بررسی کردند تا ببینند آیا میتوانند بر ذخایر نوکلئوتیدی درونسلولی — بهویژه گوانوزین تریفسفات (GTP)، یک حامل انرژی کمتر مورد توجه قرار گرفته — تأثیر بگذارند یا خیر.
GTP در عملکردهای سلولی متعددی شرکت دارد از جمله دینامیک میکروتوبولها، حملونقل درونسلولی و اتوفاژی — سیستم سلول برای تجزیه و بازیافت پروتئینها و اندامکهای آسیبدیده. پژوهشهای قبلی کاهش وضعیتهای انرژی نورونی و اختلال در پروتئواستاز را با پیری و بیماریهای نورودژنراتیو مرتبط کردهاند. آزمایشهای جدید کاهش GTP را بهعنوان یک عامل مکانیستی بالقوه در تجمع پیشرونده پروتئینهای سمی مرتبط با سن معرفی میکنند.
روشها و نتایج کلیدی آزمایشی
در آزمایشهای درونآزمایشگاهی، از نورونهای قشری موش در کشت استفاده شد که در معرض EGCG و نیکوتینامید قرار گرفتند، هم جداگانه و هم بهصورت ترکیبی. محققان سطوح GTP درونسلولی، نشانگرهای اتوفاژی و حضور تجمعهای آمیلوئید بتا را اندازهگیری کردند و همچنین نشانگرهای آسیب مرتبط با پیری نورونها را بررسی نمودند.
درمان ترکیبی نسبت به کنترلها افزایش قابلاندازهگیری در GTP تولید کرد و نورونهایی که GTP بالاتری داشتند، جریان اتوفاژی تقویتشدهای نشان دادند — نشانهای از عملکرد مؤثرتر ماشینآلات بازیافت سلولی. بهطور مهم، سلولهای درمانشده تجمع آمیلوئید بتا را کمتر نشان دادند و برخی نشانگرهای پیری سلولی تا حدودی بازگشت یافتند. این نتایج نشان میدهد که بازگرداندن تعادل نوکلئوتیدی انرژی میتواند نورونها را قادر سازد تا پروتئینهای سمی را پاک کنند.
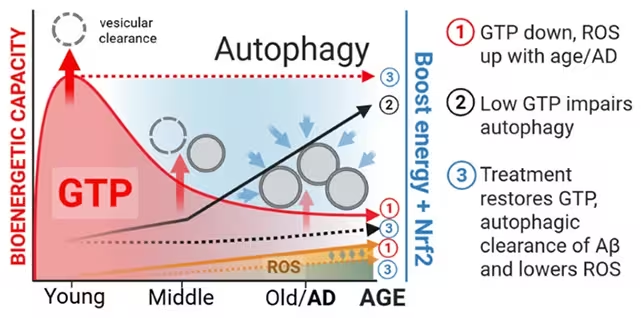
این مطالعه تأکید میکند که اثرات مشاهدهشده وقتی EGCG و نیکوتینامید با هم اعمال شدند قویتر بودند که نشاندهنده همافزایی است: اثرات آنتیاکسیدانی و سیگنالدهی EGCG ممکن است مکمل نقش نیکوتینامید در متابولیسم نوکلئوتیدها و NAD+ باشد و بهطور جمعی از بازسازی GTP حمایت کنند.
پیامدها برای پژوهش و توسعه درمانی آلزایمر
این کار GTP را بهعنوان محرکی نسبتاً کمتر مورد توجه در عملکردهای نگهداری نورونی برجسته میکند. اگر کاهش GTP در تجمع تدریجی پروتئینهای دگرشکلشده در مغزهای پیر نقش داشته باشد، درمانهایی که تعادل نوکلئوتیدی را بازمیگردانند میتوانند سرعت یا روند پاتولوژی بعدی، از جمله تجمع آمیلوئید مرتبط با بیماری آلزایمر، را کند یا متوقف کنند.
اگرچه EGCG و نیکوتینامید از طریق رژیم غذایی و مکملها در دسترساند، نویسندگان و سایر متخصصان هشدار میدهند که این نتایج از مدلهای سلولی موش بهدست آمدهاند. ترجمه این یافتهها به انسان نیازمند بهینهسازی دوز، مطالعات فارماکوکینتیک و کارآزماییهای بالینی کنترلشده است تا ایمنی و اثربخشی در پیشگیری یا تغییر سیر بیماریهای نورودژنراتیو تعیین شود.
مطالعات اپیدمیولوژیک قبلی مصرف منظم چای سبز را با ضایعات سفید مغزی کمتر و خطر کمتر زوال عقل مرتبط ساختهاند، اگرچه علیت در آنها ثابت نشده است. نیکوتینامید و پیشسازهای مرتبط NAD+ اثرات نورومحافظتی در مدلهای سکته و سایر مطالعات نورودژنراسیون نشان دادهاند. این پیوند مکانیکی جدید با GTP توضیح بیوشیمیایی معقولی برای برخی از این مشاهدات ارائه میکند و یک هدف بیوشیمیایی مشخص برای پژوهشهای بعدی فراهم میآورد.
دیدگاه کارشناسی
دکتر آمنه پاتل، استاد نوروبیولوژی در مؤسسه سلامت مغز (نمونهای فرضی)، اظهار میکند: «یافتههای UC Irvine جلب توجه میکنند زیرا تمرکز را به وضعیتهای انرژی نوکلئوتیدی — بهویژه GTP — بهعنوان یک عامل قابلتغییر در نگهداری نورونی منتقل میکنند. باید ببینیم آیا کسریهای مشابه GTP در نورونهای انسانی در پیری و مغزهای مبتلا به آلزایمر وجود دارد و آیا رویکردهای تغذیهای یا مکمل میتوانند غلظتهای درمانی را در سیستم عصبی مرکزی انسان ایجاد کنند یا خیر.»
دکتر پاتل میافزاید: «تشویقکننده است که این ترکیبات در بسیاری از زمینهها برای ایمنیشان شناخته شدهاند، اما ترجمه بالینی نیازمند انجام کارآزماییهای دقیق است. این مطالعه به ما یک فرضیه بیوشیمیایی روشن برای آزمون میدهد.»
محدودیتها، ایمنی و گامهای بعدی
محدودیتهای کلیدی که باید در نظر گرفته شوند:
- این آزمایشها در نورونهای کشتشده موش انجام شدهاند، نه در حیوانات زنده یا انسان. پاسخهای سلولی ممکن است در بافت مغزی یکپارچه بسیار متفاوت باشند.
- غلظتهای مؤثر در شرایط درونآزمایشگاهی ممکن است در انسان قابلدستیابی یا ایمن نباشند مگر آنکه فرمولاسیون یا راههای انتقالی که زیستدسترسپذیری مغزی را افزایش میدهند توسعه یابند.
- اثرات طولانیمدت، تداخل با داروهای دیگر و پیامدهای خارجهدف احتمالی ناشی از دستکاری مزمن مخازن نوکلئوتیدی نامشخصاند.
گامهای بعدی برنامهریزیشده شامل تایید پاسخ GTP در مدلهای حیوانی پیری و آلزایمر، روشنسازی مسیرهای بیوشیمیایی دقیق که توسط EGCG و نیکوتینامید GTP را افزایش میدهند، و طراحی مطالعات ترجمهای که دوز، نفوذپذیری سد خونی-مغزی و ایمنی در بزرگسالان مسن را مورد بررسی قرار دهند، خواهند بود.
فنآوریها و جهتهای پژوهشی مرتبط
- فرمولاسیونهای نوتریسوتیک و پرودرگهایی که تحویل CNS از جمله EGCG یا مشتقات نیکوتینامید را افزایش میدهند.
- بیومارکرهایی برای پایش سطح GTP نورونی یا فعالیت اتوفاژی در زنده.
- استراتژیهای ترکیبی که پشتیبانی متابولیک را با درمانهای ضدآمیلوئید یا ضدتاو جفت میکنند.
نتیجهگیری
مطالعه UC Irvine یک مسیر بیوشیمیایی امیدوارکننده را مشخص میکند — بازسازی GTP نورونی از طریق یک پلیفنول چای سبز (EGCG) بهعلاوه نیکوتینامید — که اتوفاژی را فعال کرده و تجمع آمیلوئید بتا را در نورونهای کشتشده موش کاهش میدهد. این نتایج مکانیزم ممکن ارتباطدهنده رژیم غذایی، متابولیتهای قابلتکمیل و پروتئواستاز مغزی را روشن میکند و از انجام پژوهشهای پیشبالینی و بالینی بیشتر حمایت مینماید. اگرچه امیدوارکننده است، این یافتهها مقدماتی باقی میمانند: مطالعات کنترلشده در حیوانات و کارآزماییهای انسانی لازم است تا مشخص شود آیا این رویکرد میتواند بهعنوان استراتژی پیشگیری یا درمان امن و مؤثر برای بیماری آلزایمر ترجمه شود.
منبع: sciencealert
.avif)


نظرات