8 دقیقه
خلاصه و یافتهٔ کلیدی
یک تیم پژوهشی بینالمللی نشان داده است که افزایش فعالیت میتوکندری — «نیروگاههای» سلولی — میتواند نقصهای حافظه و حرکتی را در موشهایی که بهمنظور نمایاندن علائم شبیه دمانس مهندسی شدهاند، معکوس کند. این تحقیق که در Nature Neuroscience منتشر شده است، از ابزاری تحقیقاتی به نام mitoDREADD-Gs برای تحریک انتخابی عملکرد میتوکندری در نورونها استفاده میکند و شواهدی ارائه میدهد که کاهش عملکرد میتوکندری میتواند محرک اصلی علائم نورودژنراتیو باشد و نه صرفاً یک پیامد ثانویه.
آزمایشها نه تنها همبستگی بلکه رابطهٔ علت و معلولی را نشان میدهند: هنگامی که فعالیت میتوکندری بهصورت شیمیایی افزایش مییابد، اختلالات شناختی و حرکتی بهبود مییابند؛ وقتی عملکرد میتوکندری دارویی سرکوب و سپس با همان ابزار دوباره فعال میشود، نارساییها بازمیگردند و دوباره قابل نجات هستند. این نتایج میتوکندری را بهعنوان یک هدف امیدوارکننده برای درمانهای آینده در بیماری آلزایمر و دیگر اختلالات نورودژنراتیو مطرح میکند.
پیشزمینهٔ علمی: میتوکندری و دژنراسیون عصبی
میتوکندریها اندامکهای داخلسلولی مسئول تولید آدنین تریفسفات (ATP)، واحد انرژی مورد نیاز فرآیندهای سلولی هستند. در نورونها که نیاز انرژی بالایی دارند، عملکرد میتوکندری برای نشانهدهی سیناپسی، پلاستیسیته و بقا اهمیت ویژهای دارد. در دههٔ گذشته، مطالعات متعددی اختلال عملکرد میتوکندری را با پیری و بیماریهای دژنراتیو عصبی مانند آلزایمر و پارکینسون مرتبط دانستهاند، اما سؤال پایدار این بوده است که آیا شکست میتوکندری علت از دست رفتن نورونها و کاهش شناخت است یا تنها یک پیامد ثانویهٔ دیگر فرآیندهای پاتولوژیک.
با ایجاد چارچوبی تجربی برای روشن و خاموش کردن فعالیت میتوکندری در بافت عصبی زنده، تیم پژوهشی مستقیماً مسئلهٔ علت و معلول را بررسی کرد. Giovanni Marsicano، نوروساینتیست از INSERM، توضیح میدهد که این کار اولین نشان شفاف است که اختلال میتوکندری را به علائم رفتاری دژنراسیون عصبی مرتبط میسازد و پیشنهاد میکند که نارسایی انرژی در نورونها ممکن است آبشاری را آغاز کند که به دژنراسیون منجر میشود.
جزئیات آزمایش: mitoDREADD-Gs، CNO، مدلهای موش و سلولهای انسانی
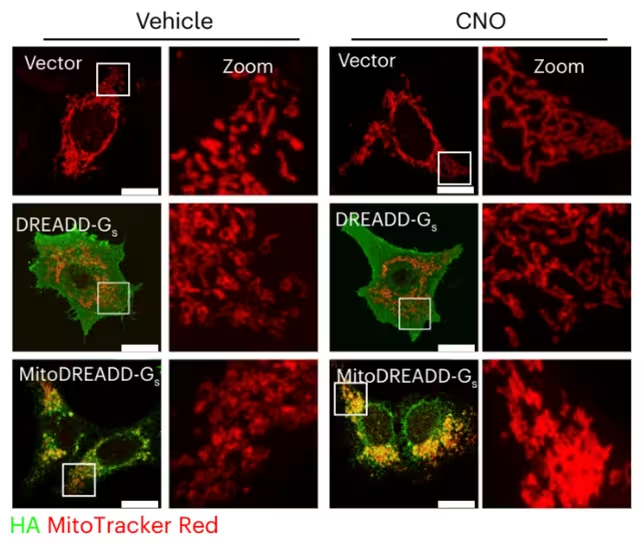
پیشرفت اصلی تجربی mitoDREADD-Gs است، یک عامل رمزگذاریشده ژنتیکی هدفگیر شده به میتوکندری که به داروی طراحیشده کلوزاپین-ان-اکساید (CNO) پاسخ میدهد. در واقع، CNO مانند کلید اشتعال عمل میکند: اتصال به mitoDREADD-Gs سیگنالدهی میتوکندری را افزایش داده و تولید ATP را در سلولهایی که این عامل را بیان میکنند تحریک میکند. با درمان CNO، فعالیت میتوکندری (به رنگ قرمز) افزایش یافت (پنلهای سمت راست). (Zottola et al., Nat. Neurosci., 2025)
پژوهشگران mitoDREADD-Gs را وارد نورونهای موشهایی کردند که از نظر ژنتیکی برای مدلسازی ویژگیهای کلیدی دمانس اصلاح شده بودند. آنها همچنین سیستم را در سلولهای انسانی کشت دادهشده در آزمایشگاه تست کردند. در هر دو محیط، فعالسازی گذرای فعالیت میتوکندری عملکرد حافظه را در آزمونهای رفتاری بهبود بخشید و نقصهای حرکتی را کاهش داد. برای آزمون بازگشتپذیری، تیم از داروهایی برای کاهش دارویی فعالیت میتوکندری استفاده کرد؛ اعمال CNO برای فعالسازی mitoDREADD-Gs سپس عملکرد را بازیابی کرد که این تفسیر را تقویت میکند که اختلال میتوکندری مسئول علائم مشاهدهشده بوده است و نه آسیبهای اتفاقی.
آزمایشها زیستشناسی مولکولی، تصویربرداری سلول زنده، الکتروفیزیولوژی و آزمونهای رفتاری را ترکیب کردند تا بیوانرژتیک سلولی را به نتایج در سطح ارگانیسم مرتبط سازند. مهم است بدانیم که mitoDREADD-Gs یک ابزار تحقیقاتی است نه یک محصول درمانی. با این حال، توانایی آن در تعیین زمان و مکان تأثیر فعالسازی میتوکندری بر عملکرد نورونی، الگویی برای شناسایی اهداف مولکولی قابل دارودرمانی فراهم میکند.
پیامدها برای آلزایمر و راهبردهای درمانی آینده
این مطالعه زاویهٔ جدیدی برای توسعه درمانهای بیماریهای نورودژنراتیو پیشنهاد میکند: بازگرداندن یا حفظ عملکرد میتوکندری در نورونهای آسیبپذیر. Étienne Hébert Chatelain از Université de Moncton اشاره میکند که این ابزار میتواند به نقشهبرداری مسیرهای مولکولی و سلولی که از نارسایی انرژی تا اختلال نورونی میروند کمک کند و بدین ترتیب جستجوی اهداف درمانی مؤثر را راهنمایی کند. اگر اختلال عملکرد میتوکندری یک محرک بالادستی در برخی از انواع دمانس باشد، راهبردهای دارویی که متابولیسم میتوکندری را تقویت یا از افول آن جلوگیری میکنند ممکن است علائم را کند یا معکوس کنند.
پژوهشگران چندین احتیاط را تأکید میکنند. دمانس چندوجهی است: عوامل ژنتیکی، متابولیک، عروقی و محیطی متعددی به شروع و پیشرفت بیماری کمک میکنند. آنچه در یک مدل موش خاص یا سیستم کشت سلولی کنترلشده کار میکند ممکن است مستقیماً به مغز پیچیدهٔ انسان ترجمه نشود. اثرات بلندمدت نیز نیاز به ارزیابی دقیق دارند: تحریک مزمن عملکرد میتوکندری ممکن است پیامدهای ناخواستهای از جمله تغییر در سیگنالدهی سلولی، استرس اکسیداتیو یا عدم تعادل متابولیک داشته باشد. Luigi Bellocchio از INSERM اولویتهای تجربی بعدی را اینگونه بیان میکند: اندازهگیری اثرات تحریک طولانیمدت میتوکندری بر بقای نورونها، پیشرفت بیماری و اینکه آیا مداخلهٔ زودهنگام میتواند از دست دادن نورونی را به تأخیر اندازد یا جلوگیری کند.
فناوریهای مرتبط و رویکردهای مکمل
این کار در کنار دیگر راهبردهای هدفگیری میتوکندری که در حال بررسی هستند قرار میگیرد، از جمله مولکولهای کوچک که بیوژنز میتوکندری را تقویت میکنند، آنتیاکسیدانهایی که گونههای اکسیژن واکنشپذیر را کاهش میدهند و درمانهای ژنی که نقصهای DNA میتوکندری را تصحیح میکنند. ترکیب فعالسازی میتوکندری با درمانهایی که روی آمیلوئید، تاو، التهاب یا سلامت عروقی تمرکز دارند ممکن است برای مقابله با طبیعت چندعاملی بیماری آلزایمر ضروری باشد.
دیدگاه کارشناسان
دکتر Maria Alvarez، نوروساینتیستی که روی بیوانرژتیک سلولی متمرکز است، اظهار داشت: "این آزمایشها شواهد علتمحور قانعکنندهای ارائه میدهند که نارسایی انرژی نورونی میتواند محرک علائم رفتاری باشد. رویکرد mitoDREADD-Gs روش ظریفی برای کنترل فعالیت میتوکندری با دقت زمانی و مکانی است. برای ترجمه به بالین، چالش یافتن داروشناسی ایمن بالینی است که این فعالسازی انتخابی را تقلید کند بدون اینکه اثرات خارجهدف ایجاد کند."
دکتر Alvarez اضافه میکند که مطالعات آینده باید بهصورت طولی در مدلهای پیرتر انجام شوند و ترکیباتی با درمانهای محافظتکنندهٔ سیناپس را بررسی کنند تا مشخص شود آیا حمایت میتوکندری میتواند مدارهای عصبی را برای ماهها یا سالها حفظ کند نه فقط برای ساعات یا روزها.
گامهای بعدی و چشماندازهای آینده
نویسندگان چند مسیر پیگیری پیشنهاد میکنند: گسترش آزمایشها به مدلهای دیگر دژنراسیون عصبی و اختلالات روانپزشکی مرتبط با اختلال عملکرد میتوکندری؛ نقشهبرداری مسیرهای مولکولی پاییندستی که با بازگردانی فعالیت میتوکندری فعال میشوند؛ و غربالگری نامزدهای دارویی که میتوانند اثرات mitoDREADD-Gs را در فرمولاسیونهای سازگار با انسان بازتولید کنند. مسیر ترجمه نیازمند پروفایل ایمنی قوی، بهینهسازی مکانیزمهای تحویل و آزمایش در مدلهای حیوانی بزرگ قبل از مدنظر قرار دادن مطالعات بالینی انسانی خواهد بود.
اگر ثابت شود که نارسایی میتوکندری رویداد ابتدایی و مهمی در برخی اشکال دمانس است، هدفگیری متابولیسم انرژی سلولی ممکن است بخشی اساسی از یک راهبرد درمانی چندوجهی شود. حتی اگر اختلال میتوکندری تنها یکی از چندین عامل باشد، مداخلاتی که عرضه انرژی نورونی را بهبود میبخشند ممکن است پیشرفت علائم را کند یا اثربخشی سایر درمانها را افزایش دهند.
این پژوهش در Nature Neuroscience منتشر شده است و ابزار تجربی و دادهها نقشهراهی برای تیمهایی فراهم میکند که نقش میتوکندری در پیری مغز و بیماری را بررسی میکنند.
نتیجهگیری
این مطالعه شواهد تجربی محکمی ارائه میدهد که افزایش مستقیم فعالیت میتوکندری در نورونها میتواند نقصهای حافظه و حرکتی را در مدلهای موشی دمانس معکوس کند و از رابطهٔ علتومعلولی بین اختلال میتوکندری و علائم نورودژنراتیو پشتیبانی میکند. در حالی که mitoDREADD-Gs خود یک ابزار آزمایشگاهی است نه درمان بالینی، مسیرهای مولکولی و رویکردهای تجربی جدیدی را روشن میکند که میتوانند توسعهٔ داروهای آینده را راهنمایی کنند. گامهای حیاتی بعدی شامل ارزیابی اثرات بلندمدت، آزمایش در مدلهای متنوع بیماری و شناسایی راهکارهای ایمن و سازگار با انسان برای تعدیل عملکرد میتوکندری بهعنوان بخشی از تلاشهای جامع برای پیشگیری یا درمان آلزایمر و اختلالات مرتبط است.
منبع: sciencealert
.avif)

نظرات