6 دقیقه
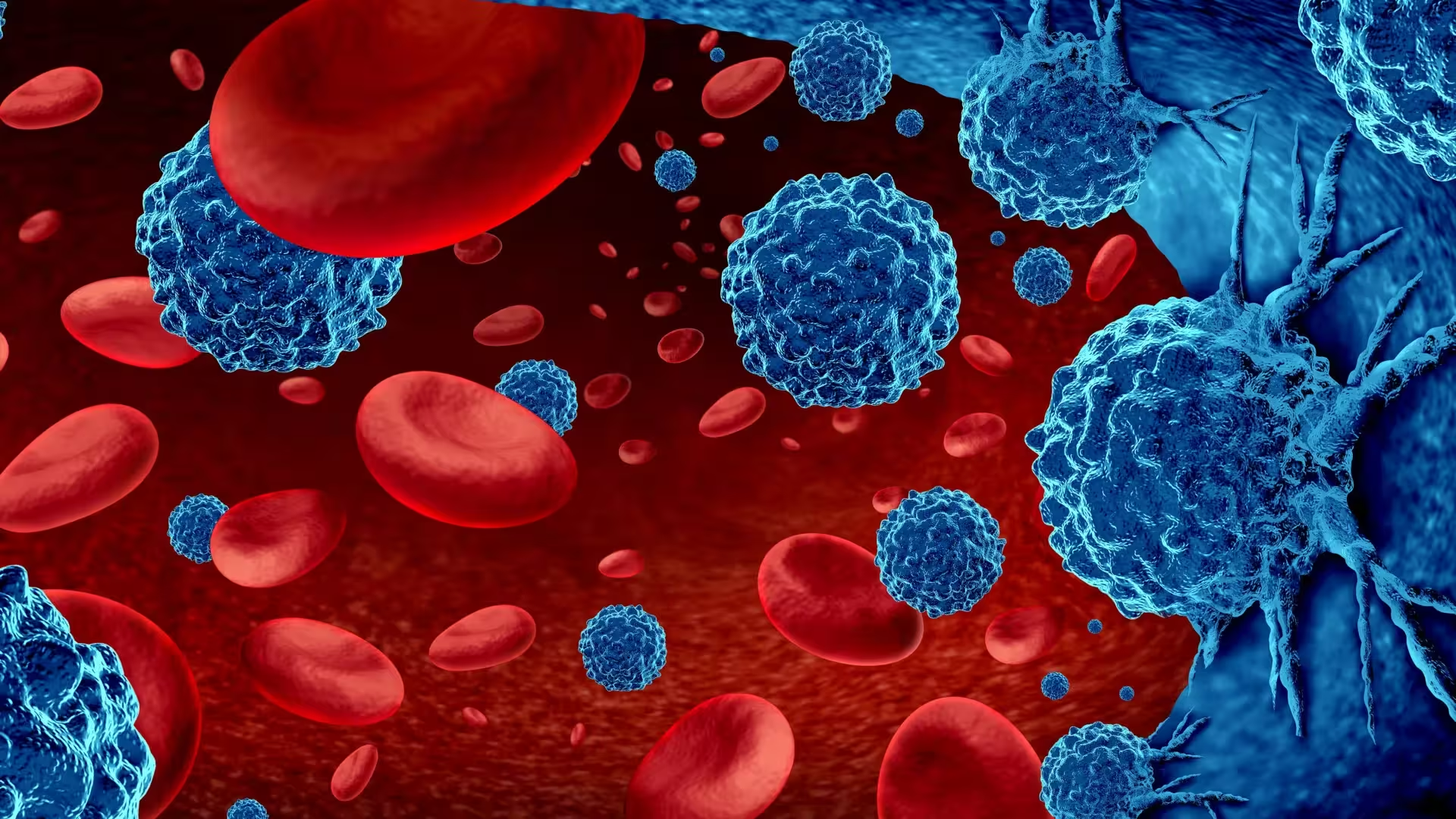
قطع جریان خون به بافتها میتواند مغز استخوان را بهطور زودرس پیر کند و سیستم ایمنی را به حالتی که نسبت به سرطان تسامحآمیز است سوق دهد، براساس مطالعه تازهای از NYU Langone Health که در JACC: CardioOncology منتشر شده است. در مدلهای موشی سرطان پستان، ایسکمی موقت در یک اندام خلفی رشد تومور را در مقایسه با موشهایی که جریان خون طبیعی داشتند دو برابر کرد. این آزمایشها نشان میدهند که ایسکمی محیطی — کاهش رساندن اکسیژن ناشی از انسداد شریانها در پاها — برنامهریزی سلولهای بنیادی مغز استخوان را بازنویسی میکند و تولید سلولهای ایمنی را به سمت جمعیتهایی سوق میدهد که تومورها را سرکوب میکنند تا آنها را هدف قرار دهند. اعتبار تصویر: Shutterstock
پیشزمینه علمی: ایسکمی، بیماری شریان محیطی و خطر سرطان
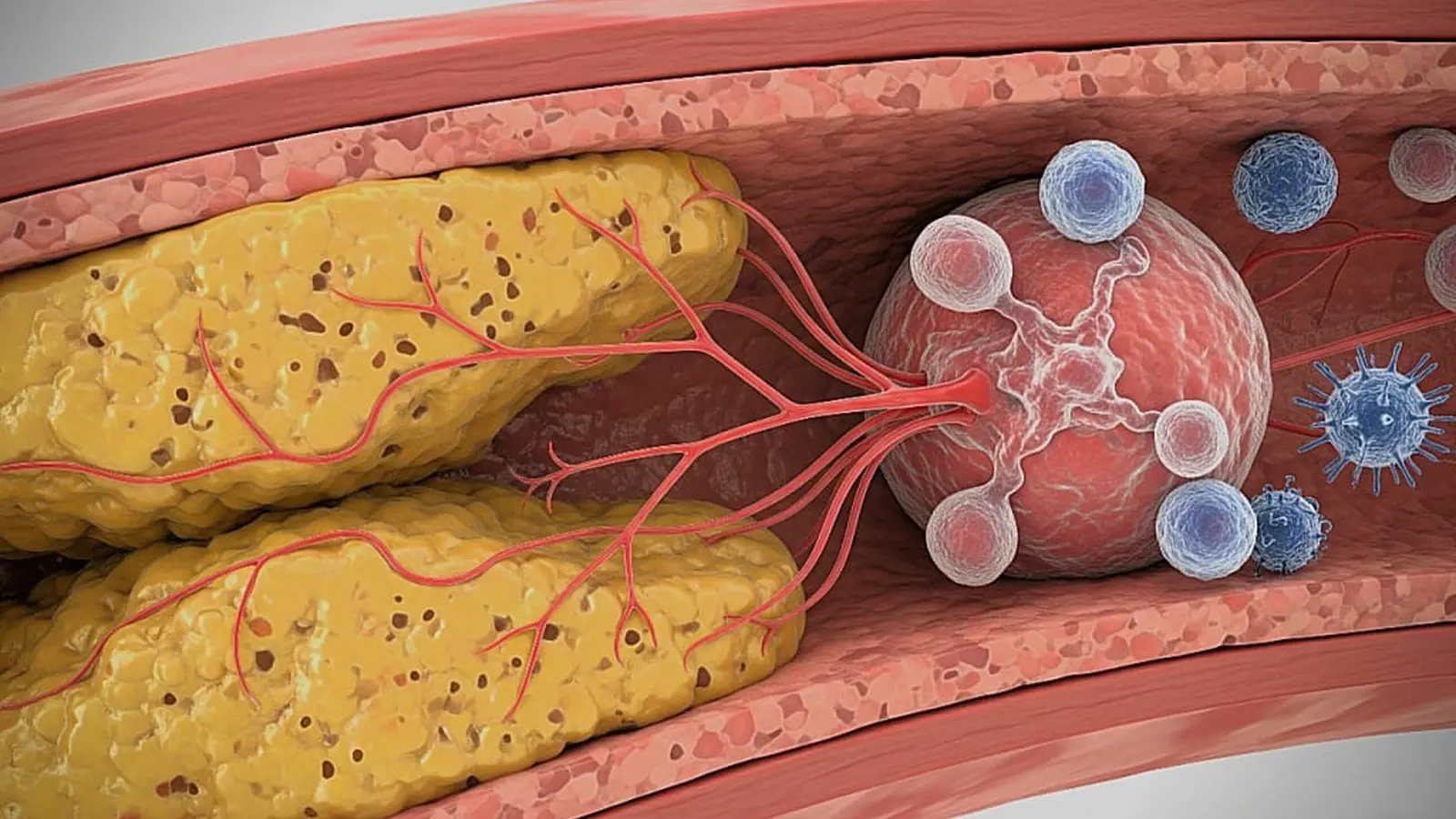
ایسکمی زمانی رخ میدهد که چربی، کلسترول و التهاب شریانها را تنگ میکنند و رساندن خون غنی از اکسیژن را محدود میسازند. در پاها، این وضعیت بهعنوان بیماری شریان محیطی (PAD) شناخته میشود که میلیونها نفر را در سراسر جهان درگیر میکند و خطر حمله قلبی و سکته را افزایش میدهد. پژوهشگران NYU بر پایه کارهای قبلی (از جمله یک مطالعه ۲۰۲۰ که ایسکمی مرتبط با حمله قلبی را به رشد سریعتر تومور پیوند میداد) بررسی کردند که چگونه ایسکمی خارج از قلب ایمنی سیستمیک و پیشرفت سرطان را تحتتأثیر قرار میدهد.
سیستم ایمنی برای جایگزینی و تأمین سلولهای سفید خون در طول زندگی متکی به سلولهای بنیادی مغز استخوان است. در شرایط جریان خون طبیعی، این سیستم بین پاسخهای التهابی (برای پاکسازی عفونتها یا بافت آسیبدیده) و سیگنالهای تنظیمی که از آسیب فرعی جلوگیری میکنند، تعادل برقرار میکند. مطالعه NYU نشان میدهد که ایسکمی این تعادل را با تغییر برنامهریزی سلولهای بنیادی در مغز استخوان مختل میکند.
روشها و یافتههای کلیدی
تیم پژوهشی از مدل موشی کنترلشدهای که حامل تومورهای پستان بود استفاده کرد و برای شبیهسازی PAD، ایسکمی موقتی در یک اندام خلفی ایجاد کرد. آنها پیشرفت تومور، پروفایل سلولهای ایمنی و تنظیم ژنی را بین حیوانات ایسکمیدیده و کنترل مقایسه کردند.
یافتههای کلیدی:
- رشد تومور در موشهایی با ایسکمی اندام نسبت به کنترلها دو برابر شد.
- سلولهای بنیادی مغز استخوان بهگونهای بازبرنامهریزی شدند که تولید رده میلوییدی (مونوکیتها، ماکروفاژها، نوتروفیلها) را ترجیح دهند؛ ردههایی که با سرکوب ایمنی مرتبطاند.
- تولید لنفوسیتها، بهویژه سلولهای T که ایمنی ضدتومور را واسطه میکنند، کاهش یافت.
- ریزمحیط تومور شاهد تجمع جمعیتهای ایمنساز بود، از جمله مونوکیتهای Ly6Chi، ماکروفاژهای شبیه M2 با مشخصه F4/80+ MHCIIlo و سلولهای تنظیمکننده T (Tregs).
- ایسکمی منجر به تغییرات پایدار در صدها ژن و بازآرایی ساختار کروماتین در سلولهای ایمنی شد، که فعالسازی برنامههای ضدسرطان را دشوارتر میسازد.
مکانیسم: پیرشدن مغز استخوان و تغییر گرایش ایمنی
نویسندگان گزارش میدهند که ایسکمی بهطور موثر فنوتیپی از پیرشدن زودرس را در مغز استخوان القا میکند. بازآرایی کروماتین و تغییرات بیان ژنی خروجی سلولهای بنیادی را دگرگون کرده و چشمانداز ایمنی سیستمی را تولید میکنند که رشد تومور را تحمل میکند. به گفتهی نویسنده مربوطه Kathryn J. Moore, PhD، «مطالعه ما نشان میدهد که جریان خون مختلشده رشد سرطان را صرفنظر از محل وقوع در بدن تسریع میکند. این پیوند بین بیماری شریان محیطی و رشد سرطان پستان اهمیت حیاتی پرداختن به عوامل خطر متابولیک و عروقی را بهعنوان بخشی از یک استراتژی جامع درمان سرطان برجسته میسازد.»
برنامهریزی مجدد ایمنی بلندمدت
فراتر از التهاب گذرا، ایسکمی تغییرات اپیژنتیک و رونویسی ماندگاری ایجاد کرد. این تغییرات پایدار توضیح میدهند که چرا یک رخداد عروقی موضعی میتواند ایمنی سیستمیک را بازسازی کند و محیطی مساعد برای پیشرفت سرطان پدید آورد.
پیامدهای بالینی و مسیرهای آینده
این کار چند مسیر ترجمهپذیر را پیشنهاد میدهد: غربالگری زودتر سرطان برای بیماران مبتلا به PAD، آزمایشهای بالینی برای ارزیابی اینکه آیا درمانهای تنظیمکننده التهاب یا اپیژنتیک میتوانند تغییرات ایمنی ناشی از ایسکمی را معکوس کنند، و راهبردهای مراقبتی یکپارچه که سلامت عروقی و خطر سرطان را همزمان هدف میگیرند. نویسنده اول Alexandra Newman, PhD اشاره میکند، «این یافتهها درهایی به سوی استراتژیهای جدید در پیشگیری و درمان سرطان باز میکنند، مانند غربالگری زودهنگام سرطان برای بیماران مبتلا به بیماری شریان محیطی و استفاده از درمانهای ضدالتهابی برای مقابله با این اثرات.»
گامهای بعدی
تیم NYU قصد دارد مطالعات بالینی را پشتیبانی کند تا ارزیابی کند آیا داروهای ضدالتهاب مورد تأیید یا عاملهایی که دسترسی کروماتین را تغییر میدهند میتوانند پس از اپیزودهای ایسکمیک ایمنی ضدتومور را بازیابی کنند.
دیدگاه کارشناسی
دکتر Elena Sánchez، پژوهشگر ایمونو-انکولوژی (کارشناس ساختگی برای زمینه)، اظهار میکند: «این مطالعه بهطور ظریف پاتولوژی عروقی را به پیری سیستم ایمنی متصل میکند. اگر مکانیسمهای مشابه در انسانها عمل کنند، غربالگری خطر سرطان در بیماران مبتلا به PAD میتواند به یک اقدام پیشگیرانه مهم تبدیل شود. همچنین این مطالعه بر درمان التهاب و بیماریهای عروقی بهعنوان راهبردهایی برای حمایت از نظارت ایمنی تأکید میکند.»
نتیجهگیری
مطالعه NYU Langone شواهد مکانیکی ارائه میدهد که انسداد جریان خون خارج از تومور — مانند بیماری شریان محیطی — میتواند با بازبرنامهریزی سلولهای بنیادی مغز استخوان و ترویج جمعیتهای سلولی سرکوبکننده ایمنی، سرطان را تسریع کند. این نتایج سلامت عروقی را به پیشرفت سرطان پیوند میزند و بر ارزش مراقبت تلفیقی قلبیعروقی و انکولوژیک، انجام غربالگری زودهنگام برای بیماران در معرض خطر و بررسی درمانهایی که التهاب و تغییرات اپیژنتیک را هدف میگیرند تا ایمنی ضدتومور قوی را بازیابی کنند، تأکید میکند.
منبع: sciencedaily
.avif)

نظرات