6 دقیقه
تحقیقات اخیر فرضیهای نگرانکننده را تقویت کردهاند: ممکن است بیماری آلزایمر شامل فرایندهای عفونی باشد که از خارج مغز، از جمله حفره دهان، شروع میشوند. چندین مطالعه اکنون به Porphyromonas gingivalis — باکتریای که بیشترین ارتباط را با پریودنتیت مزمن (بیماری لثه) دارد — بهعنوان یک عامل بالقوه در پاتولوژی آلزایمر اشاره میکنند. این دیدگاه، تصور مرسوم از آلزایمر بهعنوان صرفاً یک اختلال نورودژنراتیو درونی را به چالش میکشد و راههای جدیدی برای تشخیص و درمان باز میکند.
زمینه علمی و اهمیت P. gingivalis
Porphyromonas gingivalis یک باکتری گرم منفی بیهوازی است که در التهاب مزمن پریودنتال نقش دارد. عفونت طولانیمدت لثه موجب التهاب سیستمیک میشود و میتواند اجزای باکتریایی و سموم را وارد جریان خون کند. در تحقیقات مربوط به آلزایمر، پژوهشگران روی دو پدیده پیوند خورده تمرکز کردهاند: ظهور پروتئینهای مشخصه در مغز — آمیلوئید بتا (Aβ) و تاو هایپرفسفریله شده — و وجود آنتیژنها یا آنزیمهای میکروبی که ممکن است این پاتولوژی را القا یا تشدید کنند.
یک یافته کلیدی که در سال ۲۰۱۹ منتشر شد، DNA مربوط به P. gingivalis، پروتئینهای باکتریایی و پروتئازهای سمیای به نام ژینگیپینها را در مغز افراد متوفی مبتلا به آلزایمر شناسایی کرد. این مطالعه همچنین آنتیژنهای ژینگیپین را در مغز افرادی یافت که پاتولوژی آلزایمر داشتند اما در طول زندگی تشخیص زوال عقلی نگرفته بودند. این الگو نشان میدهد که تهاجم باکتریایی ممکن است پیش از افت شناختی بالینی رخ دهد و نه صرفاً نتیجه بهداشت دهان ضعیف در بیماران مبتلا به دمانس.
جزئیات مطالعه و کشفیات اصلی
در آزمایشهای آزمایشگاهی هماهنگشده توسط Cortexyme و به رهبری پژوهشگرانی مثل یان پوتمپا و استیفن دومینی، تحلیلهای پس از مرگ مغز انسان همراه با مدلهای حیوانی ترکیب شد. مشاهدات اصلی شامل موارد زیر بود:
- شناسایی ماده ژنتیکی P. gingivalis و آنزیمهای ژینگیپین در مغزهای مبتلا به آلزایمر، که با نشانگرهای تاو و یوبیکوئیتین همراه بود.
- در موشها، عفونت دهانی با P. gingivalis منجر به استقرار در مغز، افزایش تولید Aβ و تغییرات التهابی عصبی شد که با پاتولوژی مشابه آلزایمر همخوانی داشت.
- یک مهارکننده مولکول کوچک که توسط Cortexyme توسعه یافت، COR388 (آتوزاگینستات)، بار باکتریایی در مغز موشها را کاهش داد، تولید آمیلوئید بتا را کم کرد و التهاب عصبی را در مدلهای پیشبالینی کاهش داد.
این نتایج بهتنهایی علتشناسی آلزایمر در انسان را اثبات نمیکنند، اما چند معیار معقول زیستی را برآورده میکنند: مسیر محتمل عفونت (از دهان به گردش خون تا مغز)، شناسایی اجزای میکروبی در بافت بیمار، و تغییر در حضور میکروب و نشانگرهای بیماری وقتی پروتئازهای باکتریایی هدف قرار گرفتند.
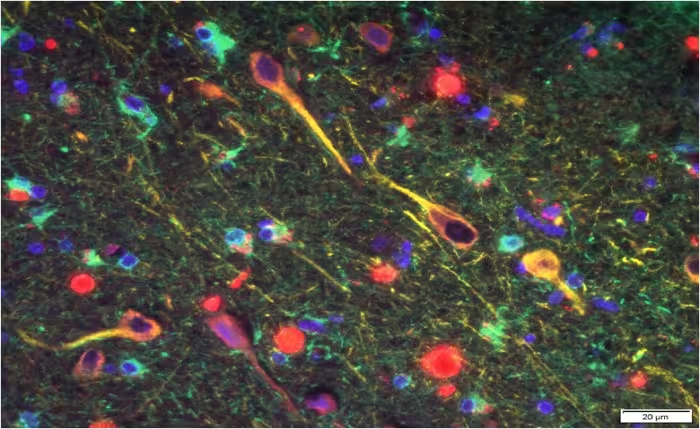
نشانگرها و مکانیسمها
ژینگیپینها آنزیمهای پروتئولیتیکیای هستند که توسط P. gingivalis ترشح میشوند و میتوانند پروتئینهای میزبان را تجزیه کرده و پاسخهای ایمنی را تغییر دهند. حضور آنها با سطوح بالاتر پاتولوژی تاو و تگینگ یوبیکوئیتین همبستگی داشت — نشانههایی از اختلال هموستازی پروتئینی در نورونها. آمیلوئید بتا که مدتها با تشکیل پلاک در آلزایمر مرتبط بوده نیز در موشهای آلوده افزایش یافت که از این فرض پشتیبانی میکند که Aβ ممکن است بهعنوان بخشی از پاسخ ایمنی ذاتی به تهاجم میکروبی تولید شود.
پیامدها برای درمان و پیشگیری
اگر عوامل بیماریزای دهانی در پیشرفت آلزایمر نقش داشته باشند، استراتژیهایی برای کاهش بیماری پریودنتال و هدفگیری فاکتورهای ویروژنی باکتری میتواند بخشی از رویکردی چندجانبه برای پیشگیری و مداخلات زودهنگام شود. درمانهایی که به خنثیسازی ژینگیپینها یا پاکسازی عفونتهای مزمن دهانی میپردازند، ممکن است مکمل پژوهشهای موجود درباره داروهای هدفگیرنده آمیلوئید و استراتژیهای ضدالتهابی باشند.
«عاملهای عفونی قبلاً در توسعه و پیشرفت آلزایمر مطرح شدهاند، اما شواهد علتمندی قانعکننده نبوده است»، استیفن دومینی و همکارانش اشاره کردهاند. «اکنون برای اولین بار شواهد محکمی پیوند میان پاتوژن داخلسلولی گرم منفی P. gingivalis و پاتوژنز آلزایمر را نشان میدهد.» دیوید رینولدز از مؤسسه تحقیقات آلزایمر اضافه کرده که هرچند فواید تا کنون محدود به مطالعات حیوانی بوده، بررسی رویکردهای متنوع ضروری است چرا که مدت طولانی است درمانهای جدید دمانس کمتر شدهاند.
دیدگاه کارشناسی
دکتر النا مورالس، نورولوژیست و پژوهشگر میکروبیوم، میگوید: «این مجموعه مطالعات نشاندهنده پیوستگی سلامت سیستمیک و سلامت مغز است. عوامل بیماریزای دهانی مانند P. gingivalis میتوانند شرایط التهابی مزمن ایجاد کنند که در طول دههها ممکن است مغز مستعد را به سمت نورودژنراسیون سوق دهد. این باکتری بهتنهایی همه موارد آلزایمر را توضیح نمیدهد، اما پیشنهاد میکند اقدامات عملی پیشگیرانه — بهبود مراقبتهای پریودنتال و استراتژیهای ضد میکروبی هدفمند — میتواند خطر را کاهش دهد. بهطور حیاتی، کارآزماییهای بالینی در مقیاس بزرگ لازم است تا مشخص شود آیا مداخلاتی که عفونت دهان را کاهش میدهند، مسیر دمانس را در انسانها تغییر میدهند یا خیر.»
آیا بیماری لثه باعث آلزایمر میشود، یا افراد مبتلا به دمانس در معرض بهداشت دهان ضعیفتر قرار میگیرند؟ (Jonathan Borba/Unsplash)
نتیجهگیری
شواهدی که عوامل بیماریزای دهانی — بهویژه Porphyromonas gingivalis — را با تغییرات مغزی مرتبط با آلزایمر پیوند میدهند، میدان تحقیق را به سمت در نظر گرفتن عفونت و التهاب مزمن بهعنوان عوامل مشارکتکننده در نورودژنراسیون سوق داده است. اگرچه علتشناسی در انسان هنوز اثبات نشده، شناسایی ژینگیپینها و نشانههای باکتریایی در مغز بیماران مبتلا به آلزایمر همراه با دادههای حمایتی حیوانی و نامزدهای درمانی مرحلهاول مانند COR388، نیاز به پژوهشهای بالینی بیشتر را توجیه میکند. در همین حال، بهداشت خوب دهان و مراقبتهای پریودنتال اقدامات کمخطر و بالقوه سودمندی برای سلامت سیستمیک و مغز محسوب میشوند.
منبع: sciencealert
.avif)

نظرات