8 دقیقه
تصور کنید سالها پیش از آنکه فراموشی یک نام یا جا گذاشتن کلید اولین نشانهها را بدهد، دریابید که در مسیری به سمت زوال عقل قرار دارید. این وعده پشتِ یک «ساعت مولکولی» ساده اما مؤثر مبتنی بر آزمایش خون است که میتواند زمان تقریبی آغاز علائم آلزایمر را در یک بازه سه تا چهار ساله محدود کند.
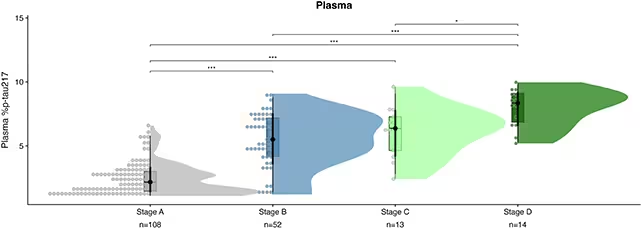
سطوح پروتئین p-tau217 نشان داده شد که با پیشرفت آلزایمر همبستگی دارند.
چگونه یک پروتئین در خون سالها تغییر مغز را نگاشت میکند
دانشمندان دانشگاه واشینگتن در سنتلوئیس یک آزمون خون موجود برای p-tau217 را اقتباس کردند و مدلسازی ریاضی را بر آن افزودند. نتیجه چه شد؟ ابزاری که سطوح سنجیدهشدهٔ این پروتئین را به نقطهای مرتبط میکند که در آن حافظه و سایر اختلالات شناختی قابل تشخیص میشوند. ساده بهنظر میرسد؛ اما در عمل قدرتمند است.
چرا p‑tau217؟ زیرا این شکل فسفریلهشدهٔ تاو، دو نشانگر زیستی اساسی آلزایمر را دنبال میکند: تودههای تار مانند تاو (tau tangles) و پلاکهای آمیلوئید‑بتا. غلظتهای خونی p‑tau217 فرآیندهایی را که درون مغز رخ میدهد منعکس میکند و پنجرهای به پاتوژنی طولانیمدت و کند حرکت میگشاید، بدون هزینه و ناراحتی PET اسکن یا نمونهگیری مایع نخاعی (لومبار پنچر).
محققان دادههای طولی خون 603 شرکتکننده را که طی چندین سال جمعآوری شده بود، بررسی کردند. با نگاشت مسیرهای p‑tau217 در برابر سنی که علائم شناختی نخستینبار ظاهر شدند، فرمولهایی استخراج کردند که یک فرد را بر روی خط زمان بین نخستین تغییرات زیستی و نزول بالینی قرار میدهد. فاصلهٔ معمول بین تغییرات اولیه در مغز و اختلال شناختی قابلتشخیص طولانی است—اغلب 10 تا 30 سال—بنابراین ابزاری که پیشبینی را به چند سال محدود کند برای برنامهریزی پژوهشی و در نهایت مراقبت از بیمار ارزشمند است.
این رویکرد مبتنی بر دادههای طولی و مدلسازی ریاضی است؛ به این معنا که با مشاهده روند تغییرات بیومارکر در زمان میتوان نقاط عبور از آستانههای پاتولوژیک را شناسایی کرد. ترکیب آزمایشهای حساس p‑tau217 با مدلهای آماری امکان میدهد تا جایگاه یک فرد روی منحنی بیماری تعیین شود و زمان تقریبی ظهور علائم بالینی تخمین زده شود.
با این همه، محدودیتهایی وجود دارد. در حال حاضر این روش برای پیشبینی در سطح گروهی مناسبتر است. این ابزار میتواند گروههایی را که احتمالاً در یک بازهٔ مشخص دچار علائم خواهند شد بهطور قابلاعتمادی جدا کند اما هنوز پیشبینیهای دقیق نقطهای برای یک فرد بهتنهایی ارائه نمیدهد. پژوهشگران تأکید میکنند که پیش از آنکه این روش به یک آزمایش پیشآگهی روتین در کلینیک تبدیل شود، نیاز به دادهها و پالایش بیشتر است.
الگوها، تأثیر سن و اهمیت ساعت
نویسندهٔ اصلی، کلن پترسن، تجمع آمیلوئید و تاو را به حلقههای درخت تشبیه میکند. اگر حلقهها را اشتباه بخوانید، سن را اشتباه قضاوت میکنید. اگر درست بخوانید، میتوانید زمان رویش درخت را برآورد کنید. این تشبیه دو نکته را در بر میگیرد: نخست اینکه تجمع پیشروندهٔ این نشانگرها مسیر ثابتی را در بسیاری از افراد دنبال میکند؛ دوم اینکه سنی که در آن این بیومارکرها از آستانهٔ پاتولوژیک عبور میکنند، پیشبینیکنندهٔ قوی زمان ظهور علائم است.
یکی از یافتههای برجسته این بود که افراد مسنتر معمولاً فاصلهٔ کوتاهتری بین آغاز تغییر زیستی و ظهور علائم داشتند. مغزهای جوانتر ممکن است برای مدت طولانیتری مقاومت نشان دهند و حتی در حالیکه پاتولوژی در حال انباشت است، آسیب را پنهان کنند. این موضوع پیامدهای مهمی برای طراحی کارآزماییها دارد: جذب شرکتکنندگان جوانتر که بیومارکر مثبت دارند ممکن است نیاز به پیگیری طولانیتری برای ثبت بروز علائم داشته باشد، در حالیکه شرکتکنندگان مسنتر ممکن است تغییرات را سریعتر نشان دهند.
فواید عملی این روش گسترده است. کارآزماییهای بالینی که داروهای پیشگیرانه را آزمایش میکنند به شرکتکنندگانی نیاز دارند که احتمالاً در بازهٔ زمانی مطالعه دچار علائم شوند. یک ساعت مبتنی بر خون به هدفگیری این افراد کمک میکند، اندازه و طول مطالعه را کاهش داده و کارآیی را افزایش میدهد. علاوه بر این، دسترسی را گسترش میدهد: آزمایشهای خون بهمراتب ارزانتر و آسانتر برای مقیاسپذیری هستند تا روشهای تصویربرداری یا تشخیص مایع نخاعی که گران و در بسیاری از مناطق در دسترس نیستند.
از نظر فنی، تبدیل غلظتهای p-tau217 به یک «زمان مورد انتظار» نیازمند کالیبراسیون دقیق آزمون و در نظر گرفتن متغیرهای همنهشت است؛ مانند وضعیت ژنتیکی (برای مثال APOE)، عوامل همبیماری، تفاوتهای تکنیکی بین آزمایشگاهها و ویژگیهای جمعیتی. به همین دلیل تیم تحقیقاتی از دادههای طولی متعدد و تکنیکهای بهینهسازی پارامترها برای کاهش خطا و افزایش قابلیت تعمیم استفاده کرد.
اما سوالات اخلاقی باقی میمانند. آیا افراد مایلند بازهٔ زمانی محدودتری برای بروز علائم بدانند اگر گزینههای درمانی محدود باشد؟ چگونه باید پیشبینیهای احتمالاتی را به بیماران اطلاع داد؟ اینها فقط مسائل فنی نیستند؛ آنها به رضایتآگاهانه، مشاوره روانشناختی و برنامهریزی بهداشت عمومی گره خوردهاند.
دیدگاه کارشناسان
«این نوع پیشرفت ترجمهای همان چیزی است که ما امیدواریم — پل زدن نشانگرهای آزمایشگاهی و تصمیمگیری عملی»، دکتر مایا چن، اپیدمیولوژیست عصبی که با مطالعه ارتباطی نداشت، میگوید. «اگر در جوامع گوناگون اعتبارسنجی شود، یک ساعت خونی میتواند نحوهٔ جذب شرکتکنندگان در کارآزماییها و اولویتبندی نظارت توسط پزشکان را دگرگون کند. اما باید آن را با منابع مشاورهای قوی همراه کنیم؛ دانستن بازهای بدون گزینههای پیشگیرانهٔ روشن میتواند بیش از نفع، آسیب برساند.»
این مطالعه در نشریهٔ Nature Medicine منتشر شده و توسط نورولوژیستهایی در دانشگاه واشینگتن هدایت شده است، از جمله سوزان شیندلر که بر دسترسی تأکید میکند: آزمایشهای خونی میتوانند دامنهٔ پژوهش و خدمات بالینی را فراتر از مراکزی که قادر به انجام PET اسکن یا نمونهگیری مایع نخاعی هستند، گسترش دهند. گامهای بعدی شامل آزمون مدل در جمعیتهای بزرگتر و متنوعتر، تلفیق سایر بیومارکرهای خونی و پالایش الگوریتمها برای بهبود دقت در سطح فردی است.
در عین حال، برای افزایش قابلیت اجرای این رویکرد در عمل بالینی، استانداردسازی آزمایشها میان آزمایشگاهها ضروری است. بدون استانداردسازی، نتایج مقایسهپذیر نخواهند بود و مدلها ممکن است در جمعیتهای جدید عملکرد متفاوتی نشان دهند. همچنین لازم است پژوهشهای اقتصادی انجام شود تا مزیت هزینه-اثربخشی استفاده از ساعت مولکولی خون در مقایسه با روشهای مرسوم ارزیابی شود.
برای حال، ساعت مولکولی کمتر یک طالعبینی شخصی است و بیشتر یک ابزار علمی — ابزاری که وعدهٔ تیزتر کردن زمانبندی کارآزماییها و عمیقتر کردن درک ما از لغزش سالها-در-طولِ آلزایمر را میدهد. امید این است که زمانبندی بهتر، درمانها را تسریع کند و روزی به افراد حس واضحتری از آنچه انتظار دارند و زمان اقدام بدهد.
در ادامه به چند نکتهٔ فنی و توصیه برای پژوهشگران و کلینیکها اشاره میشود:
• اعتبارسنجی بینمرکزی: تکرار نتایج در آزمایشگاهها و جمعیتهای مختلف برای اطمینان از سازگاری و کاهش سوگیریهای نمونه ضرورت دارد.
• ترکیب بیومارکرها: افزودن نشانگرهای دیگر خونی (مانند نوروفیلامنت لایت چین یا نشانگرهای التهابی) ممکن است دقت پیشبینی را در سطح فردی افزایش دهد.
• مدلسازی پیچیدهتر: استفاده از یادگیری ماشین و مدلهای غیرخطی میتواند الگوهای پنهانتر را استخراج کند، اما همراه با نیاز به مجموعههای دادهٔ بزرگتر و شفافیت بیشتر در تبیین مدلها است.
• چارچوبهای اخلاقی و مشاوره: توسعهٔ پروتکلهایی برای اطلاعرسانی نتایج به شرکتکنندگان، همراه با حمایت روانشناختی و راهنمایی بالینی، ضروری است.
• سیاستهای بهداشتی: تصمیمگیرندگان باید دربارهٔ ورود این نوع آزمونها به خدمات بهداشتی عمومی، پوشش بیمهای و اولویتبندی منابع فکری کنند تا دسترسی منصفانه تضمین شود.
در مجموع، این ساعت مولکولی بر پایهٔ p‑tau217 یک گام مهم به سوی تشخیص زودهنگام و هدفمند کردن تلاشها برای پیشگیری و درمان آلزایمر است. اما برای تبدیل شدن به یک ابزار بالینی قابلاطمینان، نیاز به تکرار، استانداردسازی و توجه همزمان به مسائل اخلاقی و اجتماعی دارد.
منبع: sciencealert
نظرات
آسمانچرخ
ما تو خونواده چند نفرو دیدیم که تا آخر PET نکردن؛ اگه خون بتونه زودتر هشدار بده، خیلی کمک میکنه. البته باید با مشاوره همراه بشه
توربو
زیاد هیجان زده نشید؛ به نظر میاد کمی تبلیغیه، مخصوصا بدون استانداردسازی و دادههای متنوع. اما یه قدم رو به جلو هست...
سینا
معقول به نظر میاد. برای کارآزماییها عالیه، برای تصمیم شخصی هنوز زوده.
بیوانیکس
جالبه، ولی واقعا تا چه حد قابل اعتماد؟ تستها توی آزمایشگاههای مختلف یکی میشن؟ نمونهگیری، تفاوت فنی، اینا چطور حل میشه؟
دیتاپالس
واااای، اگه واقعیت داشته باشه یعنی میشه سالها قبل فهمید... هم امیدوارم هم ترسیدهم، کلی سوال هم هست!

ارسال نظر