6 دقیقه
خلاصه مطالعه و زمینه
یک تیم در دانشکده پزشکی دانشگاه واشنگتن در سنت لوییس گزارش دادهاند که لمبوروکسانت، یک داروی خواب مورد تأیید FDA، الگوهای خواب سالمتری را بازگردانده و آسیبهای مرتبط با تائو را در مدلهای موشی نورودژنراتیو کاهش داده است. این مطالعهٔ داوریشده که در Nature Neuroscience منتشر شده است، بهبود خواب را با سطوح پایینتر پروتئین غیرطبیعی تائو، التهاب عصبی کمتر و کاهش از دستدادن نورونها در موشهایی که به تجمع تائو مستعد هستند، پیوند میدهد.
یک کمکخواب آشنا و مورد تأیید FDA خواب سالمتری را بازگرداند و آسیبهای مغزی ناشی از تائو را در موشهای مدل آلزایمر کاهش داد؛ این مسئله نشان میدهد مدارهای خواب میتوانند اهرمی علیه تحلیل عصبی باشند. با مسدود کردن سیگنالدهی اورکسین، این دارو تائوی غیرطبیعی و التهاب را کاهش داد؛ رویکردی که میتواند مکمل درمانهای ضدآمیلوئید باشد. اعتبار: Shutterstock
نویسندهٔ اول Samira Parhizkar، PhD، و نویسندهٔ ارشد David M. Holtzman، MD نشان میدهند که هدفگیری مدارهای تنظیمکنندهٔ خواب میتواند مسیرهای مولکولی مرتبط با بیماری آلزایمر و سایر تائوپاتیها را تحت تأثیر قرار دهد. یافتهها نشان میدهند که آنتاگونیستهای گیرندهٔ اورکسین مانند لمبوروکسانت ممکن است بهعنوان مکملی برای درمانهای ضدآمیلوئید موجود مفید باشند، که تا کنون تنها اثرات جزئی بر پیشرفت بیماری داشتهاند.
مکانیزم، طراحی آزمایشی و نتایج
لمبوروکسانت یک آنتاگونیست دوگانهٔ گیرندهٔ اورکسین است؛ یعنی هر دو نوع گیرندهٔ اورکسین 1 و 2 را مسدود میکند. اورکسینها نوپپتیدهایی هستند که بیداری را تقویت میکنند و فرآیندهای فیزیولوژیک مانند چرخهٔ خواب-بیداری و اشتها را تنظیم میکنند. با مهار سیگنالدهی اورکسین، لمبوروکسانت ساختار خواب را در موشهای تحت درمان تغییر داد و به نظر میرسد فسفریلاسیون غیرطبیعی و تجمع پروتئین تائو را کاهش داده است. اضافه شدن گروههای فسفات روی تائو باعث کلوخهوار شدن آن میشود که این روند التهاب و مرگ نورونی را در چندین بیماری تخریبی عصبی تحریک میکند.
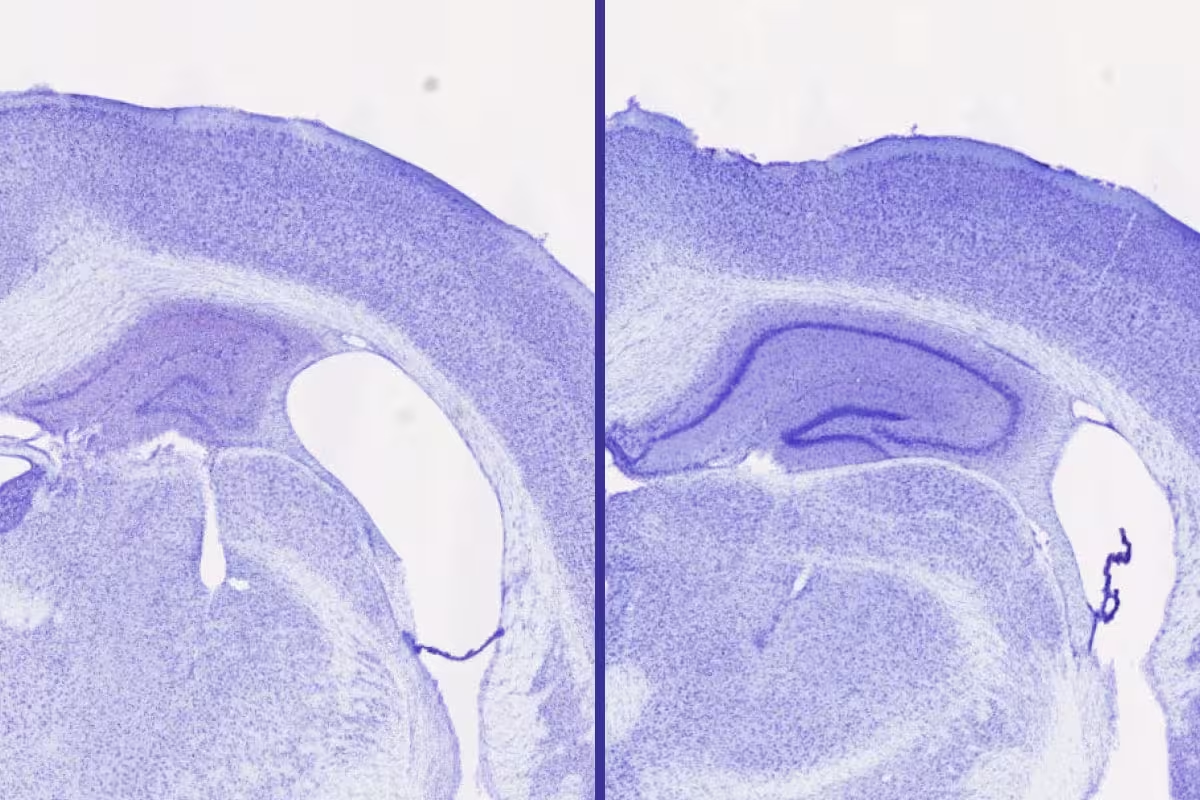
یک مطالعهٔ جدید توسط پژوهشگران WashU Medicine نشان میدهد که لمبوروکسانت و داروهای خواب با مکانیزم مشابه ممکن است به درمان یا پیشگیری از آسیب ناشی از تجمع مضر پروتئین تائو در چندین بیماری نورودژنراتیو، از جمله آلزایمر، کمک کنند. تصاویر مقاطع عرضی بافت مغز دو موش را نشان میدهند که از نظر ژنتیکی مستعد تجمع تائو هستند. درمان با لمبوروکسانت (سمت راست) منجر به حجم بزرگتر هیپوکامپ (حلزون مرکزی بنفش) میشود که برای حافظه اهمیت دارد، و فاصلهٔ خالی در بافت مغزی (فضای سفید) نسبت به حالت بدون درمان (سمت چپ) کمتر است. اعتبار: Samira Parhizkar/WashU Medicine
در موشهای مهندسیشدهای که معمولاً پاتولوژی تائو را توسعه میدهند، موشهای نر تحت درمان با لمبوروکسانت 30 تا 40 درصد حجم هیپوکامپ بیشتری نسبت به کنترلهای بدون درمان حفظ کردند. مطالعه شامل مقایسهٔ مستقیم با زولپیدم، یک آرامبخش-هیپنوتیک که سیگنالدهی GABA را تقویت میکند، نیز بود: زولپیدم خواب را افزایش داد اما تجمع تائو یا نورودژنراسیون مرتبط را کاهش نداد. این تضاد از این ایده پشتیبانی میکند که اثر نوروتصویتی به تنظیم مسیر اورکسین بستگی دارد نه صرفاً مدت خواب. مهم این که لمبوروکسانت در این مدلها هماهنگی حرکتی را دچار اختلال نکرد، نکتهای کلیدی در نظر برای استفادهٔ بالقوه در افراد دارای اختلال شناختی.
پژوهشگران اثرات سودمند را عمدتاً در موشهای نر مشاهده کردند، نتیجهای وابسته به جنسیت که در حال بررسی بیشتر است. Holtzman اشاره میکند که موشهای ماده در این مدل در خط مبنا دژنراسیون کمتری داشتند که ممکن است توانایی آشکارسازی مزیت دارو را در آن گروه محدود کرده باشد.
پیامدها برای مراقبت از آلزایمر و تحقیقات آینده
این کار پیشبالینی مدارهای خواب را بهعنوان یک عامل قابل تعدیل در پاتولوژی تائو معرفی میکند. چون درمانهای تأییدشدهٔ فعلی که آمیلوئید را هدف میگیرند برخی جنبههای بیماری را کاهش میدهند اما پیشرفت را بهطور کامل متوقف نمیکنند، ترکیب درمانهای ضدآمیلوئید با عواملی که تجمع تائو را مهار میکنند میتواند استراتژی امیدبخشی باشد. لمبوروکسانت و سایر آنتاگونیستهای گیرندهٔ اورکسین در حال حاضر دادههای ایمنی و فارماکولوژی از استفادهٔ انسانی بهعنوان درمان بیخوابی دارند که میتواند مطالعات انتقالی را تسریع کند.
با این حال، نتایج موشها تضمینی برای سودمندی در انسان نیست. آزمایشهای بالینی لازم است تا بررسی کنند آیا آنتاگونیستهای اورکسین تجمع تائو را کند میکنند، التهاب را کاهش میدهند و شناخت را در افراد در معرض خطر یا مراحل اولیهٔ آلزایمر و تائوپاتیهای مرتبط حفظ میکنند یا نه. داروی مورد مطالعه توسط شرکت Eisai در قالب یک تلاش تحقیقاتی مشترک فراهم شده بود.
فناوریها و جهتگیریهای پژوهشی مرتبط
کارهای آینده ممکن است رویکردهای ترکیبی را بررسی کنند که هم آمیلوئید و هم تائو را هدف میگیرند، نشانگرهای زیستی (بایومارکرها) برای پایش غیرتهاجمی فسفریلاسیون تائو توسعه دهند، و اینکه آیا کرونوتهراپی یا زمانبندی دوز بهینه نتایج را بهبود میبخشد را مطالعه کنند. درک تفاوتهای وابسته به جنسیت، ایمنی طولانیمدت در سالمندان و تداخل با سایر درمانهای نورودژنراتیو ضروری خواهد بود.
نظر کارشناس
دکتر Elena Morales، نورولوژیست بالینی و پژوهشگر خواب، اظهار میکند: «این نتایج قانعکنندهاند زیرا به یک رویکرد مبتنی بر مکانیزم اشاره میکنند نه صرفاً ترویج علائم خواب. بهرهگیری از داروهایی که مدارهای خواب را بازساز میکنند میتواند یک محور درمانی جدید علیه تائو باز کند. اما تبدیل یافتههای موشی به آزمایشهای انسانی به طراحیهای مبتنی بر نشانگر زیستی و توجه به اثرات وابسته به جنسیت نیاز خواهد داشت.»
نتیجهگیری
این مطالعه لمبوروکسانت و آنتاگونیستهای مشابه گیرندهٔ اورکسین را بهعنوان نامزدهای امیدوارکنندهای معرفی میکند که میتوانند از طریق تنظیم مدارهای خواب پاتولوژی تائو را تغییر دهند. در حالی که نتایج پیشبالینی نقشی بالقوه در پیشگیری یا کند کردن نورودژنراسیون مرتبط با تائو را پشتیبانی میکنند، آزمایشهای بالینی برای ارزیابی اثربخشی، دوز بهینه و ایمنی در افراد مبتلا یا در معرض خطر آلزایمر و سایر تائوپاتیها ضروری هستند.
منبع: scitechdaily


ارسال نظر