10 دقیقه
دیدگاه تازه درباره گرههای لنفاوی و جراحی سرطان
تحقیقات جدید از موسسه پیتر دوهرتی برای عفونت و ایمنی نشان میدهد که گرههای لنفاوی صرفاً ایستگاههای بیجان برای عبور سلولهای ایمنی نیستند، بلکه بهعنوان «مرکز آموزش» فعال عمل میکنند که ایمنی ضدتومور و ضدویروسی را شکل میدهند. نتایج این پژوهشها که در نشریه Nature Immunology منتشر شده، نشان میدهد گرههای لنفاوی محیط میکروویژهای فراهم میکنند که از سلولهای T نوع «شبیه-بنیادین» (stem-like) پشتیبانی میکند؛ جمعیتی که قادر به تکثیر، بقاء طولانی و تولد سلولهای قاتل قدرتمندی هستند که به تومورها و عفونتهای ویروسی مزمن حمله میکنند.
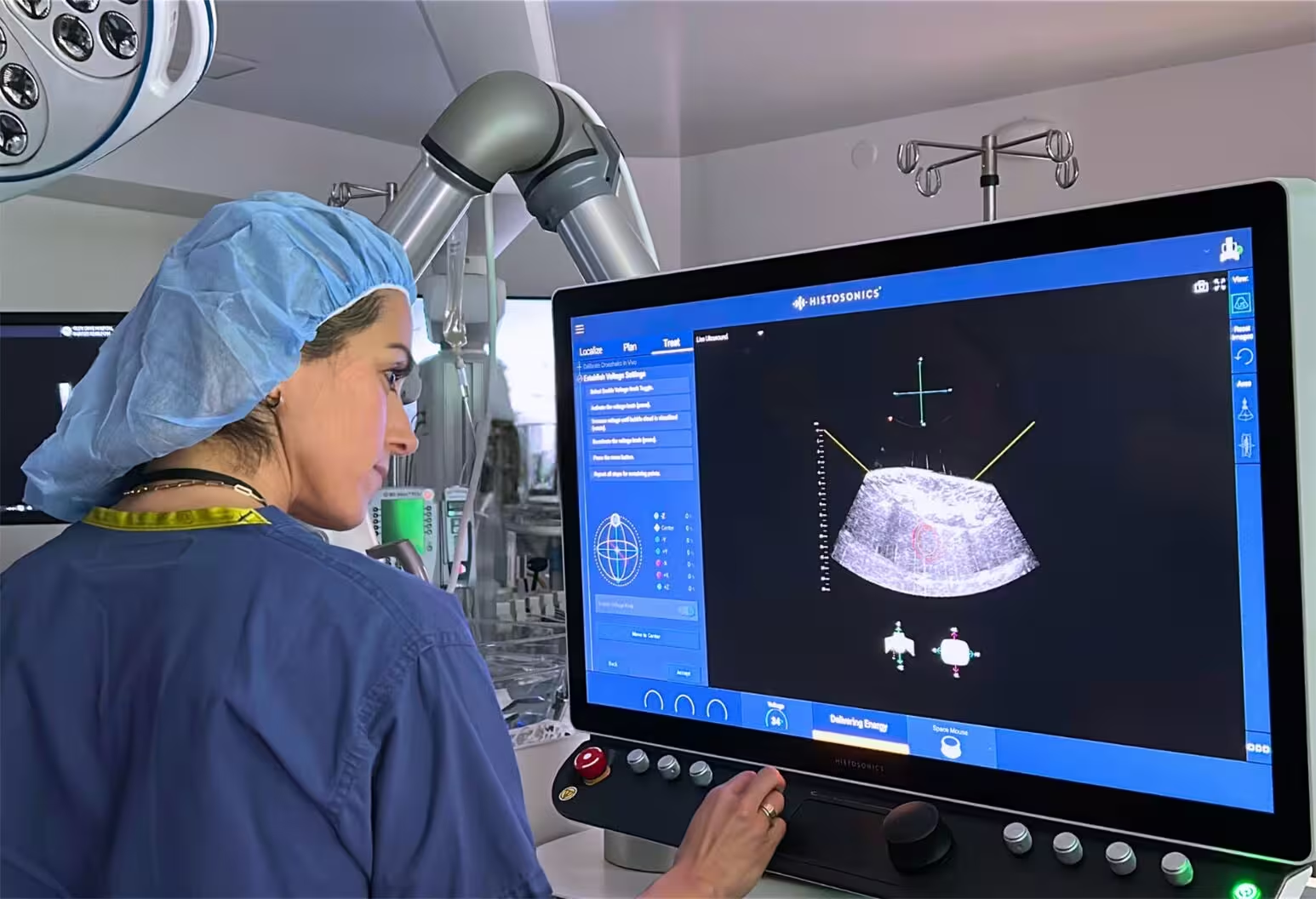
تحقیقات انجامشده در موسسه دوهرتی نشان میدهد گرههای لنفاوی چگونه بهعنوان میدانهای تمرینی فعال برای سلولهای ایمنی عمل میکنند و آنها را برای مقابله بهتر با سرطان و عفونتهای مزمن آماده میسازند. Credit: Stock
زمینه علمی: چرا گرههای لنفاوی اهمیت دارند
گرههای لنفاوی اندامهای کوچک و ساختاریافتهای هستند که در طول سیستم لنفی توزیع شدهاند. این ساختارها مایع لنف را پالایش میکنند و با جمعآوری سلولهای ارائهدهندهٔ آنتیژن، سایتوکاینها و سلولهای T، پاسخ ایمنی تطبیقی را تنظیم میکنند. کارهای اخیر در ایمونولوژی جمعیتهایی از سلولهای T را شناسایی کرده که به آنها «شبیه-بنیادین» یا progenitor exhausted گفته میشود؛ این جمعیت بهعنوان مخزنی حیاتی مطرح شده که در طول پاسخهای ایمنی طولانیمدت، سلولهای کارآمد قاتل (effector) را بازتولید میکند و به حفظ توانایی دفاعی بدن کمک مینماید.
تیم پژوهشی دوهرتی رفتار این سلولهای شبیه-بنیادین را در گرههای لنفاوی با رفتار آنها در دیگر اندامهای کمکی لنفاوی مانند طحال مقایسه کرد. در مدلهای پیشبالینی، محققان دریافتند محیط گره لنفاوی بهطور منحصربهفردی از بقای این جمعیت و تکثیر آن پشتیبانی میکند. در مقابل، طحال و سایر ارگانها از نظر علائم سلولی و مولکولی لازم برای حفظ این جمعیت فقیرتر بودند که در نتیجه تولید سلولهای سیتوتوکسیک (قاتل) ضعیفتر میشد. تفاوت مذکور پیامد مستقیمی بر عملکرد ایمنوتراپیها دارد؛ زیرا منبع پشتیبان سلولهای پیشماده برای پاسخهای ایمنی طولانیمدت را تحت تأثیر قرار میدهد.
برای درک بهتر، میتوان گره لنفاوی را شبیه یک مدرسه تخصصی در نظر گرفت: جایی که سلولهای T اولیه آموزش میبینند تا ویژگیهای لازم برای مبارزه مؤثر با تومور یا ویروسهای مزمن را بهدست آورند. این آموزش شامل تعامل با سلولهای ارائهدهندهٔ آنتیژن، دریافت سیگنالهای سیتوکاینی، و قرارگیری در یک شبکه سلولی پشتیبان است که از دوام و تمایز آنها حمایت میکند.
یافتههای کلیدی و پیامدهای بالینی
یافتهٔ محوری این است که گرههای لنفاوی یک فضای سازگار ایجاد میکنند که در آن سلولهای T شبیه-بنیادین میتوانند پایدار بمانند و به سلولهای قاتل مؤثری تمایز یابند. از آنجا که بسیاری از جراحیهای سرطان برای کاهش خطر متاستاز، گرههای لنفاوی نزدیک را برداشته یا حذف میکنند، این رویهٔ رایج ممکن است بهطور ناخواسته منبعی کلیدی از سلولهای T مورد نیاز برای پاسخهای پایدار ایمنوتراپی را حذف کند؛ شامل درمانهایی مانند مهارکنندههای چکپوینت و روشهای سلولی مثل CAR-T.
این موضوع از چند جهت اهمیت دارد: نخست، نشان میدهد که استخراج بیشازحد گرههای لنفاوی ممکن است توانایی بدن در بازتولید سلولهای قاتل ضدتومور را کاهش دهد. دوم، این پژوهش مولکولها و مسیرهای سیگنالدهی را شناسایی کرده که تنظیمکنندهٔ این سلولهای پیشماده هستند؛ این اطلاعات میتواند مبنایی برای طراحی داروها یا سیستمهای دارورسانی باشد که عملکرد گره لنفاوی را تقویت کنند یا سیگنالهای حمایتی آن را تقلید نمایند.
پیامدها برای ایمنوتراپی
حفظ گرههای لنفاوی هرگاه از لحاظ جراحی ممکن باشد، میتواند پاسخ بیماران به مهارکنندههای ایمنی (immune checkpoint inhibitors) و درمانهای سلولی را با نگهداری مخزن سلولهای شبیه-بنیادین بهبود ببخشد. علاوه بر این، شناسایی سیگنالهای مولکولی که این پیشسازها را تنظیم میکنند، راه را برای طراحی داروهای هدفمند، واکسنهای نانوذرهای یا افزایندههای موضعی باز میکند که بهطور خاص عملکرد مفید گرههای لنفاوی را تقویت کنند.
پروفسور آکسل کالیز، سرپرست آزمایشگاه در موسسه دوهرتی و نویسنده ارشد این مطالعات، نکته مهمی را خلاصه کرد: «کار ما گرههای لنفاوی را بهعنوان مربیان فعال سلولهای T بازتعریف میکند. حذف جراحی این مراکز ایمنی ممکن است ظرفیت بدن برای تولید پاسخهای ضدتومور پایدار را کاهش دهد.» دکتر کارلسون تسویی، نویسنده مسئول یکی از مقالات، افزود که مسیرهای مولکولی شناساییشده میتواند راهنمایی برای نسل بعدی ایمنوتراپیها باشد که هدفشان تقویت این جمعیتهای پیشماده است.
برای مثال، اگر دارویی بتواند سیگنالهای نگهدارندهٔ بقا یا تقسیم سلولی در محیط گره لنفاوی را تقلید کند، میتوان بدون نیاز به حفظ کامل ساختار گره یا در شرایطی که حذف گره ضروری است، اثر مشابهی در حفظ مخزن سلولی ایجاد کرد. از سوی دیگر، داروها یا فرمولههایی که بهصورت موضعی وارد گره لنفاوی میشوند (مانند نانوذرات یا حاملهای بیولوژیک) میتوانند بهطور مستقیم این میکرومحیط را تقویت کنند تا پاسخ ایمنی مقاومتری تولید شود.
از آزمایشگاه تا بالین: ترجمه و محدودیتها
این مطالعات در مدلهای حیوانی انجام شدهاند، بنابراین برای اثبات و تعمیم به انسان نیازمند تأییدات بالینی هستند. تیم تحقیقاتی در حال همکاری با پژوهشگران کلینیکی برای بررسی عملکرد گرههای لنفاوی در بیمارانی است که مهارکنندههای چکپوینت دریافت میکنند، بهویژه در سرطان ملانوما که نمونههای بالینی و پاسخ ایمنی قابل ردیابیتری دارد. پروفسور شاهنین ساندهو از مرکز سرطان پیتر مککالوم تأکید کرده که ادغام نمونههای پیشبالینی و بالینی برای ترجمهٔ این نتایج به دستورالعملهای جراحی و راهبردهای درمانی ضروری خواهد بود.
کاربردهای بالینی احتمالی شامل بازنگری در روشهای بیوپسی گره لنفاوی نگهبان (sentinel lymph node biopsy)، کاهش برداشتهای غیرضروری نودها و توسعهٔ ادجوانتهای هدفمند گره لنفاوی یا درمانهای موضعی سیتوکاینی است که نقش حمایتی گره را حفظ یا بازسازی کنند. مسیرهای ترجمهای دیگر عبارتاند از واکسنهای نانوذرهای طراحیشده برای رساندن سیگنالهای محرک به گرههای لنفاوی یا رژیمهای دارویی که بهصورت انتخابی نگهداری سلولهای شبیه-بنیادین را تقویت میکنند.
علاوه بر این، شناسایی نشانگرهای مولکولی خاص میتواند به توسعهٔ بیومارکرهایی کمک کند که پیشبینی کنندهٔ چگونگی تأثیر حذف گره لنفاوی بر پاسخ ایمنوتراپی در یک بیمار خاص باشند. این امر میتواند منجر به تصمیمگیری جراحی شخصیسازیشده شود: در برخی بیماران که احتمال متاستاز پایین است و در عین حال نیاز به پاسخ ایمنی طولانیمدت دارند، حفظ گرهها ممکن است اولویت یابد؛ در مقابل، در مواردی که برداشتن نودها برای کنترل بیماری ضروری است، تیمهای درمانی میتوانند پیش و پس از جراحی از مداخلات دارویی برای بازیابی یا حفظ مخزن سلولی استفاده کنند.
محدودیتهای موجود را نباید دستکم گرفت: تفاوتهای گونهای بین مدلهای حیوانی و انسان، پیچیدگی میکرومحیط تومور و متغیرهای بالینی متعدد (مانند نوع سرطان، مرحله بیماری، درمانهای قبلی و وضعیت ایمنی بیمار) همگی بر قابلیت تعمیم نتایج تأثیر میگذارند. بنابراین مطالعات آینده باید نمونهبرداری دقیق از بافتهای انسانی، تحلیلهای چندپارامتری و کارآزماییهای بالینی کنترلشده را شامل شوند تا مشخص شود کدام بیماران از تغییرات در رویکرد جراحی یا استفاده از تقویتکنندههای گره لنفاوی سود میبرند.
دیدگاه کارشناسان
«این پژوهش یادآور اهمیت گستردهٔ شرایط میکرومحیطی فراتر از خود تومور است»، گفت دکتر میرا پاتل، پزشک-پژوهشگر در حوزه ایمونوانکولوژی با تجربه در درمانهای سلولی (نقش فرضی). «حفظ یا تقویت درمانی عملکرد گره لنفاوی میتواند راهی عملی برای افزایش درصد بیمارانی باشد که از مهارکنندههای چکپوینت و درمانهای CAR-T سود میبرند.» این نظر بر امکان همراستا کردن روشهای جراحی و درمانهای ایمنی برای دستیابی به نتایج بهتر تاکید میکند.
کارشناسان ایمنیشناسی و جراحی سرطان معمولاً اشاره میکنند که تصمیمگیری در مورد برداشت گره لنفاوی باید مبتنی بر ارزیابی چندبعدی ریسک متاستاز در برابر منافع بلندمدت ایمنی بیمار باشد. اطلاعات جدید از دوهرتی احتمالاً این توازن را پیچیدهتر میکند، اما در عین حال فرصتهایی برای نوآوری در استراتژیهای درمانی و طراحی کارآزماییهای بالینی ایجاد میکند. بهعنوان نمونه، آزمایشی میتواند بررسی کند آیا بیماران مبتلا به سرطانهای ویژه که گرههای لنفاوی آنها حفظ شده، پاسخ به مهارکنندههای PD-1 یا PD-L1 بهتری نشان میدهند یا خیر.
از منظر فناوری، ترکیب مهندسی بافت، دارورسانی هدفمند و ایمنیشناسی مولکولی میتواند راهحلهایی ارائه دهد که در آن حتی پس از برداشت گره لنفاوی، محیط حمایتی مصنوعی یا جایگزین بازتولید شود. بهعنوان مثال، ایمپلنتهای زیستی یا حاملهای نانوذرهای که سیگنالهای بازدارندهٔ خستگی یا محرک تکثیر را ارائه میدهند، میتوانند نقش گره را برای مدتی شبیهسازی کنند و زمان کافی برای تولید پاسخ ایمنی مؤثر فراهم آورند.
نتیجهگیری
یافتههای موسسه دوهرتی گرههای لنفاوی را بهعنوان محلهای حیاتی آموزش ایمنی معرفی میکند که سلولهای T شبیه-بنیادین را نگهداری میکنند و از این طریق بنای پاسخهای مؤثر ضدتومور را فراهم میسازند. در صورت تأیید در مطالعات بالینی، این کار میتواند روشهای جراحی در سرطان را بازنگری کرده و الهامبخش درمانهای نوینی شود که زیستشناسی گره لنفاوی را هدف میگیرند تا پاسخ به ایمنوتراپی را بهبود بخشند. پژوهشهای آتی باید این مکانیسمها را در بافتهای انسانی تأیید کنند و مداخلاتی را طراحی کنند که بدون بهخطرانداختن کنترل سرطان، محیط حمایتی گره لنفاوی را حفظ یا بازسازی نمایند.
در پایان، ترکیب دادههای مولکولی، مدلهای بالینی و فناوریهای نوظهور میتواند نقشه راهی ایجاد کند که طی آن تصمیمات جراحی، برنامهریزی درمانی و طراحی داروها هماهنگ شوند تا بیشترین سود ممکن برای بیماران سرطان حاصل شود. این مسیر نیازمند همکاری میانتخصصی بین جراحان، ایمونولوژیستها، آنکولوژیستها و مهندسان زیستپزشکی است تا نتایج آزمایشگاهی به راهکارهای عملی و قابل اجرا در کلینیک تبدیل شود.
منبع: scitechdaily

ارسال نظر