10 دقیقه
نامرئی برای گوشهای ما اما قدرتمند در کلینیک، اولتراسوند متمرکز بهعنوان یک روش غیرتهاجمی در درمان اختلالات مغزی و سرطان در حال ظهور است. پیشرفتهای اخیر به پزشکان امکان میدهد انرژی صوتی متمرکز را روی حجمهای بسیار کوچک بافت هدف بگیرند تا موانع را باز کنند، داروها را وارد مغز سازند، پاسخهای ایمنی را تحریک کنند و در بعضی موارد بافت بیمار را تخریب نمایند — همه بدون برش جراحی یا پرتو درمانی. این روش بهتدریج در درمانهای عصبی و انکولوژی نقش عملیتر و بالینیتری یافته است.
How focused ultrasound harnesses inaudible sound
اولتراسوند از امواج صوتی فراتر از محدوده شنوایی انسان برای تولید تصاویر پزشکی و بهطور فزایندهای برای درمان بیماریها استفاده میکند. یک ترانسدیوسر سیگنالهای الکتریکی را به ارتعاشات مکانیکی تبدیل میکند؛ این امواج در بدن حرکت کرده، از مرزهای بافت منعکس میشوند و بهصورت اکو به ترانسدیوسر بازمیگردند که سپس توسط کامپیوترها به تصاویر قابل مشاهده تبدیل میگردند. اما زمانی که همان امواج در یک هدف کوچک — اغلب حجمی به کوچکی یک دانه برنج — متمرکز میشوند، اثرات مکانیکی و حرارتی آنها تغییر میکند. اولتراسوند متمرکز میتواند بافت را گرم کند، به دیواره رگها فشار وارد کند یا باعث نوسان حبابهای گازی ریز معلق در جریان خون شود. این اثرات زمینهساز استراتژیهای درمانی متعددی میشوند که شامل گرمادهی موضعی، باز کردن انتخابی موانع فیزیولوژیک و تشدید پاسخ ایمنی است.
سیستمهای اولتراسوند متمرکز هدایتشده با MRI لایه دیگری از کنترل را فراهم میآورند. تصویربرداری به پزشکان اجازه میدهد هدف را در زمان واقعی ببینند، تغییرات دمایی را پایش کنند و دهها تا هزاران پرتوی صوتی کوچک را هدایت کنند تا دقیقاً در نقطه موردنظر همگرا شوند. آزمایشهای اولیه بیش از هشتاد سال پیش نشان دادند که اولتراسوند متمرکز میتواند بافت مغز را نابود کند — مشابه متمرکز کردن نور خورشید با ذرهبین — اما سالها بهبود در تصویربرداری، آرایههای ترانسدیوسر و مدلسازی آکوستیک لازم بود تا پزشکان بتوانند بهطور قابلاطمینان و ایمن از این روش در مغز استفاده کنند.
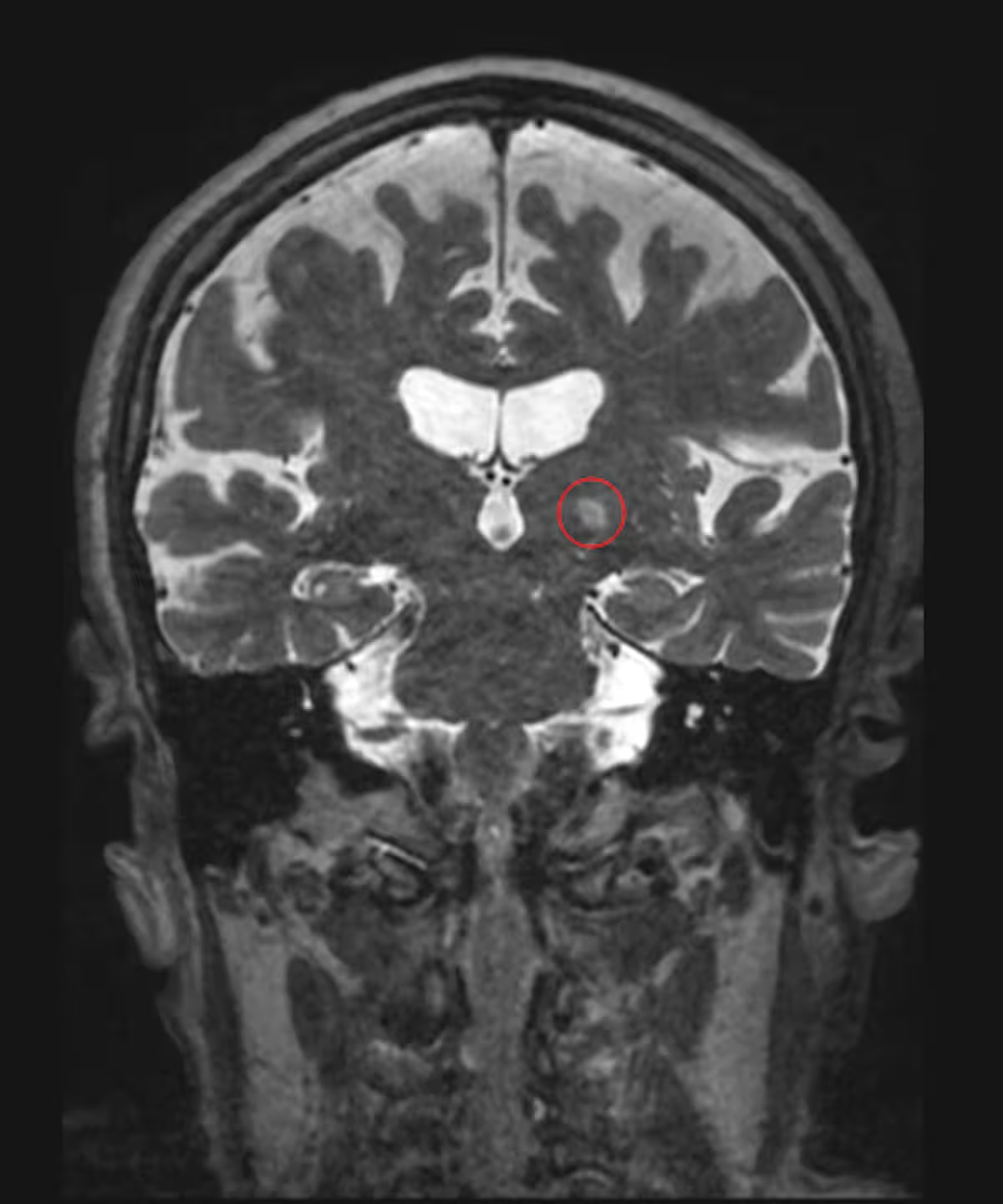
تصویربرداری MRI از بیمانی که برای لرزش اساسی با اولتراسوند متمرکز درمان شده است، بخشی از مغز هدفگذاریشده با دایره قرمز مشخص شده است. (Jmarchn/Wikimedia Commons, CC BY-SA)
Opening the blood-brain barrier — a targeted door for medicines
پرده خونی–مغزی (BBB) یک سپر سلولی بهشدت تنظیمشده است که با محدود کردن عبور موادی از گردش خون به بافت عصبی، مغز را محافظت میکند. این محافظت در عین حال مانع عبور بسیاری از داروها، مولکولهای بزرگ و درمانهای ژنی به مناطق بیمار میشود. اولتراسوند متمرکز راهحلی انتخابی ارائه میدهد: پالسهای با شدت پایین که به نقطه مشخصی هدفگیری میشوند باعث میشوند میکروبابلهایی که در خون حضور دارند نوسان کنند. نوسان این میکروبابلها بهطور موقت اتصالات محکم دیواره رگ را شل میکند و منافذ نانومتری ایجاد مینماید که عاملهای درمانی میتوانند از طریق آن وارد مغز شوند — اما تنها در محلی که اولتراسوند اعمال شده است.
باز شدن هدفمند BBB در مطالعات حیوانی و کارآزماییهای انسانی اولیه تایید شده است. پژوهشگران از اولتراسوند متمرکز برای افزایش انتقال شیمیدرمانی به گلیوبلاستوم و متاستازهای مغزی استفاده کردهاند و بهمنظور افزایش غلظت درمانهای آزمایشی ابتلا به آلزایمر در نواحی درگیر مغز نیز تحقیقاتی انجام شده است. مطالعات موازی نویدبخش انتقال ناقلهای ویروسی و سایر حاملهای درمان ژنی هستند که معمولاً نمیتوانند از BBB عبور کنند، و این امید را تقویت میکند که درمانهای ژنتیکی برای بیماریهای نورودژنراتیو و اختلالات تکاملی مغز به هدف عملیتری تبدیل شود.
Why this matters
- دقت: تنها ناحیه هدفگیریشده با اولتراسوند نفوذپذیر میشود و این امر عوارض سیستمیک را کاهش میدهد.
- قابلیت تکرار: این فرایند را میتوان چندین بار تکرار کرد و امکان دوزبندی مرحلهای یا تقویتکنندهها (booster) را فراهم میآورد.
- سازگاری: اولتراسوند متمرکز میتواند روشهای موجود درمانی و دارویی را تکمیل کند و لزوماً جایگزین آنها نشود.
Wakening the immune system: ultrasound plus immunotherapy
بسیاری از تومورهای جامد به لحاظ ایمنی «سرد» هستند: آنها سلولهای ایمنی را جذب نمیکنند یا سیگنالهای اندکی برای تحریک حمله ارائه میدهند. اولتراسوند متمرکز میتواند این وضعیت را تغییر دهد. با ایجاد اختلال مکانیکی در تومور یا گرمادادن کنترلشده آن، اولتراسوند سلولهای تومور را به قطعات تبدیل کرده و آنتیژنهای توموری را آزاد میسازد. این قطعات ممکن است به غدد لنفاوی منتقل شوند، جایی که سلولهای ایمنی یاد میگیرند تومور را شناسایی و هدفگیری کنند؛ فرایندی که میتواند اثربخشی ایمنیدرمانیهای سیستمیک را افزایش دهد.
آزمایشگاهها و برنامههای بالینی اولیه در حال بررسی ترکیب اولتراسوند متمرکز با مهارکنندههای نقطه بازرسی (checkpoint inhibitors) و سایر ایمنیدرمانیها هستند. هدف، تبدیل تومورهای سرد — مانند برخی انواع سرطان پانکراس، پستان و مغز — به تومورهای داغی است که به داروهای مبتنی بر پاسخ ایمنی سیستمیک واکنش نشان میدهند. در سال 2022 دانشگاه ویرجینیا مرکزی ویژه برای تسریع پژوهشهای ایمونوآنکولوژی با استفاده از اولتراسوند متمرکز راهاندازی کرد و کارآزماییهای آزمایشی ترکیب اولتراسوند با ایمنیدرمانیها برای ملانوما پیشرفته و سایر سرطانها آغاز شده است.
Examples in practice
- آبلاسیون مستقیم: اولتراسوند متمرکز با شدت بالا (HIFU) میتواند تومورهای کوچک را بهصورت حرارتی نابود کند بدون اینکه برش جراحی لازم باشد.
- آمادهسازی ایمنی: اولتراسوند زیرآبلاسیون (sub-ablative) میتواند آنتیژنها و سیگنالهای التهابی را آزاد نموده و شناسایی ایمنی را افزایش دهد.
- تحویل دارو: باز کردن موضعی عروق با اولتراسوند تحویل موضعی شیمیدرمانیها یا داروهای آنتیبادی را بهبود میبخشد.
Beyond common diseases: rare disorders and structural lesions
در حالی که سرطان و آلزایمر بخش عمدهای از توجه را به خود جلب کردهاند، اولتراسوند متمرکز همچنین پتانسیل کاربرد در اختلالات نادر عروقی و ضایعات ساختمانی مغزی را دارد. یکی از نمونهها ناهنجاری غار مانند مغزی (cerebral cavernous malformation یا CCM) است، وضعیتی که در آن سلولهای عروقی بهطور غیرطبیعی تکثیر میشوند و ضایعات شکنندهای ایجاد میکنند که ممکن است خونریزی یا تشنج ایجاد کنند. جراحی اغلب استاندارد مراقبت است، اما برخی ضایعات عمیق یا نزدیک بافتهای حیاتی قرار دارند و عمل جراحی مخاطرهآمیز است.
تحقیقات پیشبالینی نشان میدهد که اولتراسوند متمرکز میتواند هم انتقال دارو به CCMها را بهبود بخشد و هم — بهطرز شگفتآوری — رشد ضایعه را در مدلهای حیوانی تثبیت کند حتی بدون دارودرمانی همزمان. مکانیسم دقیق هنوز در دست بررسی است، اما این مشاهده جراحان مغز و اعصاب را ترغیب کرده تا کارآزماییهای مرحله اولیه بالینی برنامهریزی کنند. اگر این نتایج در انسان نیز تکرار شود، اولتراسوند متمرکز میتواند گزینهای کمتهاجمیتر برای مدیریت برخی CCMها و سایر ضایعات دسترسیناپذیر مغزی فراهم آورد.
Technical hurdles, safety and the path to wider adoption
اولتراسوند متمرکز درمانی عمومی نیست که برای همه کاربردها مشابه عمل کند. شکل و چگالی جمجمه میتواند امواج صوتی را دفرمه کند، که نیازمند مدلهای آکوستیک فردی و آرایههای بزرگ چندعنصری ترانسدیوسر برای جبران این تغییرات است. پایش دما و تصویربرداری زمان واقعی برای تضمین ایمنی بیمار و جلوگیری از صدمات ناخواسته ضروری است. علاوه بر این، تاییدیههای نظارتی وابسته به کارآزماییهای بیماریمحور هستند که نه تنها ایمنی بلکه سود بالینی معنیدار نسبت به استانداردهای موجود را نشان دهند.
با وجود این موانع، صدها کارآزمایی بالینی در سراسر جهان برای آزمون اولتراسوند متمرکز در کاربردهای مختلف عصبی و انکولوژیک آغاز شدهاند. لرزش اساسی در بسیاری از مراکز بهطور روتین با اولتراسوند درمان میشود و کارآزماییهای در حال انجام هدفهای متعددی مانند گلیوبلاستوم، بیماری متاستاتیک مغز، آلزایمر و چندین حالت نادر سیستم عصبی مرکزی را دنبال میکنند. در هر مورد بالینی، طراحی پروتکلهای دقیق برای پایش بیومتریکها و نتایج عملکردی ضروری است.
Future directions: combining technologies for smarter therapies
جالبترین چشماندازها از جفتسازی اولتراسوند متمرکز با مدالیتههای نوظهور بهدست میآید: نانوبلورها و نانوذرات هدفمند، ناقلهای ویرایش ژن و ایمونوتراپیهای پیشرفته. تصور کنید ابزارهای CRISPR دقیقاً به تومور یا ناحیه مغزی مبتلا تحویل داده شوند، یا از اولتراسوند برای هدایت محمولههای نانوذرات استفاده شود که تنها پس از باز شدن BBB دارو آزاد کنند. این رویکردهای ترکیبی وعده افزایش اثربخشی را با محدود کردن سمیت سیستمیک میدهند.
مهندسین همچنین در حال کوچکسازی سیستمهای اولتراسوند و بهبود هدایت پرتو هستند، که ممکن است امکان درمانهای سرپایی یا در مطب را فراهم آورده و دسترسی را فراتر از مراکز تخصصی گسترش دهد. با بالغتر شدن مدلهای آکوستیک، تصویربرداری و سامانههای بازخورد زمان واقعی، پزشکان کنترل تنگتری بر مکان و چگونگی اثر اولتراسوند در مقیاس سلولی و مولکولی خواهند داشت.
Expert Insight
«اولتراسوند متمرکز یک جعبهابزار است، نه یک درمان واحد»، دکتر النا مورالس، مهندس زیستپزشکی که با تیمهای بالینی در توسعه دستگاهها همکاری میکند، میگوید. «نقاط قوت آن دقت و انعطافپذیری است — میتوان انرژی را تنظیم کرد تا پرده خونی-مغزی را باز کند، بافت را بهاندازه کافی گرم کند تا سلولهای تومور از بین بروند، یا نیروهای مکانیکی ایجاد نماید که سیستم ایمنی را هوشیار سازد. چالش کنونی ادغام هوشمندانه آن با داروها و بیولوژیکها برای حل مشکلات واقعی بالینی است.»
ارزیابی او بازتاب دیدگاهی گستردهتر در پژوهش ترجمهای است: بیشترین ارزش اولتراسوند متمرکز ممکن است بهعنوان یک فناوری توانمندساز باشد که سایر درمانها را کارآمدتر میسازد.
What patients and clinicians should know now
برای بیمارانی که در جستجوی درمان با اولتراسوند متمرکز هستند، مهم است بپرسند آیا درمان بخشی از یک پروتکل تاییدشده است یا در قالب یک کارآزمایی بالینی اجرا میشود، خطرات شناختهشده برای آن رویه خاص چیست و تیم چگونه پایش و پیگیری پس از درمان را انجام خواهد داد. برای پزشکان، ادغام اولتراسوند متمرکز در عمل بالینی مستلزم همکاری بین رشتهای — جراحی مغز و اعصاب، رادیولوژی، انکولوژی، مهندسی و ایمونولوژی — برای طراحی کارآزماییهایی است که سود بالینی را بهطور شفاف اندازهگیری کنند.
اولتراسوند متمرکز بهسرعت از یک کنجکاوی فیزیکی تجربی به یک فناوری بالینی مرتبط تبدیل شده است. دهه آینده مشخص خواهد کرد که آیا وعدههای آن — تحویل هدفمند دارو و ژن، فعالسازی ایمنی علیه تومورها و گزینههای درمانی ایمنتر برای بیماریهای نادر مغزی — به نتایج پایدار برای بیماران منجر خواهد شد یا خیر. در هر صورت، ترکیب پژوهش دقیق، توسعه فناوری و کارآزماییهای بالینی مبتنی بر شواهد برای تحقق پتانسیل کامل این فناوری حیاتی خواهد بود.
منبع: sciencealert


ارسال نظر