8 دقیقه
پژوهشگران دریافتند ریلمنییدین، دارویی که معمولاً برای درمان فشار خون بالا تجویز میشود، میتواند طول عمر را در حیوانات آزمایشگاهی افزایش دهد و نشانگرهای سلامت را بهبود بخشد. به نظر میرسد این دارو در سطح سلولی شبیه یک تقلیدکننده محدودیت کالریک عمل کند — یافتهای که امیدها را برای بازاستفاده از داروهای موجود به منظور کند کردن برخی جنبههای پیری بدون پیروی از رژیمهای سخت کالریک افزایش میدهد. این نتایج میتواند راه را برای پژوهشهای بیشتر درباره داروهای ضدپیری و مداخلههای تقویتکننده سلامت هموار کند.
From worms to mice: surprising signs of longevity
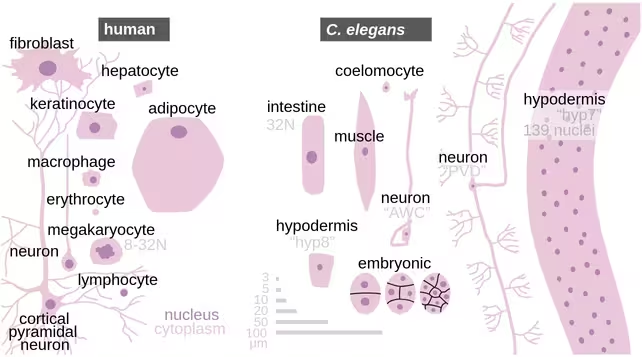
در آزمایشهایی که با Caenorhabditis elegans انجام شد — نماتد میکروسکوپیای که بهطور گسترده در پژوهشهای پیری بهکار میرود — کرمهای جوان و پیر که با ریلمنییدین درمان شدند، عمر طولانیتری داشتند و در چند شاخص سلامت فیزیولوژیک بهبود نشان دادند. این اثرات شباهت زیادی به فواید ناشی از محدودیت کالریک داشت؛ مداخلهای شناختهشده که طول عمر را در گونههای مختلف افزایش میدهد اما پایایی آن برای انسان دشوار است و میتواند عوارضی مانند نازک شدن مو، سرگیجه و کاهش تراکم استخوان را به همراه داشته باشد. در این مطالعه، پژوهشگران نه تنها بقا را ردیابی کردند، بلکه مجموعهای از نشانگرهای بیولوژیک و عملکردی را نیز بررسی کردند تا تصویر جامعتری از سلامت حیوانات فراهم آید.
«برای اولین بار توانستیم در حیوانات نشان دهیم که ریلمنییدین میتواند طول عمر را افزایش دهد»، گفت ژان پدرو ماگالهاس، زیستشناس مولکولی و متخصص بیوجرونتولوژی از دانشگاه بیرمنگام. مطالعهای که در نشریه Aging Cell منتشر شد، فعالیت ژنی و تغییرات فیزیولوژیک را پیگیری کرد که حالتهایی مشابه با وضعیت ناشی از محدودیت کالریک را منعکس میکردند. این نوع مطالعاتِ ترکیبی که از معیارهای مولکولی تا عملکردی را بررسی میکنند، به درک بهتر مکانیسمهای زیرین کمک میکنند و اعتمادپذیری نتایج را افزایش میدهند.
How rilmenidine may mimic calorie restriction
در سطح مولکولی، به نظر میرسد ریلمنییدین سیگنالدهی انرژی سلولی را به گونهای تغییر میدهد که با مسیرهای فعالشده در محدودیت کالریک همپوشانی دارد. پژوهشگران تغییرات مشابهی در بیان ژن در بافتهای کلیه و کبد موشهایی که دارو را دریافت کرده بودند مشاهده کردند، که نشان میدهد اثر ریلمنییدین محدود به نماتدها نیست و ممکن است در پستانداران نیز عمل کند. این همبستگی بین گونهها اهمیت بالقوه دارو را برای تحقیقات ترجمهای افزایش میدهد.
یافته برجستهای شامل گیرندهای موسوم به nish-1 بود. وقتی محققان ژن nish-1 را حذف کردند، اثرات افزایش طول عمر ریلمنییدین از بین رفت. بازگرداندن nish-1 آن مزایا را دوباره پدید آورد، که نشان میدهد این هاب سیگنالدهی ممکن است هدفی مناسب برای توسعه درمانهای ضدپیری آینده باشد. نتایج چنین آزمایشهایی نشان میدهد که اثرات دارو وابسته به مسیرهای خاصی است و نه صرفاً نتیجهٔ تغییرات غیرمستقیم یا سمی.
در چارچوب مکانیسمهای شناختهشده مرتبط با پیری، مسیرهایی مانند mTOR، AMPK و اتوفاژی (autophagy) معمولاً در مطالعات محدودیت کالریک دخیل گزارش شدهاند. ریلمنییدین ممکن است با تعدیل متابولیسم سلولی، بهینهسازی استفاده از انرژی و افزایش پاکسازی مولکولها و اندامکهای معیوب از طریق اتوفاژی، برخی از مزایای محدودیت کالریک را تقلید کند. با این حال، لازم است مطالعات مکانیکی بیشتری انجام شود تا ارتباط دقیق بین ریلمنییدین و این مسیرهای سیگنالی بهطور قطعی روشن گردد.

Why repurposing drugs matters for aging research
توسعه داروهای جدید از پایه فرایندی زمانبر و پرهزینه است؛ در مقابل، بازاستفاده از داروهایی که قبلاً برای مصارف دیگر تأیید شدهاند، میتواند مسیر ورود به آزمایشهای بالینی را تسریع کند. ریلمنییدین به دلایل عملی جذاب است: تجویز خوراکی دارد، به شکل گستردهای تجویز شده و معمولاً به خوبی تحمل میشود. عوارض گزارششده نسبتا نادر و اغلب خفیفاند — مانند تپش قلب، بیخوابی و خوابآلودگی در اقلیتی از بیماران — که این ویژگیها آن را به گزینهای مناسب برای مطالعات بالینی طولانیمدت تبدیل میکند.
با این وجود، انتقال نتایج از نماتدها و موشها به درمانهای انسانی هیچگاه تضمینشده نیست. C. elegans بسیاری از مسیرهای ژنتیکی حفاظتشده را با انسان به اشتراک میگذارد، به همین دلیل در پژوهشهای پیری کاربرد فراوانی دارد، اما همچنان فاصله تکاملی و پیچیدگیهای فیزیولوژیک بین گونهها چالشی واقعی است. دادههای موشی، استدلال را قویتر میکنند، اما برای ارزیابی ایمنی و اثربخشی ریلمنییدین بهعنوان یک مداخله ضدپیری در انسان، به آزمایشهای انسانی بزرگ و کنترلشده نیاز است. علاوه بر آن، مسائل دوزینگ، تداخلهای دارویی، اثرات در گروههای سنی و جنسیتی مختلف، و پیامدهای بلندمدت باید با دقت بررسی شوند.
Lessons from related drugs
داستان ریلمنییدین در چارچوب علاقه فزاینده به داروهای بازاستفادهشده قرار میگیرد. برای مثال، تحلیلهای مشاهدهای روی متفورمین — داروی شناختهشده دیابت — نشان دادهاند در برخی جمعیتها بقا یا بُعد سالمندی طولانیتری وجود داشته است. یک مطالعه طولانیمدت در ایالات متحده روی زنان پس از یائسگی نشان داد زنانی که متفورمین مصرف میکردند در برخی تحلیلها ریسک کمتری برای مرگ قبل از 90 سال داشتند نسبت به زنانی که داروی دیگری برای دیابت مصرف میکردند، هرچند از دادههای مشاهدهای نمیتوان رابطه علّی را مستقیماً نتیجه گرفت.
این یافتهها هم وعده و هم محدودیت رویکرد بازاستفاده را برجسته میکنند: مجموعهدادههای مشاهدهای بزرگ میتوانند کاندیداها را مشخص کنند، اما برای اثبات منافع واقعی در زمینه پیری یا طول عمر، آزمایشهای تصادفیشده کنترلشده (RCT) لازم و حیاتیاند. علاوه بر این، یافتههای مشاهدهای باید با بررسیهای مکانیکی و مدلهای حیوانی پشتیبانی شوند تا علتیابی و درک اثرات جانبی احتمالی بهبود یابد.
What’s next for rilmenidine research?
دانشمندان در حال برنامهریزی مطالعات پیشبالینی بیشتر برای ترسیم دقیق مسیرهایی هستند که ریلمنییدین از طریق آنها عمل میکند، و نیز برای آزمایش دامنه دوزها و اثرات بلندمدت در مدلهای پستاندار. اگر نتایج همچنان امیدوارکننده باقی بماند، گام بعدی طراحی و اجرای آزمایشهای انسانی با دقت بالاست تا مشخص شود آیا این دارو میتواند بهصورت ایمن مدت «سلامتمحوری» (healthspan) — یعنی سالهایی که فرد در سلامت خوب به سر میبرد — را بدون ریسکهای غیرقابلقبول افزایش دهد یا خیر. طراحی چنین کارآزماییهایی باید شامل معیارهای بالینی و مولکولی، گروههای سنی متنوع، پیگیری بلندمدت و ارزیابی دقیق عوارض و تعاملات دارویی باشد.
«با جمعیت پیرشونده جهانی، فواید به تأخیر انداختن پیری، حتی بهاندازهای اندک، عظیم است»، اشاره کرد ماگالهاس. «بازاستفاده از داروهایی که قادر به افزایش طول عمر و طول دوران سلامت هستند، پتانسیل بزرگی در علم ترجمهای پیری دارد که هنوز بهطور کامل مورد بهرهبرداری قرار نگرفته است.» این دیدگاه تاکید میکند که ترکیب دادههای تجربی، تحلیلهای مولکولی و مطالعات بالینی میتواند راهی مؤثر برای توسعه درمانهای ضدپیری قابل قبول و عملی فراهم آورد.
Expert Insight
دکتر النا رویز، محقق گرواساینس که در مطالعه دخیل نبود، اظهار داشت: «این یافتهها امیدوارکنندهاند چون مسیرهای متابولیک محافظتشده را هدف قرار میدهند. اما افزایش طول عمر در حیوانات همیشه نتایج انسانی را پیشبینی نمیکند. تمرکز کنونی باید بر روی مطالعات مکانیکی باشد که بتوانند آزمایشهای بالینی هدفمند و ایمن را اطلاعرسانی کنند. اگر دارویی مانند ریلمنییدین بتواند بهطور ایمن مزایای مشابه محدودیت کالریک را بازتولید کند، میتواند پزشکی پیشگیرانه برای سالمندان را دگرگون کند.»
در حال حاضر ریلمنییدین نشانهای وسوسهانگیز ارائه میدهد: ممکن است داروهای موجود پتانسیلهای غیرمنتظرهای برای تنظیم زیستشناسی پیری داشته باشند. مسیر از کرم تا کلینیک طولانی است، اما این پژوهش یک مورد ارزشمند دیگر به فهرست نامزدهای درمانی طول عمر اضافه میکند و چارچوبی برای مطالعات بعدی فراهم میآورد. برای رسیدن به نسخههای کاربردی بالینی، ترکیب تحقیقات مولکولی، مطالعات پیشبالینی گستردهتر و کارآزماییهای انسانی دقیق ضروری خواهد بود.
منبع: sciencealert
نظرات
ماکس_
شبهه دارم؛ شبیه هیاهو ولی اگر بشه بدون رژیم سخت سالهای سالم بیشتری داشت که عالیه. هنوز تبلیغاتیو قبول ندارم، صبر لازم داریم.
مهدی
من تو آزمایشگاه خوندم که خیلی از داروها خواص غافلگیرکننده دارن، دیدن اثر روی نماتد و موش خوشحال کننده ست، ولی به چشم انسان باید محتاط بود.
بیونیکس
تحلیل جالب، مخصوصا وقتی که nish-1 حذف میشه اثر از بین میره. اما از کرم تا انسان کلی فاصله هست، لازم ددلاین مطالعات مکانیکی و RCT
توربو
این واقعیه؟ یعنی ریلمنییدین واقعا عمر رو زیاد میکنه؟ بعید نیست اما خیلی چیزا باید مشخص بشه، دوز، تداخل دارویی، خطرات بلندمدت...
دیتاپالس
وای، از کرم تا موش، یعنی واقعا یک قرص ممکنه مثل رژیم غذا عمل کنه؟ امیدوارم آزمایشهای انسانی هم بهتر پیش برن…


ارسال نظر