8 دقیقه
تصور کنید قرصی وجود داشته باشد که نیرویش را دقیقاً روی کبد و روده متمرکز کند تا یک کلید متابولیک را خاموش کند و سپس شاهد کاهش چشمگیر چربیهای خون باشیم. این وعده اکنون در تحقیقات کاردیومتابولیک برانگیخته شده است؛ پس از آزمایشهای اولیه روی انسان، ترکیب خوراکی TLC-2716 در یک کارآزمایی کوتاهمدت بیش از ۶۰ درصد کلسترول باقیمانده (remnant cholesterol) را کاهش داد و تریگلیسیرید را نزدیک به ۴۰ درصد پایین آورد.
چگونه دانش ژنتیکی به درمان هدفمند انجامید
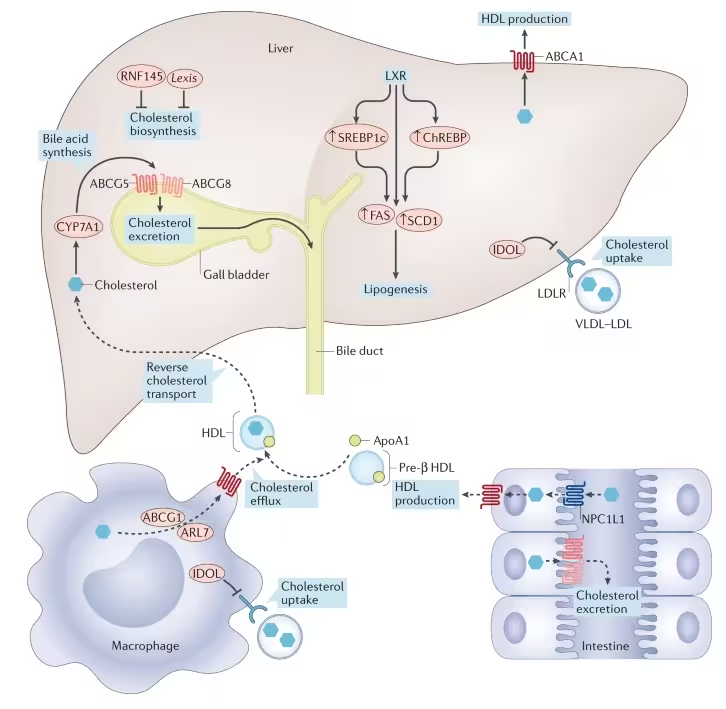
مسیر منتهی به TLC-2716 از دادههای ژنتیکی آغاز شد. محققانی که مجموعههای بزرگ داده انسانی را بررسی میکردند، ژن NR1H3 را که پروتئینی به نام گیرنده X کبدی آلفا (LXRα) را رمزگذاری میکند، بهعنوان تنظیمکنندهای کلیدی در مدیریت لیپیدها در کبد و روده شناسایی کردند. با استفاده از روش تصادفیسازی مندلی (Mendelian randomization) — تکنیکی که از تنوع ژنتیکی طبیعی برای استنتاج روابط علی بهره میگیرد — پژوهشگران نشان دادند که افزایش بیان NR1H3 با سطوح بالاتر تریگلیسیرید، تغییرات در کلسترول HDL و نشانگرهایی از بیماری کبدی همراه است.
LXRα در نقطهای کنترلی برای سنتز و حملونقل چربی قرار دارد. فعالسازی گستردهٔ این گیرنده میتواند مسیرهای مفید حذف کلسترول را در سلولهای ایمنی تحریک کند، اما همزمان تولید چربی در کبد و روده را نیز افزایش دهد. این دوگانگی از مدتها پیش یکی از مشکلات اساسی حوزه بوده است: چگونه میتوان اثرات مضرِ ایجاد چربی را مهار کرد بدون اینکه نقشهای محافظتی این گیرنده در بافتهای دیگر از بین برود؟
استراتژی تیم تحقیقاتی مبتنی بر «فضاییسازی» بود. بهجای بلاککنندهای که در تمام بدن اثر کند، آنها ترکیبی را طراحی کردند که فعالیتش محدود به کبد و روده باشد. مطالعات پیشبالینی در جوندگان، ارگانوئیدهای کبدی بیمار انسانی و نخستیسانان غیرانسانی نشان داد که TLC-2716 یک نامزد متناسب است که لیپوژنز کبدی (سنتز چربی در کبد) را کاهش میدهد، جذب چربی غذایی را کند میکند و پاکسازی لیپیدهای گردشکننده را افزایش میدهد — در حالی که عملکرد LXR را در بافتهای خارج از این ناحیه حفظ میکند.
آزمایش انسانی اولیه: یافتههای کارآزمایی
در یک کارآزمایی فاز ۱ تصادفیشده که در نشریه Nature Medicine منتشر شده است، حدود ۱۰۰ داوطلب سالم بالغ به مدت ۱۴ روز روزانه دوزهای خوراکی TLC-2716 یا دارونما دریافت کردند. این مطالعه که توسط یوهان آوِرکس در EPFL هدایت شد و بخشی از آن توسط شرکت بیوتکنولوژی OrsoBio تأمین مالی شد، بر فارماکولوژی، ایمنی و اثرات متابولیک کوتاهمدت متمرکز بود. طراحی تصادفی و کنترلشده و توجه به پارامترهای ایمنی، مقدمات محکمی برای ارزیابی اولیه فراهم آورد.
نتایج برای یک آزمایش انسانی اولیه چشمگیر بود. رژیمهای با دوز بالا تریگلیسیرید ناشتا را تا ۳۸.۵ درصد کاهش دادند. کلسترول باقیمانده — بخشی آترودرموژنیک که پس از وعدههای غذایی در گردش باقی میماند — در اندازهگیریهای پس از غذا تا ۶۱ درصد افت کرد. شرکتکنندگان در ابتدا پروفایلهای لیپیدی نرمال داشتند و از داروهای کاهشدهنده لیپید دیگری استفاده نمیکردند. در گروههای دوز، دارو گزارش شد که ایمن و بهطور کلی قابلتحمل بوده است؛ رویدادهای ناخواسته جدی گزارش نشده یا محدود به موارد خفیف تا متوسط بودهاند.
چرا کاهش کلسترول باقیمانده اهمیت دارد؟ زیرا این بقایای لیپوپروتئینی غنی از تریگلیسیرید هستند و بهراحتی وارد دیواره رگها میشوند و در شکلگیری بیماریهای عروقی آترواسکلروتیک (ASCVD) نقش دارند. آنها همچنین در پانکراتیت حاد و بیماری کبدی استئاتویک مرتبط با اختلال متابولیک (MASLD) درگیرند؛ اصطلاحی نوین برای آنچه پیشتر بهطور متداول «کبد چرب غیرالکلی» نامیده میشد. کاهش این فرکشنهای آترژنیک میتواند بار مخاطره قلبی-عروقی را کم کند و پیامدهای کبدی و التهابی مرتبط را اصلاح نماید.
مسیر خوراکی ترکیب نیز یک مزیت عملی است. یک قرص موثر که روزانه یک بار مصرف شود میتواند درمان را ساده کند، هزینهها را نسبت به بیولوژیکهای تزریقی کاهش دهد و بهراحتی با درمانهای تثبیتشده کاهشدهنده لیپید مانند استاتینها یا فرمولههای امگا-۳ ترکیب شود. این مزیت ترکیبی برای پذیرش بالینی و دسترسی بیماران اهمیت دارد، بهخصوص در جمعیتهایی که تداوم درمان و پذیرش تزریق محدود است.
پیامدها، احتیاطها و مسیر پیشرو
این سیگنالهای اولیه امیدوارکنندهاند، اما احتیاط لازم است. کارآزماییهای فاز ۱ برای ارزیابی ایمنی و فارماکولوژی در گروههای کوچک و معمولاً سالم طراحی شدهاند؛ آنها اثبات سودمندی بلندمدت در بیماران مبتلا به بیماری نیستند. تیم تحقیقاتی اشاره کرده است که بهبودهای متابولیک مشاهدهشده در داوطلبانی با سطوح نرمال لیپید ممکن است در افرادی که واقعاً هیپرترایگلیسیریدمی یا MASLD دارند، تشدید شود؛ اما این فرضیه نیازمند آزمایش در جمعیتهای بیمار است.
گامهای بعدی زمانبَر خواهد بود: مطالعات با مدتزمان طولانیتر در افراد دارای اضافهوزن یا چاقی با تریگلیسیرید بالا و بیماری کبد چرب، تعیین دوز بهینه در جمعیتهای متنوع، و پایش دقیق برای هرگونه اثرات ناخواسته خارج از هدف در صورت خروج مولکول از بخش کبد–روده. نظارت دقیق بر بیومارکرهای کبدی، آنزیمها، و شاخصهای التهابی، و همینطور ارزیابی پیامدهای قلبی-عروقی بلندمدت، برای تایید اثربخشی ضروری خواهد بود.
نظارت تنظیمی بر ترکیبی مانند TLC-2716 بر هر دو محور تمرکز خواهد کرد: اثربخشی در برابر پیامدهای سخت — مانند تعداد کمتر حملات قلبی، پیشرفت کمتر بیماری کبدی یا کاهش نیاز به بستریهای مرتبط — و ایمنی پایدار در استفاده طولانیمدت. بحثهای مربوط به تعاملات دارویی (drug–drug interactions) با استاتینها، فیبراتها، یا مکملهای امگا-۳ نیز باید بهطور کامل بررسی شوند، زیرا این ترکیبها میتوانند در عمل بالینی با هم تجویز شوند.
از منظر توسعه دارویی، چالشهای تولید، پایداری فرمولاسیون خوراکی، و تضمین اختصاصی بودن اثر در بافت هدف (tissue selectivity) از نظر فارماکودینامیک و فارماکوکینتیک اهمیت دارد. اگر مولکول در برخی افراد از غشاءهای مخاطی روده یا سدهای سلولی عبور کند و در بافتهای غیرهدف تجمع یابد، احتمال خطر تولید چربی در بافتهای دیگر یا اثرات ایمنی غیرقابل انتظار مطرح میشود.
دیدگاه کارشناسان
«آنچه TLC-2716 را جالب میکند، انتخابپذیری آن در سطح بافت است»، دکتر النا روسی، داروشناس کاردیومتابولیک در دانشگاه میلان میگوید. «هدفگیری LXRα تنها در جاهایی که موجب تولید مضر چربی میشود، از رویکرد چکشوار که تلاشهای قبلی را منحرف کرد، جلوگیری میکند. اگر این نتایج در بیماران مبتلا به دیسلیپیدمی تکرار شود، میتوانیم با یک کلاس جدید از درمانهای خوراکی روبهرو باشیم که مکمل عوامل موجود هستند نه جایگزین آنها.»
محققان تأکید میکنند که منافع متابولیک سازگار و مشاهدهشده — چه در داوطلبان انسانی و چه در مدلهای حیوانی — توجیهکننده ادامه آزمایشهای بالینی هستند. برای پزشکان و بیماران که با افزایش شیوع MASLD و خطر قلبی-عروقی ناشی از بقایای لیپوپروتئینی مواجهاند، یک تنظیمکننده LXRα متمرکز بر کبد و روده نمایی نو بر مسئلهای قدیمی ارائه میدهد.
در حال حاضر، TLC-2716 یک ترکیب آزمایشی باقی میماند. اما مفهومی که نمایندگی میکند — تعدیل هدفمند بافتی یک سوئیچ متابولیک مرکزی — ممکن است نحوهٔ تفکر دانشمندان دربارهٔ درمان اختلالات لیپیدی پیچیده را بازتعریف کند؛ و این مسیر باید با گامهایی سنجیده و مبتنی بر دادههای بالینی گسترده طی شود. اگرچه نتایج اولیه امیدوارکنندهاند، اما اثبات ایمنی و اثربخشی بلندمدت در جمعیتهای پرخطر و بیمار شرط لازم برای دستیابی به کاربرد بالینی است.
منبع: sciencealert
نظرات
کوینپیل
من تو مطب بیماران MASLD دیدم، اگه واقعا تریگلیسرید رو ~۳۸٪ کم کنه کلی مشکل حل میشه، ولی تداخل با استاتین و طول درمان باید دقیق بشه
پمپزون
خب دادهها قوی به نظر میان اما احساس میکنم کمی اغراقه؛ باید ببینیم در جمعیتهای بیمار و دورههای طولانی چی میشه، مراقب اثرات جانبی باشن
آرمین
نتایج اولیه امیدوارکننده ان ولی فازهای طولانیتری لازمه. قرص خوراکی ایدهآل برای ترکیب با استاتین به نظر میاد، اگر ایمن بمونه
بیونیکس
آیا واقعاً میشه LXRα رو فقط تو کبد و روده محدود کرد؟ نکنه در عمل اثرات خارج از هدف داشته باشه، مثل افزایش لیپوژنز جاهای دیگه؟
دیتاپالس
وای... ۶۰٪ کاهش کلسترول باقیمانده؟! یعنی یه قرص بتونه اینقدر؟ امیدوارم عواقب بلندمدتش روشن بشه

ارسال نظر