8 دقیقه
ماکروفاژها را مانند تیم نظافتگر بدن در نظر بگیرید: آنها زبالهها را پاک میکنند، عناصر حیاتی را بازیافت میکنند و بهصورت خاموش عملکرد ارگانها را تنظیم میکنند. اما چه کسی آن تیم را آموزش میدهد؟ پژوهشهای اخیر نشان میدهد یک تنظیمکننده ژنتیکی واحد است که دستورالعملهای عملکردی این سلولها را در اختیارشان قرار میدهد.
محققان دریافتهاند عاملی ژنتیکی به نام MafB بهعنوان سوئیچ اصلی عمل میکند که هویت ماکروفاژها و توانایی آنها برای محافظت از بافتها را شکل میدهد. در صورت فقدان این فاکتور، این سلولهای حیاتی ایمنی نمیتوانند بهطور کامل بالغ شوند و در نتیجه فرایندهایی از بازسازی آهن تا سلامت ریه و کلیه دچار اختلال میشود.
از مونوسیت تا ماکروفاژ بالغ: گرهچینی نقش MafB
زیر میکروسکوپ، بلوغ ماکروفاژها مانند یک نمایش هماهنگشده بهنظر میرسد. مونوسیتهای خونی وارد بافت میشوند و بسته به نشانههای محلی، نقشهای تخصصی متفاوتی را بهعهده میگیرند. MafB، یک فاکتور رونویسی، در طول این گذار بهتدریج افزایش پیدا میکند. او تنها نیست؛ MafB شبکهای گسترده از ژنها را هماهنگ میکند که ژنهای لازم برای فاگوسیتوز، پاکسازی زباله و نگهداری بافت را فعال مینمایند. اگر MafB حذف شود، بسیاری از این کلیدها هرگز روشن نمیشوند؛ سلولها در حالت تعلیق باقی میمانند: حاضرند اما مجهز نیستند.
این وضعیت تعلیق پیامدهایی دارد. در آزمایشهایی که توسط آزمایشگاه ایمنوفیزیولوژی دانشگاه لیژ رهبری شد، سلولهای فاقد MafB از نظر مورفولوژیک نابالغ بهنظر میرسیدند — گردتر، شاخهدار کمتر و از نظر عملکردی دچار نقص بودند. این تغییرات مورفولوژیک با کاهش بیان ژنهای اختصاصی بلوغ، کاهش ظرفیت فاگوسیتوز و کاهش بیان گیرندههای پاککننده (scavenger receptors) همراه بود.
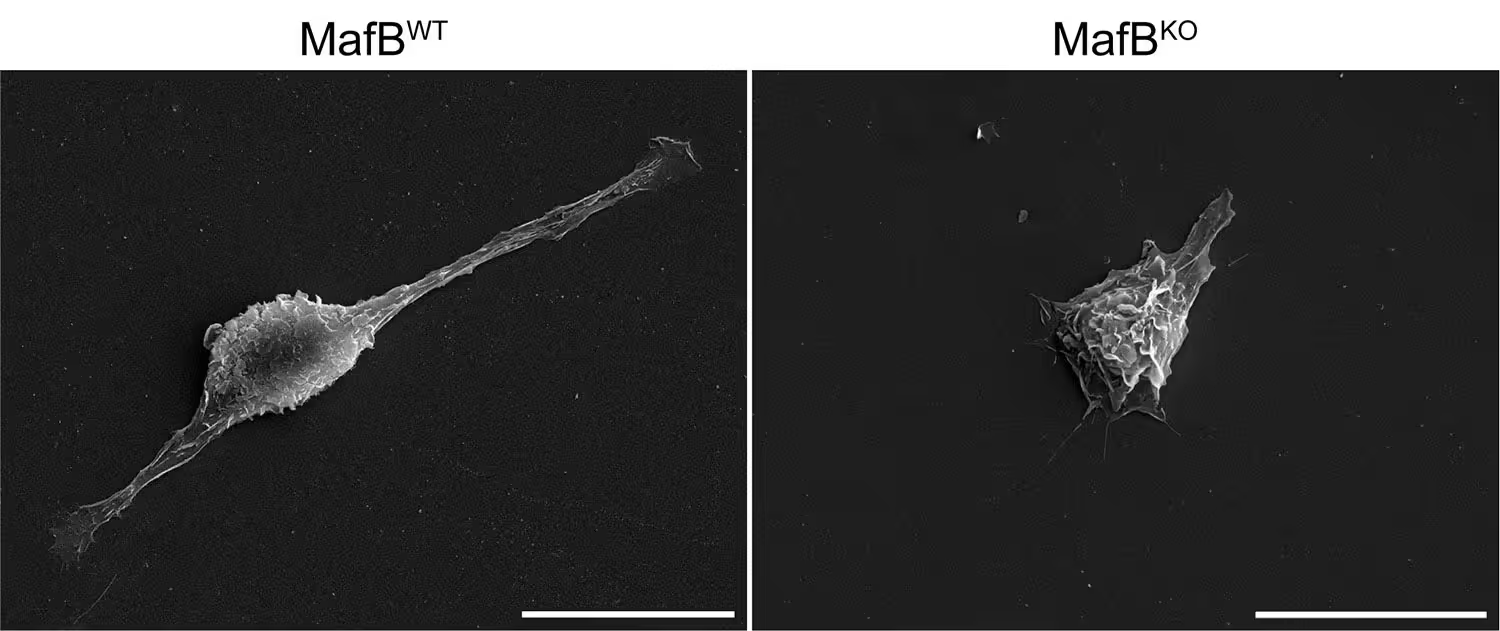
ماکروفاژهایی که MafB دارند (WT) ظاهری بالغ و منظم دارند، در حالی که آنهایی که فاقد MafB هستند (KO) گرد و کمتر توسعهیافته بهنظر میرسند.
چرا این موضوع اهمیت دارد؟ چون ماکروفاژها بیش از مبارزه با عفونت انجام میدهند. آنها آهن را از گلبولهای قرمز پیریشده منتقل میکنند، ماتریکس خارجسلولی را بازسازی میکنند و سیگنالهای متابولیک میفرستند که به متعادلنگهداشتن ریهها، کلیهها، روده و طحال کمک میکنند. یک تنظیمکننده سراسری مانند MafB هویتی محافظتشده فراهم میآورد تا ماکروفاژها بتوانند بهطور محلی سازگار شوند در حالیکه قابلیتهای اصلی را در سراسر بافتها و گونهها حفظ کنند.
حفظ تکاملی و اثرات سیستمیک
هرچه بیشتر وارد ژنوم میشوید، الگوی روشنتری پدیدار میشود. MafB شبکهای از ژنها را کنترل میکند که در موشها و انسانها یافت میشود و در میان مهرهداران بازتاب دارد. این حفاظت تکاملی نشاندهنده یک اصل بیولوژیک است: بدن برنامه ژنتیکی مشترکی را بهکار میگیرد تا بازیگرانی سلولی قابلاعتماد در هر نقطهای که نیاز است تولید کند.
وقتی این برنامه شکست بخورد، اثرات موجمانندی بهصورت اختلال در عملکرد ارگانها ظاهر میشود. تیم دانشگاه لیژ اختلال در بازسازی آهن در طحال و نقصهای ظریف اما قابل اندازهگیری در ریهها، روده و کلیه را زمانی مشاهده کردند که بلوغ ماکروفاژها متوقف شده بود. این نشانهها در سطح ارگان یک نکته مهم را برجسته میکنند: هویت سلول ایمنی، فیزیولوژی را شکل میدهد، نه صرفاً دفاع در برابر پاتوژنها.
از منظر تکاملی، حضور یک فاکتور مرکزی مانند MafB احتمالاً به بقا کمک کرده است: داشتن یک ستون فقرات ژنتیکی پایدار اجازه میدهد تا ماکروفاژها با سیگنالهای محلی هماهنگ شوند اما بدون از دست رفتن کارکردهای پایهای. این سازوکار در گونههای مختلف و شرایط محیطی متعدد کارایی زیستی را تضمین میکند.
از منظر بالینی، زاویه دیگری نیز وجود دارد. اختلالات مزمن مانند فیبروز، التهاب مزمن، بیماریهای متابولیک و برخی عفونتها در هسته خود دچار نقصهایی در عملکرد ماکروفاژها هستند. اگر MafB یا مسیرهای مهم پاییندستی آن قابل اصلاح باشند، پژوهشگران میتوانند توانایی ماکروفاژها را بازیابند و به تبع آن ترمیم بافت و هموستاز را بهبود بخشند. این مسیر طولانی است اما دارای نشانگرهای مولکولی روشنی است که راه را مشخص میکنند.
فنون و شواهد
یافتهها ترکیبی از مدلهای ژنتیکی، پروفایلینگ تکسلولی و ژنومیک تطبیقی است. دنبالکردن بیان MafB هنگام تبدیل مونوسیتها به ماکروفاژهای ساکن بافت الگوی قابل بازتولیدی را نشان داد: افزایش MafB با فعالشدن ژنهای فاگوسیتوز و دیگر نشانگرهای عملکردی همبستگی داشت. مطالعههای loss-of-function بیشترین دادههای قانعکننده را ارائه کردند: حیواناتی که MafB را در ردههای میلوئیدی از دست داده بودند، ماکروفاژهایی داشتند که بسیاری از وظایف حیاتی خود را انجام نمیدادند و این ناکامیها در تغییرات قابل اندازهگیری فیزیولوژی ارگانها تبلور یافت.
متدهای مطرحشده شامل موارد زیر بودند:
- مدلهای موشی با حذف هدفمند MafB در خطوط میلوئیدی (مثلاً با استفاده از Cre-Lox که در سلولهای میلوئیدی فعال میشود).
- پروفایلینگ تکسلولی (single-cell RNA-seq) برای دنبالکردن مسیرهای تمایز و شناسایی زیرجمعیتهای ماکروفاژی.
- آنالیزهای اپیژنتیک مانند ATAC-seq برای سنجش تغییرات دسترسی کروماتین در طول بلوغ.
- آزمایشهای عملکردی: آزمونهای فاگوسیتوز، اندازهگیری بازسازی آهن در طحال، تستهای عملکردی ریه و ارزیابی نشانگرهای التهاب مزمن.
- ژنومیک تطبیقی برای مقایسه الگوهای تنظیمی MafB بین گونهها.
اینها تغییرات انتزاعی نیستند. نقص در بازسازی آهن میتواند هموستاز سرتاسری آهن را تغییر دهد و به کمخونی بیماریهای مزمن منجر شود. اختلالات ریوی و کلیوی ممکن است بافتها را به آسیب حساستر کنند. بهطور خلاصه، نقش MafB پل مابین زیستشناسی سلولی و سلامت کل بدن است.
پیامدها برای درمان و پژوهشهای آتی
هدفگیری یک تنظیمکننده اصلی جذاب اما ظریف است. فاکتورهای رونویسی مانند MafB در قلب بسیاری از برنامههای ژنتیکی قرار دارند؛ تغییر دادن آنها میتواند اثرات گستردهای داشته باشد. مسیر محتملتر در میانمدت شامل اثرگذارهای پاییندستی است — ژنها و مسیرهایی که MafB آنها را کنترل میکند و قابل داروشدن یا تعدیل بهصورت بافتمحور هستند. استراتژی دیگر بهرهگیری از درمان سلولی است: برنامهریزی ماکروفاژها در خارج از بدن به یک وضعیت بالغ و با بیان بالای MafB و سپس بازگرداندن آنها به محل نیازمند.
چندین سوال کلیدی هنوز بیپاسخ ماندهاند. چگونه سیگنالهای بافتی محلی با MafB تعامل میکنند تا تنوع شگفتانگیز فنوتیپهای ماکروفاژی را تولید کنند؟ آیا بازیابی جزئی برنامههای هدایتشده توسط MafB میتواند عملکرد ارگان را در مدلهای بیماری نجات دهد؟ و آیا فشارهای محیطی یا متابولیک این برنامه را بهگونهای مختل میکنند که سرعت پیشرفت بیماریهای مزمن را افزایش دهد؟
پیشروی در مسیر درمانی نیازمند چند اقدام همزمان است: شناسایی اهداف پاییندستی قابلدارو، توسعه روشهای تحویل بافتمحور (مانند نانوذرات یا حاملهای سلولی)، و آزمایش ایمنی در مدلهای حیوانی متعدد. همزمان، مطالعات پایه برای درک تعاملات اپیژنتیک و سیگنالینگ موضعی با MafB ادامه باید یابد تا از پیامدهای ناخواسته جلوگیری شود.
دیدگاه کارشناسی
دکتر النور واس، ایمنولوژیست و پژوهشگر ترجمهای، اینگونه عنوان میکند: "MafB یک نقطه تکیه بین هویت و عملکرد است. مدتها میدانستیم ماکروفاژها خود را با زیستگاههای محلی وفق میدهند؛ اکنون یک ستون فقرات ژنتیکی محافظتشده را میبینیم که آن سازگاری را قابل اعتماد میسازد. از منظر درمانی، چالش این است که به آن ستون احترام بگذاریم در حالیکه خروجیهایش را بهصورت گزینشی تنظیم میکنیم. این زیستشناسی دقیق در عمل است."
درک اینکه چگونه یک فاکتور رونویسی واحد میتواند چنین مسئولیتهای گسترده سلولی را هماهنگ کند، دید ما نسبت به سلولهای ایمنی را بازتعریف میکند. اینها مدافعان موقتی صرف نیستند؛ آنها نگهبانان برنامهریزیشدهای هستند. سوال کنونی این است که چگونه آن برنامهریزی را به درمانهایی تبدیل کنیم که عملکرد را حفظ میکنند بدون آنکه شبکهای را که تکامل بهدقت ساخته، بشکنند.
برای تقویت جنبههای عملیاتی این یافتهها، مسیرهای تحقیقاتی پیشنهادی عبارتاند از:
- تحقیقات میانرشتهای بین ژنتیک، ایمنیشناسی و بیوانفورماتیک برای یافتن اهداف پاییندستی قابلکنترل.
- توسعه مدلهای بیماری انسانی و حیوانی که تغییرات عملکردی ماکروفاژ را با خوانشهای بالینی مانند عملکرد تنفسی یا پارامترهای کلیوی مرتبط کنند.
- آزمونهای پیشبالینی سلولدرمانی که در آن ماکروفاژهای برنامهریزیشده از نظر MafB در مدلهای فیبروز یا التهاب مزمن تعبیه شوند.
- مطالعه اثرات محیطی و متابولیک (مثلاً دیابت، چاقی، کمخونی نقص آهن) بر برنامه MafB برای روشنکردن رابط بیماریهای مزمن و اختلال عملکرد ماکروفاژ.
این برنامه تحقیقاتی همسو با هدفگذاری دقیق و فهم عمیقتر از بیولوژی بنیادی میتواند راهی برای توسعه درمانهایی بسازد که بازسازی بافت و هموستاز را بدون ایجاد مخاطرات سیستمی بهبود میبخشند.
در مجموع، نقش MafB نه تنها برای دانش بنیادی در زیستشناسی ایمنی اهمیت دارد، بلکه پنجرهای رو به فرصتهای درمانی و تشخیصی میگشاید. شناخت و مهندسی این «پلیکیت» تنظیمی ممکن است تحولاتی در درمان بیماریهای التهابی، فیبروتیک و متابولیک ایجاد کند — مشروط بر آنکه به دقت و با درک کامل شبکههای پاییندستی دنبال شود.
منبع: scitechdaily
نظرات
امیر
خیلی بزرگش کردن انگار، ولی ایده جالبیه. منتظر دادههای درمانی و ایمنیسنجی هستم، اگه کار کنه عالیه...
سفررو
دیدگاه متعادل؛ هم فرصت داره هم ریسک. هدفگذاری بافتی و پاییندستی منطقیه، امیدوارم مطالعات بالینی هم بیاد
لابکور
من تو آزمایشگاه دیدم ماکروفاژای نابالغ عملکردشون حسابی افت میکنه, اما تغییر کنترلکننده مرکزی کار آسونی نیست
توربو
آیا این تو انسان هم برقرار هست؟ مدل موش یه چیزه، ترجمهپذیری به انسان سوالیه...
کوینکس
معقول بنظر میاد، هدف گرفتن مسیرهای پایین دست منطقی تره و ریسک کمتری داره، نه دستکاری خام سوئیچ اصلی
دیتاپالس
واقعا؟ یعنی یه تکفاکتور میتونه اینقدر تاثیر بذاره؟ شگفتانگیز اما یه ذره هم ترسناکه... کلی سوال بیپاسخ!

ارسال نظر