9 دقیقه
شگفتانگیز، ساده و سرسختانه: کمتر خوردنِ کالری در طول سالها میتواند سیمکشی عصبی مغز را کندتر پیر کند. این پیشنهاد چشمگیر از یک آزمایش طولانیمدت نشأت میگیرد که شرکتکنندگان را در طول تمام طول عمرشان دنبال کرده و با بررسی بافت مغز در سطح سلولی، نشانههایی از تفاوتهای پیری را ثبت کرده است.
یک مطالعه چند دههای نشان میدهد که محدودیت کالری مداوم ممکن است روند پیری مغز را در سطح سلولی تغییر دهد. با تحلیل تکهستهای RNA در سلولهای مغزی مجزا، پژوهشگران دریافتند کاهش میزان کالری با عوامل کلیدی در حفظ یکپارچگی ماده سفید مغز مرتبط است؛ نتایجی که برای بحثهایی درباره تغذیه، سلامت عصبی و پیشگیری از بیماریهای نورودژنراتیو اهمیت دارد.
کاهش کالری بلندمدت و تابآوری مغز
با افزایش سن، نورونها تنها عملکرد خود را از دست نمیدهند؛ سامانههای پشتیبان اطراف آنها نیز فرسوده میشوند. میلین—لایه چربیای که آکسونها را میپوشاند و امکان انتقال سریع سیگنال عصبی را فراهم میکند—به تدریج تخریب میشود. میکروگلیاها، نگهبانان ایمنی مغز، میتوانند از نقش پاککننده و سازنده به وضعیت فعال و التهابی مزمن تبدیل شوند. نتیجه این تغییرات: کندی در ارتباط بین سلولها، شکنندگی ماده سفید و افزایش حساسیت به بیماریهای نورودژنراتیو مانند آلزایمر و بیماریهای موتور عصبی است.
دانشکده پزشکی چوبانیان و آودسیان دانشگاه بوستون مدارکی گزارش کرده است که کاهش حدود 30 درصدی کالری، که بهطور مستمر بیش از دو دهه در یک مدل تجربی نخستیسانها اعمال شده بود، با نشانههای مولکولی حفظ سلامت مغز مرتبط بوده است. تیم تحقیقاتی دو گروه را در طول طول عمر طبیعیشان دنبال کرد—یکی با رژیم غذایی متعادل و کالری معمول، و دیگری با برنامه محدودیت کالری منظم—و پس از مرگ تحلیلهای دقیق پستمورتوم انجام داد تا «سجل سلولی» نوشتهشده طی سالها را بخواند. این مدل طولانیمدت در نخستیسانها امکان بررسی تغییرات زمانمند در بافت مغزی را فراهم ساخت که در گونههای کوتاهعمرتر کمتر قابل ردیابی است.
پژوهشگران چه بررسی کردند و چه یافتند
برای نگاه عمیق به داخل هر سلول، تیم از «توالییابی RNA تکهستهای» استفاده کرد؛ روشی که فعالیت ژنی را به ازای هر هسته بهصورت جداگانه اندازه میگیرد. این امکان به آنها میداد تا الگوهای بیان ژنی را بین انواع سلولی مختلف مقایسه کنند: نورونها، الیگودندرُسیتها (سلولهایی که میلین تولید میکنند)، میکروگلیا و سایر سلولهای پشتیبان مانند آستروسیتها. تفاوتها جزئی نبودند. سلولهای گروه محدودیت کالری بیان بالاتری از ژنهای مرتبط با تولید میلین نشان دادند و فعالیت بیشتری در مسیرهای متابولیک مرکزی—بهویژه گلیکولیز و بیوسنتز اسیدهای چرب—داشتند؛ مسیرهایی که سوخت و ساز و نگهداری ساختار میلین را تأمین میکنند.
چرا این موضوع اهمیت دارد؟ زیرا میلین یک پوشش غیرفعال نیست؛ ساخت و ترمیم آن از نظر متابولیک هزینهبر است. اگر ماشینآلاتی که زیرساختها و انرژی لازم را فراهم میکنند دچار اختلال شوند، یکپارچگی میلین کاهش مییابد، انتقال سیگنال کند میشود و فرایندهای شناختی که به هماهنگی سریع نورونی وابستهاند کارایی خود را از دست میدهند. الیگودندرُسیتها نه تنها غلاف میلین را میسازند، بلکه در تأمین متابولیتهایی مانند لاکتات برای آکسونها نقشی حیاتی دارند؛ بنابراین پشتیبانی متابولیک آنها برای سلامت ماده سفید ضروری است.
مطالعه همچنین تغییراتی را در نمایههای میکروگلیا مشاهده کرد. بهجای نشانگرهای فعالسازی مزمن که معمولاً در فرایند پیری دیده میشود، میکروگلیاهای نمونههای محدودیت کالری الگوی بیانی را حفظ کردند که نشاندهنده نظارت ایمنی متعادلتر بود. به عبارت دیگر: التهاب پایدار کمتر و محیط سلولیای که احتمال نگهداری و تعمیر را بیشتر از آسیبرسانی فراهم میکند.
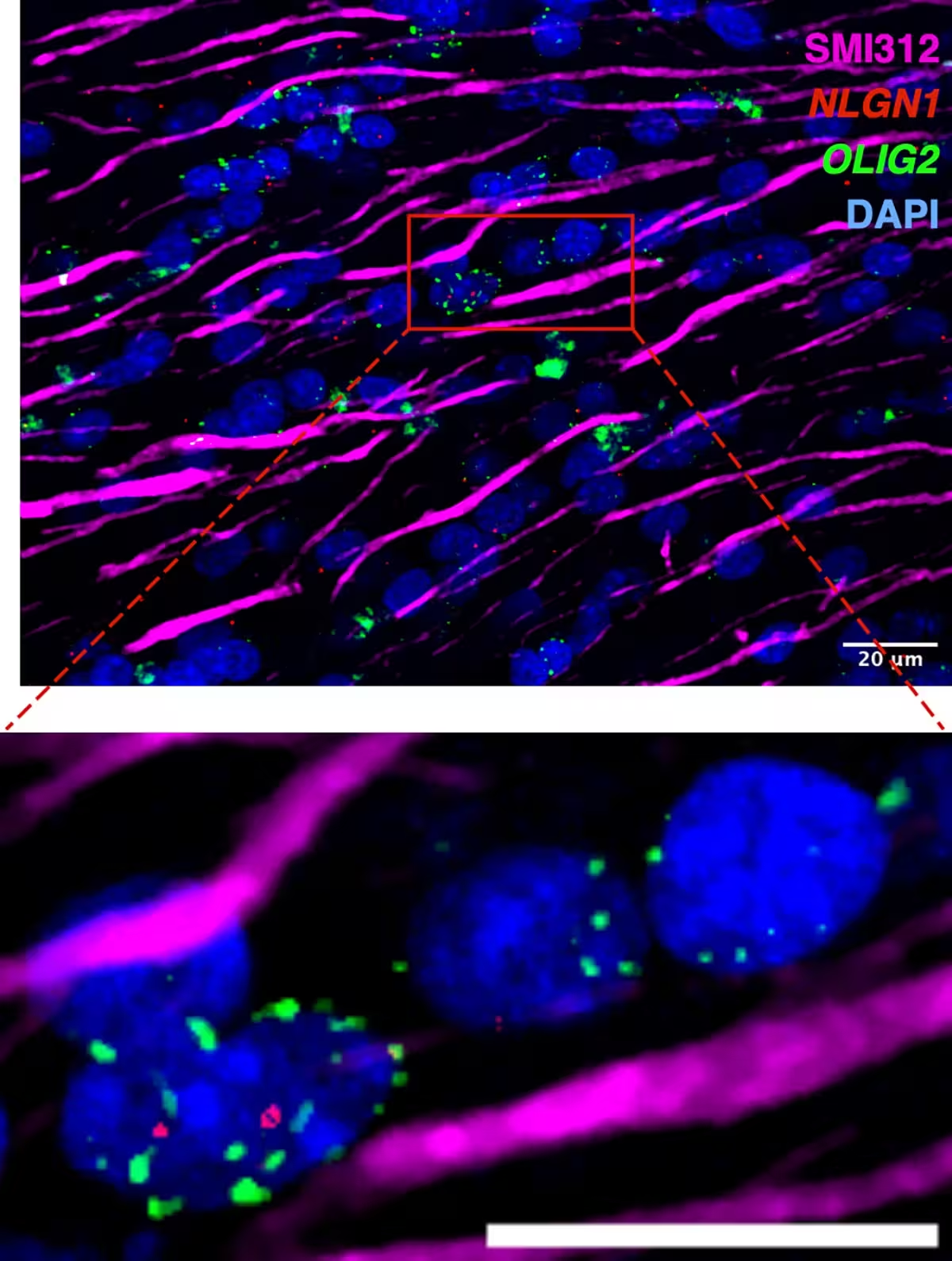
الیاف عصبی آکسونی (به رنگ ماژنتا) که توسط سلولهای پشتیبان مغز احاطه شدهاند، هستههای آنها به رنگ آبی رنگآمیزی شده است. نُقطههای سبز نشاندهنده RNA پیامرسان OLIG2 هستند که الیگودندرُسیتها را شناسایی میکند؛ همان سلولهایی که غلاف محافظ میلین را دور رشتههای عصبی تشکیل میدهند. نُقطههای قرمز NLGN1 را نشان میدهند، مولکولی که به الیگودندرُسیتها کمک میکند تا با رشتههای عصبی ارتباط برقرار کنند. معمولاً با افزایش سن سطح NLGN1 کاهش مییابد و تشکیل میلین دچار اختلال میشود. با این حال، پژوهشگران دریافتند که محدودیت کالری بلندمدت به حفظ بیان NLGN1 کمک میکند و درنتیجه ممکن است عایقبندی و ارتباط سالم بین اعصاب را حفظ نماید.
نویسندگان اصلی مقاله اهمیت وسیعتری را برجسته کردند. آنا ویتانتونیو، نویسنده مسئول و دانشجوی دکتری، اشاره کرد که هرچند محدودیت کالری مدتهاست که در گونههای کوتاهعمرتر اثرات طول عمر و متابولیکی نشان داده است، این کار شاهدی نادر و پایدار فراهم میآورد که نشان میدهد امضاءهای مولکولی محافظتی مشابه در بافت مغزی یک مدل طولانیعمر و پیچیده نیز پدیدار میشود. تارا ال. مور، دکترای علوم و همنویسنده، بر پیامدهای شناختی تأکید داشت: اگر تولید میلین و سامانههای پشتیبانی متابولیکی قویتر باقی بمانند، پایه سلولی لازم برای یادگیری و حافظه ممکن است بهتر حفظ شود.
البته دارای ملاحظاتی نیز هست. این یک مدل تجربی است، نه یک کارآزمایی تصادفی انسانی. محدودیت کالری در انسان سوالات عملی درباره تغذیه، تبعیت از رژیم و عوارض ناخواسته ایجاد میکند: خطر کمبود مواد مغذی، تحلیل توده عضلانی، تغییرات هورمونی و تفاوتهای جنسیتی که امکان دارد بر نتایج اثرگذار باشند. با این وجود، سیگنالهای سلولی—افزایش بیان ژنهای مرتبط با میلین، حفظ مسیرهای متابولیک و کاهش فعالسازی بیش از حد میکروگلیا—ارتباط مکانیکی قابلباوری بین رژیم غذایی و نحوه گذران مغز از زمان ارائه میدهند.
دیدگاه کارشناسی
«دیدن اینکه مسیرهای متابولیک مرتبط با نگهداری میلین در پاسخ به تغییرات رژیمی بلندمدت واکنش نشان میدهند، قانعکننده است،» دکتر لِنا کارتر، پژوهشگر علوم عصبی و مروج علمی (شخصیتی ساختگی اما با چهارچوب واقعی)، میگوید. «این موضوع یک پایه مکانیکی در اختیار ما میگذارد: مداخلاتی که تأمین انرژی و بیوسنتز لیپید در سلولهای گلیایی را پایدار نگه دارند میتوانند به سلامت بهتر ماده سفید منجر شوند. رژیم تنها یکی از اهرمهاست—ورزش، خواب و سلامت عروقی نیز اهمیت دارند—اما این مطالعه یادآوری میکند که آنچه طی دههها میخوریم میتواند مسیرهای سلولی را بازنویسی کند.»
قدمهای بعدی روشناند: بررسی اینکه آیا الگوهای مولکولی مشابه در انسانهایی که کاهش کالری سنجیده و تحت نظارت تغذیهای دارند پدیدار میشود یا خیر؛ کاوش در استراتژیهای رژیمی کمتر شدید یا متناوب که منفعتهای مشابه ایجاد کنند؛ و جستوجو برای مداخلات دارویی یا سبک زندگی که بدون نیاز به محدودیت طولانیمدت شدید، امضاءهای محافظتی را تقلید نمایند. ابزارهایی مانند تصویرسازی رزونانس مغناطیسی با حساسیت به ماده سفید (DTI)، بیومارکرهای خونپایه و تجزیه RNA تکهستهای در نمونههای انسانی میتوانند برای اثبات ارتباط علت-معلولی و اندازهگیری منافع بالقوه بهکار گرفته شوند.
برای اکنون، پیام ظریف است. کاهش کالری حدود سی درصد برای سالها در این ثبت تجربی بلندمدت به نظر میرسد که برخی جنبههای مولکولی پیری مغز را کند میکند—بهویژه با حمایت از سلولها و مسیرهایی که میلین را میسازند و نگه میدارند و با بازداشتن سلولهای ایمنی از لغزش به فعالسازی التهابی مزمن. این یادآور است که پیری صرفاً نتیجه شمارش سالها نیست؛ بلکه شکل میگیرد توسط دههها انتخاب متابولیک و گفتگوهای سلولیای که آن انتخابها برمیانگیزند.
از منظر سلامت عمومی و پژوهش بالینی، این نتایج لایهای از پرسشها و فرصتها را باز میکنند: آیا میتوان نشان داد کاهش کالری ایمن و موثر برای انسانهاست؟ چه گروههایی (مثلاً جنسیتها، سنین مختلف، وضعیت متابولیک پایه) بیشترین سود را خواهند برد؟ آیا مداخلات تغذیهای کوتاهمدت یا نوسانی میتوانند همان امتیازات را بدون ریسکهای بلندمدت فراهم کنند؟ پژوهشهای آینده باید این پرسشها را با ترکیب مطالعات حیوانی، مداخلات بالینی کنترلشده و ارزیابیهای مولکولی و تصویربرداری پاسخ دهند.
در نهایت، این یافتهها برای مباحث مربوط به پیشگیری از زوال شناختی و سلامت ماده سفید مغز اهمیت دارند. ترکیب دانش از زیستشناسی سلولی—مانند نقش الیگودندرُسیتها در سوخترسانی آکسونها—با دادههای بلندمدت رفتاری و تصویربرداری میتواند چارچوبی فراهم آورد تا راهکارهای تغذیهای و غیردرمانی را بهگونهای طراحی کنیم که با هدف تقویت مقاومت مغز در برابر پیری و بیماریهای نورودژنراتیو، اثرات سودمندی داشته باشند.
کلیدواژههای مرتبط در این بحث عبارتاند از: کاهش کالری بلندمدت، پیری مغز، سلامت ماده سفید، میلین، میکروگلیا، توالییابی RNA تکهستهای، گلیکولیز، بیوسنتز اسید چرب، مدلهای نخستیسان، و مداخلات تغذیهای. بهکارگیری این کلیدواژهها در مطالعات آینده و در ترجمه نتایج به آزمایشهای بالینی میتواند کمک کند تا ارتباط بین تغذیه و پیری سلولی مغز بهروشنی مشخص شود.
در کنار توصیههای پژوهشی، پیام عملی برای عموم این است که هرچند شواهد حیوانی امیدوارکنندهاند، تغییرات رژیمی شدید و بلندمدت در انسانها نیازمند نظارت پزشکی و توجه به نیازهای تغذیهای فردی است. رویکردهای محافظهکارانهتر مانند اصلاح کیفیت رژیم، افزایش مصرف اسیدهای چرب امگا-3، حفظ توده عضلانی از طریق تمرین مقاومتی، و ترکیب با عادات سالم دیگر (خواب مناسب، فعالیت بدنی منظم و کنترل فشارخون) احتمالاً مسیر عمل منطقیتری برای بهبود سلامت مغز در طول عمر فراهم میکنند.
منبع: scitechdaily
نظرات
اتو_ر
بیش از حد اغراق نشده؟ مطالعات نخستیسان امیدوارکنننده اما ترجمهاش به انسان پر از اما و اگره، امیدوارم آزمایش کنترل شده بیاد
دانیکس
تو خانوادهمون یه سالمند بود که رژیم و ورزش داشت، انگار هوشیاری بهتر موند؛ تجربه شخصیم کمه اما با این نتایج سازگار به نظر میاد 🙂
پمپزون
به نظرم معقولِ، توازن لازمه. نه افراط نه تفریط. رژیم طولانی سختِ، شاید راههای کمتر شدید هم کار کنن.
مهدی
منظورم اینه منطقیه؛ نگهداری میلین مهمه. اما کاهش شدید کالری برای همه مناسب نیست، بهتره برنامه ترکیبی و عملی طراحی بشه...
بیونیکس
واقعاً روی انسان هم صدق میکنه؟ شبیه خبر خوبه اما کلی متغیر داره تغذیه، جنسیت، ورزش... آزمایش بالینی لازمه
رودکس
واای، یعنی اگه واقعاً اینطور باشه، ۳۰٪ کمتر کالری جلوی پیری مغز رو میگیره؟ شوکه شدم، ولی ترس اینکه عضله از دست بره...


ارسال نظر