9 دقیقه
انگل مالاریا یک نقطهضعف دارد. کوچک، اما حیاتی. محققان پروتئینی را کشف کردهاند که انگلهای مالاریا برای شکلی نامتعارف از تقسیم سلولی به آن وابستهاند — و حذف این پروتئین پیشرفت آنها را متوقف میکند. این آسیبپذیری میتواند جهتگیری نسل بعدی استراتژیهای ضد مالاریا را رقم بزند.
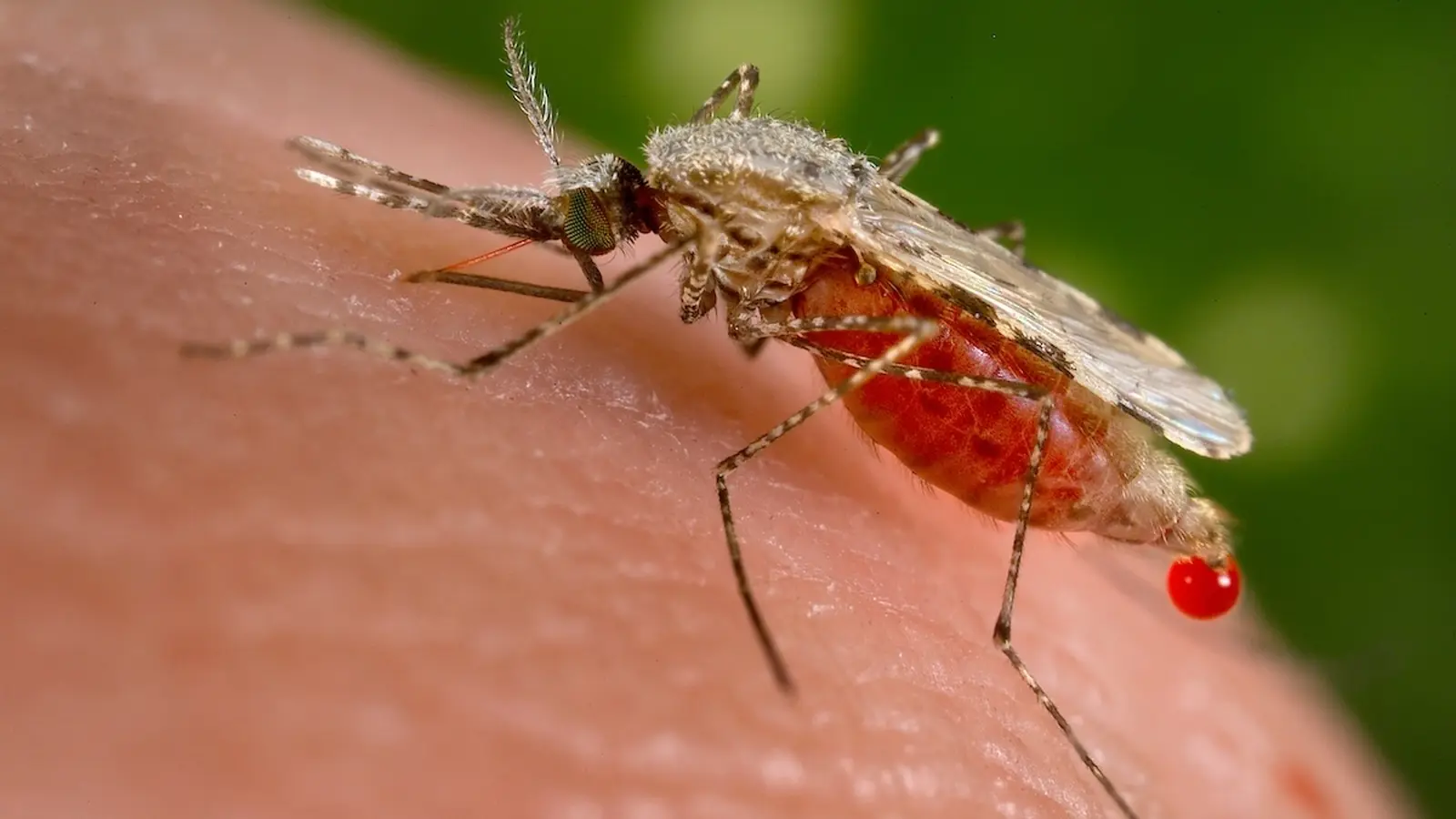
مالاریا همچنان قربانی میگیرد. در سال ۲۰۲۴ شمار قربانیان تقریباً به ۶۱۰٬۰۰۰ نفر رسید که بهطور نامتناسب کودکان در مناطق زیرصحرا آفریقا را درگیر میکند. واکسنها و اقدامات بهداشت عمومی تا حدی تأثیر گذاشتهاند، اما انگلهای پلاسمودیوم — یوکاریوتهای تکسلولی با تاریخچه تکاملی میلیونها ساله — همچنان سازگار شده و گسترش مییابند. از این رو پژوهشگران در پی یافتن نقاط ضعف مولکولی هستند که بتوان آنها را هدف قرار داد بیآنکه به انسان آسیب برسد.
چگونه آرک۱ چرخه سلولی نامتعارف را هدایت میکند
برخلاف سلولهای انسانی، پلاسمودیوم به روشهایی تقسیم میشود که زیر میکروسکوپ عجیب به نظر میرسند. میتوز در این انگل بازپخش دقیق کتابهای درسی تقسیم سلولی نیست. کروموزومها و ماشینآلات دوک تقسیم (spindle) بر اساس زمانبندی و ساختاری گرد هم میآیند و سپس از هم فرو میپاشند — معماریای که برای زیستشناسان سلولی انسانی غریب است. در میان این نمایش نامعمول پروتئینی وارد میشود که Aurora-related kinase 1 یا ARK1 نامیده میشود.
میتوان ARK1 را مانند یک کنترلکننده ترافیک هوایی داخل هسته انگل تصور کرد. این پروتئین به سازماندهی دوک میتوزی کمک میکند — چارچوب مولکولی که کروموزومهای تکثیرشده را جدا میکند — تا اطمینان حاصل شود که سلولهای دختر ژنومهای کامل را به ارث میبرند. اگر ARK1 غیرفعال شود، دوک بهدرستی تشکیل نمیشود. انگلها لکنت کرده و متوقف میشوند؛ آنها قادر نیستند چرخههای تکثیر لازم برای استقرار در میزبان انسان یا تکامل در پشه آنوفل را به پایان برسانند.
این نتیجه از آزمایشهایی بهدست آمد که از روشهای شرطی حذف یا سرکوب ژن استفاده کردند. با خاموشکردن انتخابی ARK1 در مراحل حیاتی زندگی انگل، محققان مشاهده کردند که تشکیل دوک بهطور گستردهای شکست میخورد و تکثیر انگل فروپاشی میکند. این اثر در مراحل مختلف زندگی آشکار بود: انگلها قادر به تکمیل توسعه درون سلولهای مهرهداران نبودند و پیشرفت آنها درون پشهها نیز متوقف شد. نتیجه خالص: پتانسیل انتقال بیماری بهشدت کاهش مییابد.

چرا تفاوت ساختاری برای طراحی دارو اهمیت دارد
یکی از جنبههای جذاب ARK1 این است که از کینازهای اورورا (Aurora kinases) در سلولهای انسانی بسیار متفاوت است. اختلاف در توالی و ساختار سهبعدی به معنی وجود یک پنجره درمانی بالقوه است — ترکیباتی که میتوانند پروتئین انگل را متصل کرده و مهار کنند بدون آنکه همتایان انسانی را مختل سازند. همانطور که ریتا تواری، زیستشناس سلولی انگل در دانشگاه ناتینگهام اشاره میکند، این واگرایی صرفاً موضوع نظری نیست؛ کاربردی است. اختصاصیبودن هدف خطر عوارض جانبی را کاهش میدهد که یکی از موانع اصلی توسعه داروهای ضدانگلی است.
ریوجی یاناسه، یکی از نویسندگان مشترکِ اصلی مطالعه، این کشف را مانند طلوع نوری تازه بر جنبهای پیشتر مبهم از زیستشناسی انگل توصیف کرده است. این تشبیه مناسب است: شناسایی پروتئینی که هم ضروری است و هم ساختاری متفاوت دارد، نقطهی اتکایی در اختیار شیمیدانهای دارویی قرار میدهد تا مهارکنندگانی طراحی کنند که بهطور مستقیم ماشینآلات چرخه زندگی انگل را هدف بگیرند.
هدفگیری ماشینآلات میتوزی در پزشکی نویدهای تازه نیست — درمانهای ضدسرطان بهطور روتین از این رویکرد استفاده میکنند — اما تقسیم نامتعارف پلاسمودیوم نیازمند تفکری تازه است. یک ترکیب بهینهشده برای برهمزدن عملکرد ARK1 باید مراحل مختلف چرخه زندگی انگل را در میزبان و ناقل در نظر بگیرد، جایگاههای درون سلولی آن را بشناسد و احتمال ظهور مقاومت را لحاظ کند. با این وجود، ترکیب عملکرد اساسی و تفاوت ساختاری، ARK1 را به هدفی جذاب برای داروهای ضدمالاریا تبدیل میکند.
جنبههای فنی و روششناسی
برای درک دقیقتر نقش ARK1، تیمهای تحقیقاتی از مجموعهای از فنون مولکولی و سلولی استفاده کردند. سیستمهای حذف ژن شرطی (conditional knockout)، سرکوب موقتی بیان (knockdown)، و ویرایش ژن با ابزارهایی مانند CRISPR/Cas9 یا سیستمهای نوترکیباسیون شرطی به پژوهشگران اجازه میدهد تا ARK1 را در مراحل خاصی از چرخه زندگی انگل خاموش کنند و سپس پیامدهای آن را در مقیاس سلولی و مورفولوژیک بررسی نمایند. این رویکردها، همراه با میکروسکوپی فلورسانس پیشرفته و نشانگرهای میکروتوبول و کروماتین، تصویر دقیقی از اختلال در تشکیل دوک و تقسیم کروموزومی فراهم کردند.
افزون بر این، تحلیلهای پروتئومیک و تعیین تعاملات پروتئینی آرک۱ (protein–protein interaction mapping) به شناسایی همراهان مولکولی این کیناز کمک کرد — پروتئینهایی که ممکن است در همان مسیر بیولوژیک قرار داشته باشند یا برای عملکرد کامل دوک ضروری باشند. درک شبکهٔ تعاملی ARK1 برای یافتن «پاکتهای» مناسب جهت اتصال مولکولهای کوچک و طراحی مهارکنندههای اختصاصی حیاتی است.
در سطح ساختاری، مطالعات مدلسازی و تعیین ساختار سهبعدی (مانند بلورنگاری یا کرایو-EM در صورت امکان) میتواند نقاط ضعفِ اختصاصیِ دامنهٔ کاتالیتیک یا محلهای تنظیمی ARK1 را آشکار سازد. این اطلاعات برای مهندسی مولکولهایی با «کمربند ایمنی» بالا — یعنی توانایی تمایز میان کینازهای انگل و همتایان انسانی — ضروری خواهد بود.
چالشها و ملاحظات در توسعه دارو
هرچند ARK1 هدفی امیدوارکننده است، مسیر تبدیل یک کشف بنیادی به داروی مؤثر طولانی و پیچیده است. چندین چالش کلیدی عبارتاند از:
- انتخابپذیری هدف: تضمین اینکه مولکولهای مهارکننده ARK1 با حداقل تداخل بر کینازهای انسانی عمل کنند تا عوارض جانبی کاهش یابد.
- دسترسی درونسلولی: طراحی ترکیباتی که بتوانند به اندامکها و فضای درون سلول میزبان که انگل در آن جای گرفته نفوذ کنند، بهویژه در فازهای کبدی و درونسلولی خون.
- مقاومت دارویی: پیشبینی و کاهش احتمال پدیدآیی جهشهایی که میتوانند حساسیت ARK1 را به مهارکنندهها کاهش دهند؛ راهکارهایی مانند استفاده از ترکیبات ترکیبی (combination therapy) ممکن است لازم باشد.
- مرحلهمحوری اثر: آرک۱ در کدام مراحل چرخه زندگی پلاسمودیوم بیشترین نقش را ایفا میکند؟ برای مثال، مهار در مرحلهٔ گامتوسیت ممکن است انتقال را قطع کند، در حالی که مهار در مرحلهٔ مهرهداران میتواند از بیماری جلوگیری کند؛ انتخاب استراتژی بالینی وابسته به این نکات است.
- پیشرفت از آزمایشگاه به مدلهای حیوانی و سپس مطالعات بالینی: اثبات اثربخشی در جمعیتهای مناسب و سنجش ایمنی در انسان ضروری است.
برای غلبه بر این موانع، مجموعهای از رویکردها مورد نیاز است: زیستشناسی ساختاری برای شناسایی جیبهای قابل هدف، غربالگری بالابرودت (high-throughput screening) برای یافتن اسکلتهای مولکولی اولیه، و مهندسی دارویی برای بهینهسازی خواص فارماکولوژیک و فارماکوکینتیک. علاوه بر این، آزمایشات in vivo در مدلهای حیوانی و ارزیابی سمیت و جذب، توزیع، متابولیسم و دفع (ADME/Tox) از مراحل کلیدی توسعه هستند.
دیدگاه کارشناسانه
«هدف مثل آرک۱ ارزشمند است دقیقاً به این دلیل که در گلوگاه تکثیر انگل قرار دارد»، میگوید دکتر لیلا منساه، پارازیتولوژیست مولکولی که در این مطالعه حضور نداشت. «اگر بتوانیم مولکولهایی طراحی کنیم که وارد سلولهای آلوده شده شده و بهطور انتخابی آن کیناز را مهار کنند، میتوانیم هم پیشرفت بیماری در بیماران را متوقف کنیم و هم انتقال از طریق پشهها را مسدود سازیم. این یک فرصت دو سویه است.»
کارهای آتی مسیر تعاملات ARK1 را نگاشت خواهند کرد، پاکتهای سازگار با مولکولهای کوچک را شناسایی خواهند نمود و کتابخانههای شیمیایی را برای یافتن مهارکنندههایی با تعادل مناسب میان قدرت و اختصاصیبودن غربالگری خواهند کرد. زیستشناسی ساختاری، غربالگری با توان بالا و آزمایش اثربخشی درونبدنی در مدلهای حیوانی همگی گامهایی حیاتی هستند.
افقهای آینده و اهمیت برای سلامتی جهانی
کشف ARK1 به عنوان یک «پاشنه آشیل» در زیستشناسی تقسیم پلاسمودیوم، دیدگاه جدیدی به میدان مبارزه با مالاریا میبخشد. این یافته نه تنها بینش پایهای مهمی دربارهی چگونگی تنظیم تقسیم سلولی نامتعارف در انگل ارائه میدهد، بلکه یک هدف عملپذیر برای توسعه داروهای نسل بعدی معرفی میکند که میتوانند هم بیماریزایی را کاهش دهند و هم زنجیرهٔ انتقال را قطع کنند.
موفقیت در این مسیر میتواند تأثیر بهسزایی بر بار بیماری در مناطق پرخطر داشته باشد؛ بهویژه زمانی که درمان جدیدی با ایمنی و کارایی مناسب ترکیب شود با ابزارهای پیشگیریای مانند کنترل ناقلین، تشخیص سریع و واکسیناسیون. البته اینکه آیا این کشف به دارویی منجر خواهد شد که هزاران زندگی را نجات دهد، هنوز نیازمند پژوهشها و آزمونهای بالینی است، اما مسیر پیشرو واضحتر و ساختارمندتر از گذشته شده است.
در مجموع، ترکیب دانش زیستشناسی سلولی انگل، فناوریهای نوین ژنتیکی و ابزارهای شیمیایی دارویی افق امیدوارکنندهای برای هدفگیری ARK1 فراهم میآورد. این رویکرد میتواند نمونهای از شیوهٔ نوینی باشد که پژوهش بنیادی را مستقیماً به راهحلهای بالینی برای مبارزه با بیماریهای عفونی متصل میکند — و شاید نقطهٔ عطفی در تلاش جهانی برای ریشهکنی مالاریا باشد.
نظرات
پمپزون
معقول بنظر میاد، اگر انتخابپذیری باشه میتونه خیلی موثر باشه اما تنهایی جواب نمیده، ترکیب درمانی لازم خواهد بود
رضا
کمی اغراق شده به نظرم. پنجره درمانی خوبه ولی از آزمایشگاه تا دارو کلی فاصله هست، باید صبور باشیم
بایونیکس
من رو پروتئین پروتئین کار کردم، نقشه تعاملات واقعا کلیده. اگه ARK1 شبکه مشخصی داشته باشه، میشه نقاط هدف رو دقیقتر زد
توربوام
جالبه، تلفیق زیستشناسی ساختاری و داروشناسی دقیقا همینه که لازمه. مسیر طولانیه اما قدم به قدم، باید دید
کوینپایل
واقعاً اینقدر اختصاصی میشه؟ یعنی میشه ARK1 رو بدون زدن کینازهای خودمون هدف گرفت؟ 🤔 شک دارم، اما اگر درست باشه معرکه است
دیتاپالس
وااای، این کشف میتونه واقعاً بازی رو عوض کنه! امیدوارم دارویی پیدا بشه که امن باشه و زود برسونن به بازار...

ارسال نظر