9 دقیقه
تحلیل جدید رابطه زیرگروه خونی A1 را با خطر سکته در جوانان نشان میدهد
یک تحلیل ژنتیکی گسترده که در سال ۲۰۲۲ منتشر شد، نشان داد افرادی که ژنوم آنها نشاندهنده زیرگروه خونی A1 است، با افزایش نسبتاً اندکی در خطر ابتلا به سکته ایسکمیک قبل از سن ۶۰ سالگی مواجهاند. این مطالعه دادههای چندین گروه بینالمللی را تجمیع کرد و حدود ۱۷٬۰۰۰ نفری را که بین ۱۸ تا ۵۹ سال دچار سکته شده بودند با نزدیک به ۶۰۰٬۰۰۰ کنترل بدون سابقه سکته مقایسه نمود و سیگنالی قابل تکرار را نزد ژنهایی که گروههای خونی ABO را تعیین میکنند، شناسایی کرد.
یافتهها نشان میدهد که پیوند میان ژنتیک گروه خونی و ریسک سکته زودهنگام قابل مشاهده است، اما باید به این نکته توجه داشت که افزایش خطر نسبی اندک است و در سطح مطلق برای بیشتر افراد احتمال کلی وقوع سکته همچنان پایین باقی میماند. در ادامه جزئیات طراحی مطالعه، شواهد زیستشناختی ممکن، محدودیتها و پیامدهای بالینی به تفصیل بررسی شدهاند.
طرح مطالعه و نتایج کلیدی
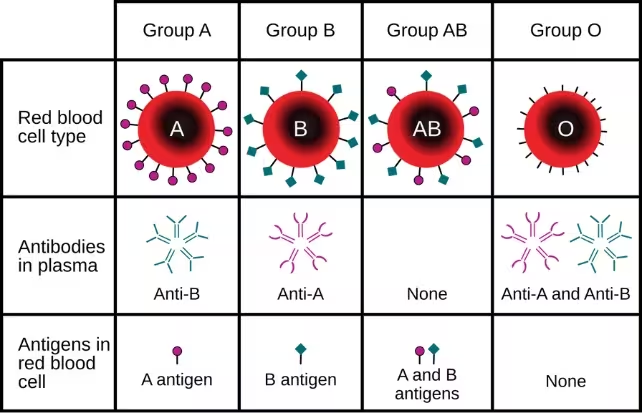
پژوهشگران دادههای ۴۸ مطالعه ژنتیکی را از مناطقی شامل آمریکای شمالی، اروپا، ژاپن، پاکستان و استرالیا ترکیب کردند. همه شرکتکنندگان در تحلیل اصلی در بازه سنی ۱۸ تا ۵۹ سال قرار داشتند تا تمرکز بر سکتههای زودهنگام حفظ شود. جستوجوی سرتاسری ژنومی (GWAS) دو ناحیه ژنومی را که با آغاز زودتر سکته مرتبط بودند برجسته کرد؛ یکی از این نواحی با لوکوس گروه خونی ABO همپوشانی داشت، لوکوسی که نشانگرهای مولکولی روی گلبولهای قرمز را رمزگذاری میکند و انواع A، B، AB و O را تعیین مینماید.
تحلیلهای هدفمند بر واریانتهای ABO نشان داد افرادی که در DNA آنها نشاندهنده زیرگونه A با عنوان A1 است، حدود ۱۶٪ افزایش خطر ابتلا به سکته قبل از ۶۰ سالگی دارند در مقایسه با کسانی که ژنوتیپهای دیگر ABO را دارند. در مقابل، افراد حامل ژنوتیپ O1 تقریباً ۱۲٪ خطر کمتر برای سکته زودهنگام نشان دادند. نویسندگان مطالعه تأکید کردند که این اندیسهای نسبی خطر متواضع هستند و از دیدگاه بالینی برای یک فرد مشخص احتمال مطلق رخداد هنوز پایین است.
تحلیلهای تکمیلی شامل تنظیم برای عوامل اختلالگر بالقوه، آزمونهای همبستگی و آنالیزهای حساسیت بود تا نشان دهد که سیگنالهای مشاهدهشده قابل اعتماد و بازتولیدپذیرند. علاوه بر این، پژوهشگران تلاش کردند اثرات بالقوه ترکیبی با سایر نشانگرهای ژنتیکی و بالینی را بررسی کنند تا بفهمند آیا ترکیب اطلاعات ژنتیکی با دادههای بالینی میتواند پیشبینی ریسک را بهبود دهد یا خیر.
از جنبه روششناختی، استفاده از نمونههای بزرگ و چندملیتی به تقویت اعتبار یافته کمک کرده، هرچند پیگیریهای بیشتر برای بررسی تکرار نتایج در جمعیتهای مستقل و متنوع لازم است. همچنین لازم است توجه شود که انواع مختلف سکته (مثلاً ایسکمی در مقابل خونریزیای) ممکن است الگوهای ژنتیکی متفاوتی داشته باشند و مطالعه حاضر بر سکته ایسکمیک تمرکز داشت.
محققان همچنین ارتباطهای ژنتیکی در سکته با آغاز زودهنگام (<60 سال) را با مجموعهای از موارد سکته در سنین بالاتر (بیشتر از ۶۰ سال) مقایسه کردند. رابطه بین زیرگروه A و سکته در گروه دچار سکته دیررس ضعیفتر شده و از نظر آماری معنیدار نبود، که نشان میدهد محرکهای بیولوژیک اولیه برای سکتههای زودهنگام و دیررس ممکن است متفاوت باشند. این اختلاف سنی بر اهمیت درک مکانیسمهای специфیک سن تأکید میکند و نشان میدهد نتایج برای پیشبینی ریسک باید در چارچوب سن و سایر عوامل بالینی تفسیر شوند.
زمینه زیستشناختی و مکانیسمهای ممکن
لوکوس ABO، انعقاد خون و زیستشناسی عروقی
لوکوس گروه خونی ABO پیشتر با پدیدههایی مانند کلسفیکاسیون عروق کرونری، انفارکتوس میوکارد و ترومبوز وریدی مرتبط دانسته شده است. شواهد آزمایشگاهی و اپیدمیولوژیک نشان میدهد واریانتهای ABO میتوانند سطح عوامل انعقادی گردشگر، تعاملات پلاکتی و عملکرد سلولهای اندوتلیال پوشاننده رگها را تحت تأثیر قرار دهند. این مسیرها مکانیسمهای زیستی معقولی هستند که میتوانند توضیح دهند چرا یک ژنوتیپ از نوع A ممکن است کمی احتمال تشکیل لخته و در نتیجه سکته ایسکمیک را افزایش دهد، بهویژه در بزرگسالان جوانی که تجمع پلاک آترواسکلروتیک بهندرت عامل اصلی است.
به طور خاص، پژوهشهای قبلی ارتباط میان گروه خونی و سطوح فاکتورهایی مانند وون ویلبراند (von Willebrand factor) و فاکتور VIII را نشان دادهاند؛ این عوامل در فرایند انعقاد خون نقش مهمی دارند و تحت تأثیر آنتیژنهای ABO قرار میگیرند. افزایش سطح وون ویلبراند یا فاکتور VIII میتواند میل به تشکیل لخته را بالا ببرد و ممکن است یکی از پلهای بیولوژیک بین ژنوتیپ A1 و سکته ایسکمیک باشد.
با وجود پیوندهای محتمل، دکتر استیون کیترن، نورولوژیست عروقی از دانشگاه مریلند و نویسنده ارشد مطالعه، هشدار میدهد که مکانیزم دقیق هنوز نامشخص است: «ما هنوز نمیدانیم چرا گروه خونی A ریسک بیشتری میدهد،» او گفت. «اما بهنظر میرسد که این مسئله مربوط به فاکتورهای انعقادی مانند پلاکتها، سلولهای پوششی رگها و سایر پروتئینهای موجود در گردش خون باشد که همه در شکلگیری لختهها نقش دارند.»
علاوه بر تاثیر بر فاکتورهای انعقادی، تغییرات در لوکوس ABO ممکن است بر سطوح التهابی سیستمی یا تعاملات بین سلولی در رگها اثر بگذارد. پژوهشهای عملکردی بیشتر، از جمله مطالعات تجربی روی مدلهای حیوانی و آزمایشهای سلولی، نیاز است تا نشان دهد کدام مسیرها و مولکولها نقش علّی دارند و آیا این مسیرها میتوانند اهداف مداخلهای بالقوه برای پیشگیری انتخابی فراهم کنند.
محدودیتها، تنوع جمعیتی و زمینه بهداشت عمومی
با اینکه نمونه تلفیقی بزرگ بود و قدرت آماری مناسبی فراهم کرد، تنها حدود ۳۵٪ شرکتکنندگان از تبار غیراروپایی بودند، بنابراین این یافتهها نیازمند تکرار در جمعیتهای متنوعتر هستند تا عمومیت نتایج مورد تأیید قرار گیرد. تفاوتهای ساختار جمعیتی، فرکانسهای آللی و تعامل ژن-محیط میتوانند اثرات اختصاصیتری را در گروههای اقلیت نشان دهند که در نمونههای فعلی بهخوبی نمایندگی نشدهاند.
شیوع سکته نیز بهطور قوی وابسته به سن است: در ایالات متحده تقریباً ۸۰۰٬۰۰۰ نفر در سال دچار سکته میشوند و حدود سهچهارم این رخدادها در افراد ۶۵ سال به بالا رخ میدهد. خطر سکته پس از سن ۵۵ تقریباً هر دهه دو برابر میشود که این مطلب کمک میکند تا افزایش نسبی ۱۶٪ در افراد جوانتر در چشمانداز واقعبینانهتری قرار گیرد — یعنی برای اکثریت افراد، ریسک مطلق همچنان پایین است.
به سبب اندازه اثر کوچک، نویسندگان مطالعه پیشنهاد نمیکنند که بر اساس تنها گروه خونی ABO، غربالگری اضافی یا مراقبت پزشکی ویژهای برای افراد معرفی شود. در عوض، آنها خواستار تحقیقات تکمیلی برای روشنسازی مکانیسمهای پیوندخورده با انعقاد خون و ارزیابی این موضوع هستند که آیا اطلاعات مربوط به نوع گروه خونی میتواند در کنار سایر نشانگرهای ژنتیکی و بالینی روزی پیشبینی ریسک فردی را بهبود بخشد یا خیر.
از منظر بهداشت عمومی، تمرکز باقی میماند بر شناسایی و مدیریت عوامل خطر اصلاحپذیر مانند فشار خون بالا، دیابت، سیگار کشیدن، چاقی و بیتحرکی. حتی اگر یک عامل ژنتیکی مانند زیرگروه A1 کمی ریسک را افزایش دهد، کاهش عوامل خطر قابلتغییر میتواند تأثیر بزرگتری در پیشگیری از سکته داشته باشد.
دیدگاه کارشناسان
دکتر ماریا سانتوس، اپیدمیولوژیست عروقی در یک مرکز پزشکی دانشگاهی، در مورد پیامدهای مطالعه اینگونه اظهار نظر کرد: «این کار اهمیت وجود تنوع ژنتیکی رایج را نشان میدهد که میتواند بهطور ظریف پروفایل ریسک برای بیماریهای جدی مثل سکته را جابهجا کند. برای پزشکان پیام عملی تغییر نمیکند: تمرکز همچنان روی کنترل فشار خون، دیابت، ترک دخانیات و سایر عوامل قابل تغییر است. برای پژوهشگران، این یافتهها مناطق مربوط به انعقاد و زیستشناسی عروقی را بهعنوان اولویتهایی برای مطالعات عملکردی بیشتر مشخص میکند تا دریابیم آیا استراتژیهای پیشگیرانه هدفمند میتوانند پدید آیند.»
او همچنین افزود که یکی از نکات مثبت مطالعه، جمعآوری دادهها از جمعیتهای مختلف جغرافیایی است که میتواند به درک بهتر اثرات تعامل ژن-محیط کمک کند، اما تکرار در گروههای بومیتر و با ساختار ژنتیکی متفاوت ضروری است. در نهایت، ترکیب شواهد اپیدمیولوژیک، ژنتیکی و آزمایشگاهی بهترین مسیر برای تعیین عواقب بالینی واقعی است.
نتیجهگیری
متا-آنالیز ژنتیکی سال ۲۰۲۲ شواهد را تقویت میکند که واریاسیونهای ارثی در لوکوس گروه خونی ABO، بهویژه زیرگروه A1، با افزایش نسبتاً اندکی در خطر سکته ایسکمیک قبل از ۶۰ سالگی همراه است، در حالی که O1 بهطور متواضعی محافظتی بهنظر میرسد. اندازه اثرها کوچک است و بهتنهایی موجه برای تغییر در روندهای غربالگری بالینی بر اساس گروه خونی نیست.
نیاز است مطالعات آینده نمایندگی ژنتیکی گستردهتری از نظر نژادی و قومی داشته باشند و کارآزماییهای آزمایشگاهی بیشتری برای بررسی مکانیسمهای پیشنهادی انجام شود تا مشخص گردد آیا ژنوتیپ ABO میتواند بهصورت معناداری به استراتژیهای پیشگیری شخصیسازیشده اضافه شود. در همین حال، پیام بالینی روشن است: اولویت با مدیریت عوامل خطر قابل اصلاح است، زیرا بیشترین تأثیر را در کاهش بار بیماری سکته خواهد داشت.
در مجموع، ترکیب شواهد ژنتیکی و دادههای بالینی میتواند چشمانداز بهتری برای درک ریسک سکته در افراد جوان بهوجود آورد، اما ترجمه این شناخت به کاربردهای بالینی نیازمند احتیاط، تکرار نتایج و بررسیهای عملکردی عمیقتر است.
منبع: sciencealert

ارسال نظر