10 دقیقه
یک کارآزمایی بالینی کوچک در ایالات متحده نشان میدهد که دو داروی بازمصرفشده — یک داروی دیابت و یک اسپری انسولین داخلبینی — ممکن است بهطور ایمن نشانگرهای سلامت مغز را در افراد پرخطر برای بیماری آلزایمر بهبود دهند. این مطالعه بر معیارهای متابولیک و نورواوراسکولار مرتبط با زوال شناختی اولیه تمرکز کرد و سیگنالهای امیدوارکنندهای تولید کرد که نیاز به محققههای بزرگتر و طولانیتر دارد.
چرا پژوهشگران روی متابولیسم و جریان خون تمرکز کردند
آلزایمر و دیگر انواع زوال عقل از نظر زیستشناختی پیچیدهاند و درمان آنها به احتمال زیاد نیازمند راهبردهای مکمل و چندجانبه خواهد بود. به جای هدف قرار دادن نشانههای مرحلهٔ نهایی مانند پلاکهای بزرگ آمیلوئید، این مطالعه درمانهایی را آزمایش کرد که بر متابولیسم سلولی، التهاب و گردش خون مغزی تأثیر میگذارند — فرایندهای اولیهای که میتوانند نورونها را مقاومتر کنند.
تمرکز بر متابولیسم و خونرسانی مغزی مبتنی بر شواهد فزایندهای است که نشان میدهد اختلالات سوختوساز سلولی و مقاومت به انسولین مغزی ممکن است پیشدرآمدی برای تجمع پروتئینهای بیماریزا و اختلال در عملکرد سیناپسی باشند. علاوه بر این، اختلال در ریزعروق و کاهش پرفیوژن موضعی میتواند انرژیرسانی به شبکههای عصبی حساس حافظه را کاهش دهد و مسیرهای التهابی را فعال کند.
به طور خلاصه، دستکاری زودهنگام متابولیسم و بهبود جریان خون مغزی میتواند به عنوان یک استراتژی پیشگیرانه یا تعدیلکننده پیشرفت بیماری عمل کند، به ویژه در مراحل پیشروی ظریف که مداخلات ضدآمیلوئیدی سنتی هنوز نتوانستهاند نتایج بالینی قاطع نشان دهند.
داروها چیستند و چگونه عمل میکنند
دو مداخله مورد بررسی عبارت بودند از امپاگلیفلوژین، یک داروی شناختهشده برای دیابت و بیماریهای قلبی-عروقی، و یک اسپری انسولین بینی که برای رساندن مستقیم انسولین به مغز طراحی شده است. امپاگلیفلوژین با تغییر در تنظیم گلوکز و سدیم در کلیهها و بافتها، بار متابولیک سلولی را کاهش میدهد، التهاب سیستمیک را کمتر میکند و میتواند کارایی انرژی سلولی را بهبود بخشد.
انسولین داخلبینی به دنبال غلبه بر مقاومت به انسولین در مغز است — یک پدیده که بهتدریج در تحقیقات ارتباط آن با زوال شناختی نشان داده شده است — و همزمان از سلامت نورونها، کارکرد سیناپسی و تنظیم ایمنی در سیستم عصبی مرکزی حمایت میکند. مسیرهای سیگنالینگ انسولین در مغز با متابولیسم گلوکز، پایداری میتوکندری و تنظیم التهاب در هم تنیدهاند، بنابراین تقویت این مسیرها میتواند اثرات ضدزوال و محافظتی داشته باشد.
هر یک از این داروها از زاویهای متفاوت به مشکل میپردازند: امپاگلیفلوژین به تنظیم وضعیت متابولیک و کاهش استرس اکسیداتیو و التهابی کمک میکند، و انسولین داخلبینی به بهبود سیگنالدهی نورونال و عملکرد سیناپسی میپردازد. ترکیب این دو رویکرد میتواند بر چگونگی تعامل متابولیسم سلولی و عملکرد ریزعروق در بافت عصبی تأثیر بگذارد.
طرح کارآزمایی و شرکتکنندگان
این مطالعه فاز II ایمنی شامل 47 بزرگسال با سنین بین 55 تا 85 سال بود که از این میان 42 نفر پروتکل چهار هفتهای را تکمیل کردند. شرکتکنندگان شامل افرادی با اختلال شناختی خفیف (MCI) یا دمانس خفیف، و همچنین داوطلبان دارای عملکرد شناختی نرمال ولی دارای نشانگرهای مولکولی آلزایمر در تستهای زیستنشانگر بودند. افراد بهصورت تصادفی به یکی از چهار گروه اختصاص یافتند: امپاگلیفلوژین تنها، اسپری انسولین تنها، هر دو درمان با هم، یا پلاسبو.
از آنجا که هدف اصلی، ارزیابی ایمنی و تحملپذیری در دوره کوتاه بود، مطالعه برای اثبات اثرگذاری قطعی طراحی نشده بود. با این حال، محققان مجموعه وسیعی از زیستنشانگرها و نتایج تصویربرداری را جمعآوری کردند — آزمونهای مایع مغزی-نخاعی (CSF)، آزمونهای شناختی، بررسی اتصال ماده سفید در تصویربرداری MRI، اندازهگیری جریان خون مغزی، و نشانگرهای لیپیدی و التهابی — تا روندهای اولیه را شناسایی کنند.
مدل انتخابی نمونهگیری و پروتکل تصویربرداری به گونهای طراحی شد که تغییرات کوتاهمدت در فیزیولوژی مغز قابل ردیابی باشد؛ برای مثال، سنجش پروتئینهای مرتبط با تائو در CSF و ارزیابی پرفیوژن مناطقی که در پردازش حافظه نقش دارند، برای شکار سیگنالهای زودهنگام در نظر گرفته شد. این مجموعه دادهها امکان بررسی همزمان تغییرات بیوشیمیایی، ساختمانی و عملکردی را فراهم کرد.
یافتههای کلیدی: سیگنالها در تائو، شناخت و گردش خون
اگرچه تفاوتها بین گروهها با توجه به حجم نمونه کوچک و پنجرهٔ درمانی کوتاه به سطح معناداری آماری نرسید، چند الگوی قابل توجه پدیدار شد. افرادی که فقط امپاگلیفلوژین مصرف کردند کاهشهایی در سطح تائو در CSF نشان دادند — پروتئینی که میتواند در مغزهای مبتلا به آلزایمر به تودههای سمی تبدیل شود — و همزمان بهبودهایی در جریان خون و برخی نشانگرهای لیپیدی مرتبط با خطر دمانس مشاهده شد.
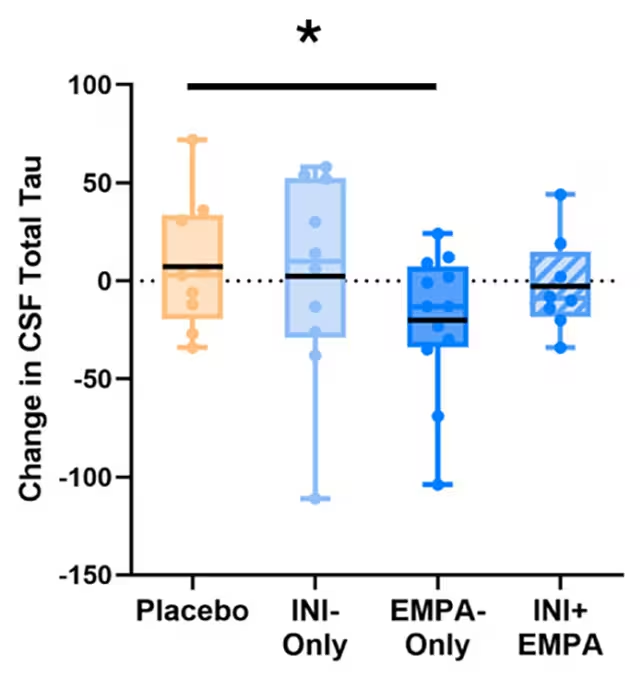
یکی از فواید مشاهدهشده در گروه امپاگلیفلوژین (EMPA-Only) علائم کاهش تجمع تائو در مایع مغزی-نخاعی بود. (Erichsen et al., A&D, 2025)
افرادی که انسولین داخلبینی دریافت کردند در آزمونهای حافظه و عملکرد اجرایی طی دوره کوتاه مطالعه امتیازات بهتری کسب کردند. تصویربرداری مغزی این شرکتکنندگان همچنین نشاندهندهٔ بهبود در اتصال ماده سفید و افزایش پرفیوژن در نواحی مرتبط با پردازش حافظه بود؛ یافتهای که با مطالعات قبلی که ارتباط سیگنالدهی انسولین با سلامت نورواوراسکولار را نشان دادهاند، همخوانی دارد.
علاوه بر این، برخی از شاخصهای التهابی و لیپیدی در گروههای درمانی تغییراتی نشان دادند که از کاهش بار التهابی سیستمیک حکایت داشت. این تغییرات در نشانگرهای التهابی میتواند یکی از مکانیسمهای واسطهای باشد که از طریق آن امپاگلیفلوژین و انسولین داخلبینی اثر محافظتی بر نورونها و میکرومحیط مغزی اعمال میکنند.
چگونگی تعامل احتمالی این داروها
نتایج مطالعه از مدلی پشتیبانی میکند که در آن تعدیل متابولیک و حمایت نوروآندوکرین هدفمند اثرات مکملی دارند. امپاگلیفلوژین به نظر میرسد التهاب سیستمیک و استرس سلولی را کاهش میدهد و بدین ترتیب فرایندهایی را کند میکند که ممکن است تائوپاتولوژی را ترویج دهند. انسولین داخلبینی بهطور مستقیم از متابولیسم نورونها، عملکرد سیناپسی و تنظیم ایمنی در مغز حمایت میکند.
وقتی این دو مداخله با هم اعمال شوند، ممکن است توازن مطلوبی بین تقویت پاسخهای ایمنی محافظتی و جلوگیری از التهاب مضر عصبی ایجاد کنند. برای مثال، کاهش استرس اکسیداتیو و بهبود کارآیی متابولیک میتواند ظرفیت نورونها برای تحمل تجمع پروتئینهای ناسالم و بازیابی سیناپسی را افزایش دهد، در حالی که سیگنالدهی مناسب انسولین ممکن است عملکرد مغزی را در سطح شبکه نگه دارد.
این ترکیب مکانیکی به ویژه در مراحل ابتدایی بیماری ممکن است مؤثر باشد، زمانی که تغییرات مولکولی و عملکردی هنوز قابل برگشت یا تعدیلاند. بنابراین، مدل ترکیبیِ تنظیم متابولیک بهعلاوه تقویت مستقیم سیگنالهای نوروتروفیک میتواند یک مسیر امیدوارکننده برای مداخلات زودهنگام باشد.
ایمنی و محدودیتها
در این مطالعه کوتاه هیچ عارضهٔ مضری گزارش نشد و هر دو درمان در گروههای سنی و زیرگروههای بالینی مختلف تحملپذیری مناسبی نشان دادند. با این حال، نویسندگان محدودیتهای مطالعه را برجسته میکنند: حجم نمونه کوچک، دورهٔ قرارگیری کوتاه (چهار هفته)، و ماهیت اکتشافی چندین نقطه پایان زیستنشانگر. برای تأیید اینکه آیا این سیگنالهای زیستنشانگر و شناختی اولیه به کاهش معنیدار بالینی در پیشرفت بیماری ترجمه میشوند، لازم است کارآزماییهای تصادفیشده بزرگتر و با مدت زمان طولانیتر انجام شود.
همچنین باید در نظر داشت که اثرات بلندمدت و تعاملات دارویی در جمعیتهای متنوعتری — شامل افراد با بیماریهای همزمان متابولیک یا وابستگیهای دارویی مختلف — به دقت بررسی شود. مطالعات بعدی باید امنیتهٔ ایمنی، دوز-پاسخ، و نقطهٔ بهینه شروع درمان را تعیین کنند تا سود بالینی حداکثری همراه با کمترین خطر حاصل شود.
از دید اپیدمیولوژیک، ارزیابی هزینه-فایده و قابلیت اجرای این رویکرد ترکیبی در محیطهای بالینی واقعی (real-world settings) نیز یک گام ضروری خواهد بود، مخصوصاً اگر هدف بازتوزیع داروهای موجود برای درمان یا پیشگیری از زوال عقل باشد.
گامهای بعدی: بزرگمقیاس کردن و درمان ترکیبی
پژوهشگران قصد دارند این درمانها را در گروههای بزرگتر و با پیگیری طولانیتر تست کنند تا اثرات روی شناخت، کاهش عملکرد روزمره و زیستنشانگرهای تأییدشده آلزایمر کمّیسازی شود. چشمانداز بازتخصیص یک داروی تأییدشده دیابت و یک دستگاه هدفمند تحویل انسولین جذاب است، زیرا هر دو پروفایل ایمنی شناختهشدهای دارند و در صورت اثبات اثربخشی در کارآزماییهای بعدی میتوانند سریعتر به بیماران برسند.
علاوه بر کارآزماییهای بزرگ بالینی، مطالعات مکانیکی پایهای بیشتری نیز لازم است تا مسیرهای مولکولی دقیقتر شناسایی شده و بیومارکرهای پیشبینیکنندهٔ پاسخ به درمان مشخص شوند. توسعه زیستنشانگرهای ترکیبی که متابولیسم، وضعیت التهابی و عملکرد ریزعروق را همزمان پایش کنند میتواند به شناسایی زیرمجموعهٔ بیماران با بیشترین احتمال بهرهمندی کمک کند.
در نهایت، برنامههای تحقیقاتی آینده باید به تعاملات دارویی، دوز بهینه، زمانبندی درمان و پیامدهای کیفیت زندگی نیز توجه کنند تا اطمینان حاصل شود که هرگونه سود بیولوژیک به نفع مراقبتهای بالینی معنادار تبدیل میشود.
دیدگاه کارشناسان
دکتر ماریا آلواز، متخصص نورولوژی و محقق بالینی که در این مطالعه دخیل نبوده است، اظهار داشت: «این کارآزمایی نمونهای از پژوهش مکانی-محور و عملیاتی است. هدف قرار دادن متابولیسم و سلامت عروقی در مراحل اولیه از منظر فیزیولوژیک معقول به نظر میرسد. سیگنالها ملایماند اما به اندازهٔ کافی سازگار هستند که توجیهکنندهٔ کارآزماییهای بزرگتر برای آزمون نتایج واقعی بالینی باشند.»
به طور کلی، یافتهها متابولیسم و سلامت نورواوراسکولار را به عنوان جبهههای قابل اقدام در مقابله با آلزایمر برجسته میکنند و راه را برای درمانهای ترکیبی که زودتر در زنجیرهٔ بیماری دخالت میکنند، باز میگذارند. این رویکرد همراستا با دیدگاه گستردهتری است که میگوید درمانهای آیندهٔ آلزایمر احتمالاً چندوجهی و شامل مداخلاتی خواهند بود که همسو با مسیرهای پایهای بیماری عمل میکنند، نه صرفاً تمرکز بر حذف نشانههای دیررس بیماری.
در مجموع، مطالعاتی از این دست اهمیت تعریف دقیق زیرگروههای بالینی، تعیین نشانگرهای پاسخ در دسترس بالینی و طراحی کارآزماییهایی با قدرت آماری کافی برای ارزیابی پیامدهای بالینی معنیدار را نشان میدهند. اگر تحقیقات آتی اثرات اولیه را تکرار و گسترش دهند، این میتواند به توسعهٔ گزینههای درمانی جدید و سریعتر قابل استفاده منجر شود که بر متابولیسم مغز، سیگنالدهی انسولین و جریان خون مغزی تأثیر میگذارند.
منبع: sciencealert
نظرات
توربو
اگه تائو کم شده باشه عالیه، اما آیا واقعا از پیشرفت بیماری جلوگیری میکنه؟ سوال مهم اینه؛ درمان ترکیبی کی و برای کی؟
خودو_ر
رویکرد چندوجهی منطقیه. ولی چهار هفته زیاده کوتاهه برای آلزایمر، بیومارکرها خوبن اما باید ترجمه به زندگی واقعی بشه
بیوانیکس
مقاله خوبیه ولی نمونه کوچک و چهار هفته واقعا کافیه؟ اثرات بلندمدت چی میشه... زیاد خوشبین نیستم هنوز
پمپزون
منطقیشه، به شرطی که نتایج بالینی واقعی باشن. منتظر بررسی بزرگترم
امیر
من پدربزرگم MCI داشت؛ ایدهی بهبود جریان خون و متابولیسم منطقیه، اما اگه اثرات فقط روی بیومارکر بمونه چه فایده؟ باید عملکرد روزمره هم بهتر شه
کوینپایل
اگر واقعا موثر باشه، بازتخصیص سریعش میتونه بازار درمان رو تکون بده، اما مراقب تعاملات دارویی باشید، هزینه و دسترسی مهمه
دیتاپالس
باورم نمیشه؛ داروهای دیابت و اسپری بینی میتونن رو مغز اثر بذارن؟! امیدوارم کارآزمایی بزرگتر هم این رو تایید کنه...

ارسال نظر