6 دقیقه
پژوهشگران یک کلاس تخصصی از سلولهای ایمنی CD4 را شناسایی کردهاند که سلولهای سنسنت — یا به عبارتی «سلولهای زامبی» که با افزایش سن تجمع مییابند و التهاب مزمن را تشدید میکنند — را شناسایی و از میان برمیدارند. این کشف، با رهبری دانشگاه بن‑گوریون نوام نگب، نشان میدهد سیستم ایمنی در طول پیری سازگاریهایی ایجاد میکند و کُشندههای هدفگیریشدهای تولید میکند که به محدود نگه داشتن آسیب بافتی کمک مینمایند. یافتهها اهمیت بالینی و پژوهشی برای مطالعات پیری، ایمنیشناسی و رویکردهای درمانی هدفگیرنده سلولهای پیری (senolytic) دارد و چشمانداز جدیدی درباره تعامل بین پیری سلولی، التهاب مزمن و تخصص ایمنی ارائه میدهد.
How the immune system adapts to aging
سلولهایی که وارد وضعیت سنسنسنس میشوند، تقسیم سلولی را متوقف میکنند اما همزمان مولکولهای التهابی، سایتوکینها، پروتئازها و دیگر عوامل اثرگذار را آزاد میکنند که محیط اطرافشان را تغییر میدهد. این مجموعه رفتارها معمولاً تحت عنوان فنوتیپ ترشحی مرتبط با پیری سلولی (senescence-associated secretory phenotype یا SASP) شناخته میشود. در طول سالها، تجمع این سلولها میتواند به ایجاد اسکار در بافت، نقص عملکردی در اندامها و التهابی مزمن و قابلتوجه که در ادبیات با واژه inflammaging توصیف میشود، منجر گردد. نقش دستگاه ایمنی در پاکسازی این سلولهای زیانبار از مدتها پیش مورد توجه بوده است، اما بازیگران دقیق و مکانیزمهای مولکولی درگیر تا کنون بهطور کامل مشخص نشده بود.
مطالعه تازه، نوعی از سلولهای T کمکی (helper T) با برچسب CD4 را معرفی میکند که پروتئین تنظیمکننده Eomes (Eomesodermin یا به اختصار Eomes) را ابراز میکنند و تحت عنوان CD4‑Eomes نامیده شدهاند؛ این زیرگروه به نظر میرسد خط مقدم دفاع علیه سلولهای سنسنت باشد. تیم پژوهشی با مقایسه سلولهای ایمنی از موشهای جوان و مسن، دو الگوی کلیدی را مشاهده کرد: نخست، حضور سلولهای سنسنت موجب میشود سلولهای CD4 به سمت فنوتیپ CD4‑Eomes تغییر وضعیت دهند؛ و دوم، موشهای تغییر ژنتیکیشدهای که قادر به ایجاد این تخصص نبودند، تجمع بیشتری از سلولهای سنسنت را نشان دادند. به عبارت دیگر، CD4‑Eomes احتمالاً یک پاسخ تطبیقی سیستم ایمنی به بارِ فزاینده سلولهای پیری است که با سن افزایش مییابد و به حفظ هومئوستازی بافت کمک میکند.
Evidence from experiments and disease models
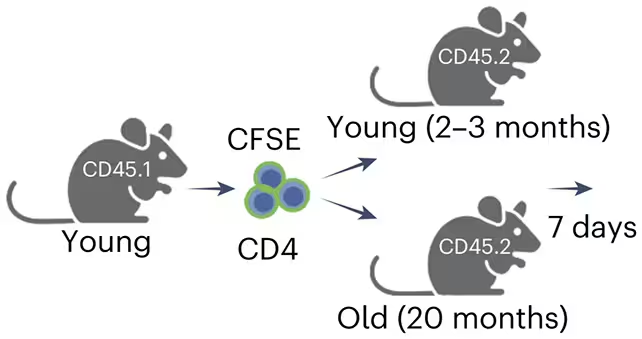
برای ارزیابی عملکرد این سلولها، پژوهشگران سلولهای CD4 را از حیوانات جوان جمعآوری و به گیرندههای جوان و مسن پیوند زدند و سپس پیامدها را پیگیری کردند. در شرایطی که تخصص CD4‑Eomes در دسترس بود، تعداد سلولهای سنسنت کاهش یافت و شاخصهای آسیب بافتی و نشانگرهای التهابی بهبود نشان دادند. اثر محافظتی این زیرگروه ایمنی نه تنها در شرایط فیزیولوژیک بلکه در مدلهای بیماری نیز مشاهده شد: در مدل موشی سیروز کبدی (liver cirrhosis) وجود CD4‑Eomes باعث محدود شدن تشکیل اسکار (فیبروز) و کاهش میزان سلولهای سنسنت در بافت آسیبدیده کبد گردید. این نتایج نشان میدهد این سلولها میتوانند بارِ سلولهای پیری را در بافتهای آسیبدیده کاهش دهند و در نتیجه عملکرد اندام را حفظ یا بخشاً بازسازی کنند.
آزمایشهای عملکردی ذکرشده شواهد مستقیمی فراهم میکنند که CD4‑Eomes نقش کنترلی و حفاظتی در برابر تجمع سلولهای سنسنت دارد. زمانی که این تخصص ایمنی بهصورت ژنتیکی حذف شد، سلولهای سنسنت تکثیر بیشتری یافتند که این امر فرضیهٔ ضروری بودن این زیرمجموعه ایمنی برای نگهداری بافتها در زمان پیری را تقویت میکند. علاوه بر این، محققان به نشانگرهای مولکولی شناختهشدهٔ پیری سلولی مانند افزایش بیان p16INK4a، p21 و فعالیت SA‑β‑gal اشاره کردند که در حضور یا غیاب CD4‑Eomes تغییر میکنند؛ چنین دادههایی به درک مکانیزمی کمک میکنند که چگونه ایمنی تطبیقی میتواند بر پاکسازی سلولهای پیری تأثیر گذارد.
Why this matters for anti-aging research
بسیاری از راهکارهای احیاء و ضدپیری (rejuvenation) بر این فرض تکیه دارند که بازتنظیم سیستم ایمنی پیر به یک وضعیت شبیه جوانی، کلید برگرداندن افت عملکردی وابسته به سن است. کار تیم دانشگاه بن‑گوریون به ما هشدار میدهد که چنین دیدگاهِ یکقالببرایهمه ممکن است سادهسازیکننده باشد. پروفایل ایمنی که شامل سلولهای CD4‑Eomes باشد ممکن است در بزرگسالان مسن مفید باشد؛ بنابراین پاکسازی یا حذف کامل ویژگیهای ایمنیِ «پیریشده» میتواند دفاعهای تطبیقی مفید را از بین ببرد و بهطور ناخواسته ریسک عوارض را افزایش دهد.
محققان اصلی پیشنهاد میکنند هدف نهایی نباید ایجاد سیستم ایمنی بهطور مصنوعی فوقالفعّال باشد، بلکه باید دستیابی به یک تنظیمبندی متناسب با مرحلهٔ زندگی فرد باشد—سیستمی که بتواند بهطور مؤثر سلولهای سنسنت را پاکسازی کند بدون اینکه التهاب خودایمنیمانند مخرب یا پاسخهای آزاردهندهٔ خارجهدف (off‑target immune effects) را برانگیزد. این نکته برای طراحی درمانهای ایمنِ تقویتکنندهٔ پاکسازی سلولهای پیری، از جمله ترکیبدرمانی با سنولیتیکها و تقویت انتخابی سلولهای تخصصی، اهمیت زیادی دارد.
Next steps and translational prospects
سؤالات کلیدی همچنان باقی است: آیا سیستم ایمنی انسان به همان شیوه سلولهای CD4‑Eomes تولید میکند و اگر چنین است، چگونه عوامل ژنتیکی، محیطی و تاریخچهٔ بیماری بر عملکرد این سلولها تأثیر میگذارند؟ تیم پژوهشی برنامه دارد پاسخهای CD4‑Eomes را در بافتهای انسانی نقشهبرداری کند، فراوانی و فنوتیپ این سلولها را در نمونههای بالینی بررسی نماید و ارزیابی کند آیا تقویت ایمن و هدفمند این سلولها میتواند پاکسازی سلولهای سنسنت را در انسانها افزایش دهد یا خیر.
اگر بتوان درمانهایی توسعه داد که عملکرد CD4‑Eomes را تقویت کنند، این رویکردها میتوانند مکمل راهکارهای موجود مانند داروهای سنولیتیک (senolytic drugs) باشند که بهطور انتخابی سلولهای پیری را میکشند یا داروهای سنومودولیتیک که ترشح SASP را کاهش میدهند. با این حال، محققان به احتیاط تأکید میکنند—انتقال یافتهها از موش به انسان نیازمند اعتبارسنجی دقیق، مطالعات ایمنی جامع و بررسی اثرات خارجهدف است تا از بروز پاسخهای ایمنی آسیبرسان جلوگیری شود.
در حال حاضر، این کشف پیری را بهعنوان یک تعامل دینامیک بین تجمع آسیب سلولی و سازگاری ایمنی نشان میدهد و مسیر جدیدی از پژوهش را باز میکند که سنسنسنس سلولی، التهاب مزمن وابسته به سن (inflammaging) و تخصص ایمنی را به هم پیوند میزند. این دیدگاه چندبعدی میتواند در توسعهٔ بیومارکرها، اهداف درمانی جدید و رویکردهای شخصیسازیشده برای کاهش بارِ سلولهای پیری نقش اساسی ایفا کند؛ از جمله استفاده از نشانگرهای مولکولی جهت تعیین نیاز به مداخله، ترکیب درمانهای سلولی و دارویی، و تعریف پروفایل ایمنی بهمنظور حداقل کردن ریسکهای جانبی و افزایش اثربخشی در جمعیتهای متفاوت سنی و بالینی.
منبع: sciencealert
نظرات
پمپزون
خُب، جذابه ولی کمی اغراق شده به نظر میاد. ترجمه از موش به انسان سخت و پر ریسک. منتظر دادههای بالینی هستم
آرمین
نکتهی مهم اینه که پاکسازی کامل ایمنی پیر ممکنه ضرر داشته باشه. باید متعادل باشه، نه فشار دادن همه چی به سمت جوانی
بیونیکس
این نشون میده سیستم ایمنی خیلی سازگاره، ولی سوال اصلی: آیا انسان هم همین سلولها رو داره؟ موش که موش... شواهد کافیه؟
دیتاپالس
وای، ایدهاش جذابه! سلولهای CD4‑Eomes انگار یه دفاع هوشمند میسازن، اگه تو انسان هم باشه… آیندهی ضدپیری میتونه جذاب باشه :)

ارسال نظر