11 دقیقه
دانشمندان از یک داروی نامزد جدید به نام NU-9 گزارش دادهاند که به نظر میرسد با هدف قرار دادن قطعات پروتئینی سمی موسوم به آمیلوئید بتا الیگومرها، تغییرات اولیه مرتبط با بیماری آلزایمر در مغز را کند میکند. این یافته که در مدلهای موشی آزمایش شده است، یک راهکار پیشگیرانه احتمالی را نمایان میسازد که میتواند به افراد در معرض خطر بالا پیش از آنکه اختلال حافظه آشکار شود، ارائه شود. یافتهها میتوانند چشماندازهای جدیدی در پیشگیری از آلزایمر و درمان زودهنگام مبتنی بر بیومارکرها، از جمله آزمایشهای خونی و تصویرسازی پیشرفته، ایجاد کنند.
هشدارگیری روی اولین جرقههای آلزایمر
از سالها پیش محققان این فرضیه را مطرح کردهاند که بیماری آلزایمر دههها پیش از ظهور علائم بالینی آغاز میشود. مجموعههای کوچک و محلول آمیلوئید بتا که به آنها الیگومر گفته میشود، بهعنوان یکی از نخستین عوامل سمی شناخته شدهاند که نورونها را مختل کرده و التهابات موضعی را در سلولهای گلیال مجاور، از جمله آستروسیتها و میکروگلیا، القا میکنند. مطالعه NU-9، که توسط تیمی در دانشگاه نورثوسترن هدایت شد، دقیقاً روی آن تغییرات مولکولی و سلولی اولیه تمرکز داشت که ممکن است بیماری را به حرکت درآورند؛ رویکردی که هدفش پیشگیری از پاتوفیزیولوژی قبل از افت عملکرد شناختی است.
در آزمایشهای پیشبالینی، موشهایی که بهصورت ژنتیکی مستعد ایجاد آسیبشناسی مشابه آلزایمر بودند، تحت درمان با NU-9 قرار گرفتند. این دارو موجب کاهش سطح الیگومرهای آمیلوئید بتا در مغز شد و بهطور مهمی آستروسیتها را در حالت حمایتکننده و کمتحرکتر نگه داشت. آستروسیتها بهصورت طبیعی در حفظ سلامت نورونها، تنظیم سیناپسها و پاکسازی متابولیتها نقش دارند، اما زمانی که واکنشپذیر میشوند—فرآیندی که آستروگلیوزیس نامیده میشود—میتوانند التهاب عصبی را تشدید کرده و سرعت آسیب را افزایش دهند؛ پدیدهای که در مراحل اولیه بیماری مغزی تحلیلرونده اهمیت دارد.
کشف نوع جدیدی از الیگومر و پیامدهای آن
یکی از نتایج غیرمنتظره این مطالعه شناسایی یک زیرنوع الیگومری بود که قبلاً شناسایی نشده بود و با برچسب ACU193+ توصیف شد. تیم پژوهشی دریافت که ACU193+ در مرحلهای بسیار اولیه داخل نورونهای تحتفشار شکل میگیرد و به آستروسیتها متصل میشود—بدون آنکه لزوماً به شکل پلاکهای آمیلوییدی بزرگ تجمع پیدا کند. این تعامل در داخل سلولی ممکن است بهعنوان ماشهای عمل کند که آستروسیتها را از حالت حمایتی به حالت واکنشپذیر و مضر سوق میدهد و در نتیجه مسیر التهاب عصبی و اختلال سیناپسی را تسریع میکند.
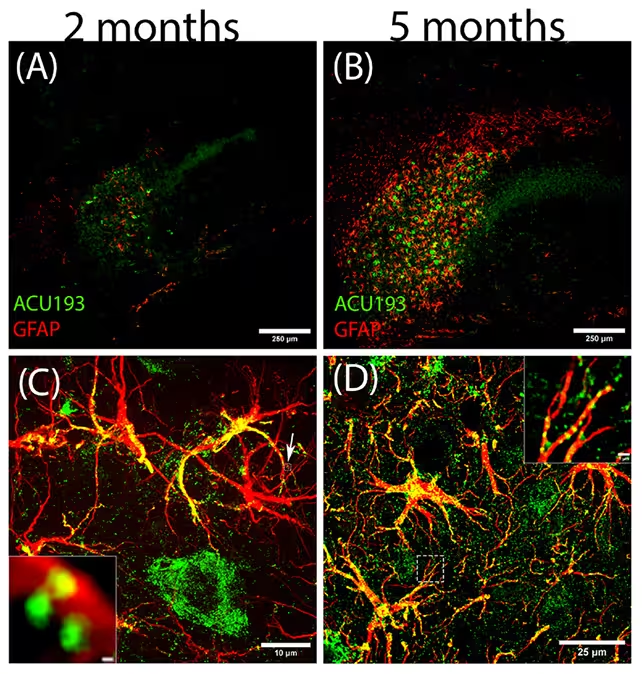
محققان نفوذ رو به رشد الیگومرهای آمیلوئید بتا (سبز) و تأثیر آنها بر آستروسیتهای واکنشپذیر (قرمز) را ردیابی کردند.
«این نتایج شگفتآور است»—ویلیام کلاین، نوروبیولوژیست، با اشاره به کاهش قابلتوجه آستروگلیوزیس واکنشپذیر پس از درمان با NU-9، که یک نشانگر کلیدی التهاب عصبی مرتبط با پاتولوژی اولیه آلزایمر است، گفت. دانیل کرانز، نوروساینتیست نورثوسترن نیز افزود که رویدادهای مولکولی اولیه—مانند انباشت داخلسلولی آمیلوئید و فعالسازی گلیا—سالها پیش از بروز نشانههای بالینی رخ میدهند؛ ناهماهنگیای که میتواند توضیح دهد چرا بسیاری از کارآزماییهای بالینی زمانی که خیلی دیر آغاز میشوند، شکست میخورند. این نکته نشان میدهد که مداخله در مرحله مولکولی اولیه، بهویژه بر روی الیگومرها، میتواند کلید موفقیت درمانهای پیشگیرانه باشد.
مکانیسم عمل NU-9 و اهمیت زمانبندی درمان
به نظر میرسد NU-9 با مداخله در فرایند تجمع الیگومرهای آمیلوئید بتا عمل میکند و از گردهمآیی و تشکیل ساختارهای سمی جلوگیری میکند که قادر به تعامل مخرب با نورونها و آستروسیتها هستند. در مطالعات سلولی قبلی، این ترکیب نشان داده بود که تشکیل الیگومر را در سلولهای مغزی انسانی کشتشده کاهش میدهد؛ اکنون اثربخشی آن در موجودات زنده، از جمله مدلهای موشی، شواهد پیشبالینی قویتری برای پیشرفت به سوی توسعه دارویی فراهم میکند. دانستن این که NU-9 چگونه با اجزای مولکولی آمیلوئید بتا تعامل میکند، برای طراحی دوز، تعیین پنجره درمانی و انتخاب جمعیت هدف در کارآزمایی انسانی حیاتی است.
از مدلهای حیوانی تا پیشگیری احتمالی در انسان
- آزمایشهای مرحله اولیه: در مدلهای موشی، NU-9 بار الیگومری را کاهش داد و نشانگرهای واکنشپذیری آستروسیت را پایین آورد، که نشان میدهد دارو میتواند از تبدیل سلولهای حمایتی به سلولهای التهابی جلوگیری کند.
- گامهای بعدی در حیوانات: محققان اکنون NU-9 را در مدلهایی که پاتولوژی پیشرفتهتر را بازسازی میکنند، آزمایش میکنند تا بررسی کنند آیا این ترکیب همچنان در مراحل پیشرفته بیماری نیز فایدهای دارد یا خیر؛ این مطالعات شامل پر کردن شکافهای زمانی طولانیتر و بررسی کارکردهای شناختی در کنار نشانگرهای مولکولی است.
- مسیر بالقوه انسانی: اگر دادههای حیوانی همچنان امیدوارکننده باقی بمانند، NU-9 میتواند وارد کارآزماییهای بالینی شود که جمعیت هدف آنها افراد دارای بیومارکرهای اولیه آلزایمر هستند—رویکردی شبیه استفاده از استاتینها برای پیشگیری از بیماری قلبی در افراد پرخطر؛ یعنی درمان پیشگیرانه براساس شناسایی زودهنگام ریسک بیولوژیک به جای انتظار برای بروز علائم بالینی.
مهم است تأکید شود که آمیلوئید بتا—چه به شکل الیگومرها و چه به شکل پلاکها—ممکن است تنها علت آلزایمر نباشد. بیماری احتمالاً از عوامل متعددی که با یکدیگر تعامل دارند ناشی میشود، از جمله پاتولوژی تاو، تغییرات عروقی، ژنتیک و عوامل سبک زندگی. با این حال، هدفگیری یک بازیگر سمی زودهنگام مانند الیگومرها میتواند بخشی از یک استراتژی چندوجهی پیشگیرانه باشد که شامل درمانهای ضدتاو، تنظیم فاکتورهای قلبیعروقی و مداخلات سبک زندگی نیز میشود.
پیامدها برای تشخیص و پزشکی پیشگیرانه
افق دارویی که بتوان آن را پیش از بروز علائم مصرف کرد، بهشدت وابسته به بهبود تشخیص زودهنگام است. بیومارکرهای خونی جدید، روشهای تصویربرداری حساستر و ابزارهای تشخیصی مولکولی در حال توسعهاند و میتوانند کاندیداها را برای درمان پیشگیرانه شناسایی کنند. اگر آزمایشهای خونی و بیومارکرهای اولیه به گونهای عمل کنند که بهطور قابلاطمینانی افراد در معرض خطر را نشان دهند، میتوان NU-9 را در گروههایی با نشانههای زیستی اولیه آلزایمر بهکار گرفت. کلاین این نکته را چنین بیان کرد: «اگر فردی بیومارکری نشاندهنده بیماری آلزایمر داشته باشد، میتواند پیش از ظهور علائم، مصرف NU-9 را آغاز کند»، و این مقایسه مستقیم با داروهای کاهشدهنده کلسترول است که برای کاهش ریسک قلبی-عروقی در افراد پرخطر تجویز میشوند.
سؤالات کلیدی که پژوهشگران دنبال پاسخدادن به آنها هستند
سؤالهای کلیدی هنوز پابرجا هستند: آیا NU-9 میتواند در مدلهای مرحلهپیشرفته پیشروی بیماری را کند یا متوقف کند؟ آیا درمان طولانیمدت ایمن و مؤثر خواهد بود؟ و یافتههای حیوانی تا چه اندازه به پیچیدگی مغز انسان قابل تعمیم هستند؟ کارهای پیشبالینی جاری تلاش میکنند به این پرسشها پاسخ دهند، در حالی که پژوهشگران مطالعات ایمنی و تعیین دوزهای لازم را برای آمادهسازی یک آزمایش انسانی برنامهریزی میکنند. علاوه بر این، مسائل فراتر از اثربخشی صرف مطرحاند: هزینه تولید و توزیع، پذیرش اجتماعی درمان پیشگیرانه، سیاستگذاری سلامت عمومی برای شناسایی و درمان افراد پرخطر، و معیارهای اخذ مجوز توسط نهادهای تنظیمی که برای داروهای پیشگیرانه ممکن است متفاوت باشد.
نکات تخصصی و دیدگاه کارشناسانه
«NU-9 نمایانگر یک جهتگیری امیدوارکننده است زیرا در مرحله مولکولی مداخله میکند که معمولاً پیش از بروز علائم رخ میدهد»—دکتر النا موریس، پژوهشگر ارشد خیالی در زمینه بیماریهای عصبی تحلیلرونده، گفت. او اضافه کرد که پزشکی پیشگیرانه عصبی نیازمند ترکیبی از تشخیص زودهنگام، درمانهایی با تحملپذیری خوب و آمادگی نظامهای بهداشتی برای درمان افرادی است که در معرض خطرند اما هنوز بیمار نشدهاند. NU-9 میتواند یکی از اجزای این معما باشد—در صورتی که مطالعات بزرگتر مزایای آن را تأیید کنند. از منظر فنی، ترکیب اختصاصی NU-9 و هدف مولکولی آن باید با دادههای فارماکولوژیک، سمیتشناسی و فارماکوکینتیک همراه شود تا پنجره درمانی و نسبت سود به ریسک مشخص گردد.
برای افزایش اعتبار علمی این رویکرد باید توجه داشت که ترکیب آنتیبادیمحور یا مولکولهای کوچک که الیگومرهای سمی را هدف قرار میدهند، باید مشخصاً تمایز میان فرمهای فیزیولوژیک آمیلوئید بتا و فرمهای پاتولوژیک را رعایت کنند تا از اختلال در عملکرد طبیعی سیناپسی جلوگیری شود. علاوه بر آن، تعامل میان آمیلوئید بتا و مسیرهای تاو، اختلالهای عروقی و سیستم ایمنی مرکزی باید بهطور یکپارچه مورد بررسی قرار گیرد، زیرا درمان تکمحوری احتمالاً برای بسیاری از بیماران کافی نخواهد بود.
در نهایت، ترکیب NU-9 با استراتژیهای تشخیصی مانند پنلهای بیومارکری خونی، PET اسکن آمیلوئید و اندازهگیری نشانگرهای التهابی یا تاو میتواند به تعیین بهترین زمان مداخله و پایش پاسخ درمانی کمک کند. رویکردی مبتنی بر دادههای زیستی طولی (longitudinal biomarker data) میتواند مشخص کند که کدام بیماران بیشترین احتمال بهرهمندی را دارند و چه زمانی باید درمان را آغاز کرد.
جمعبندی موقت و نکات عملیاتی
کشف NU-9 و شواهدی که از مدلهای حیوانی بهدست آمده، نویدبخش امکان توسعه داروهایی برای پیشگیری از آلزایمر از طریق هدفگیری الیگومرهای آمیلوئید بتا است. با این حال، مسیر از مطالعات پیشبالینی تا تایید بالینی و تجویز عمومی طولانی و پیچیده است. موفقیت آینده بستگی به مجموعهای از عوامل دارد: اثبات اثر بالینی در انسان، ایمنی در طولانیمدت، توانایی شناسایی زودهنگام افراد در معرض خطر از طریق بیومارکرها، و ظرفیت سیستمهای بهداشتی برای پیادهسازی درمان پیشگیرانه. اگر همه این قطعات با هم قرار بگیرند، NU-9 میتواند نقش مهمی در استراتژیهای پیشگیری از آلزایمر ایفا کند، اما تا آن زمان امیدوار بودن همراه با پایبندی به شواهد علمی و مطالعات کنترلشده ضروری است.
نکات پایانی برای پژوهشگران و متخصصان بالینی
پژوهشگران باید بر شفافسازی مکانیسم مولکولی ACU193+ و نحوه تعامل آن با آستروسیتها تمرکز کنند، و همچنین مطالعات طولی را برای بررسی اثرات درمانی طولانیمدت NU-9 انجام دهند. متخصصان بالینی میتوانند برنامهریزی برای کارآزماییهای بالینی فاز اولیه را آغاز کنند که افراد با بیومارکرهای مثبت را هدف بگیرد، در حالی که سیاستگذاران به ایجاد چارچوبهای اخلاقی و مقرراتی برای درمان پیشگیرانه فکر کنند. ترکیب این تلاشها با توسعه معیارهای تشخیصی دقیق و در دسترس، میتواند مسیر را برای یک رویکرد جامع پیشگیری از آلزایمر هموار سازد؛ رویکردی که در آن داروهایی مانند NU-9 بخشی از رژیم پیشگیرانهای باشند که با تغییر سبک زندگی، کنترل فاکتورهای قلبیعروقی و درمانهای هدفمند دیگر ترکیب میشود.
منابع و ارجاعات قابلاستناد
برای آگاهی بیشتر و ارجاع به روشهای آزمایشی و نتایج پیشبالینی میتوان به مقالات منتشرشده در مجلات تخصصی نوروساینس و داروشناسی، گزارشهای کنفرانسهای بینالمللی و پایگاههای داده پیشبالینی رجوع کرد. در مسیر مهاجرت از مدلهای حیوانی به انسان، دادههای فارماکولوژی، سمیتشناسی و مطالعات اثربخشی کوتاهمدت و بلندمدت اهمیت ویژهای خواهند یافت؛ منابعی که باید بهعنوان شواهد پشتیبان برای ارزیابی کامل NU-9 مورد استفاده قرار گیرند.
در یک نگاه
NU-9 یک نامزد دارویی امیدوارکننده است که با هدف قرار دادن الیگومرهای آمیلوئید بتا و جلوگیری از واکنشپذیری آستروسیتها، میتواند راهی نوین برای پیشگیری از آلزایمر در مراحل بسیار اولیه ارائه کند. با این همه، راه طولانی تا تأیید بالینی و کاربرد گسترده در انسان باقی است؛ مسیری که نیازمند مطالعات دقیق، زیرساختهای تشخیصی قوی و سیاستگذاری حسابشده است.
نظر متخصص
«NU-9 نمایانگر یک جهتگیری امیدبخش است چون در مرحله مولکولی مداخله میکند که معمولاً پیش از علائم بالینی رخ میدهد»، دکتر النا موریس افزود. «پزشکی پیشگیرانه عصبی نیازمند ترکیب تشخیص زودهنگام، درمانهای قابلتحمل و آمادگی نظام سلامت برای مراقبت از افراد در معرض خطر است. NU-9 میتواند بخشی از این راهکار باشد—مشروط بر آنکه مطالعات بزرگتر مزایای آن را تأیید کنند.»
منبع: sciencealert
نظرات
آرت_م
هیجانزدهام ولی مردد، اگر بشه الیگومرهای زودرسو تو خون دید، پیشگیری معنی پیدا میکنه… اما هنوز خیلی راه طولانیه
داوینکس
معقولِ، به شرطی که عوارض طولانیمدت معلوم بشه. اگه امن باشه و پنجره درمانی درست باشه، میتونه تغییر بزرگی باشه
کوینپیل
به نظرم کمی هایپ شده، دارو رو زود قضاوت نکنیم اما ایده پیشگیری بر اساس بیومارکر واقعا جذابه، منتظر دادههای انسانیام
بادچرخ
گزارش منطقیه ولی نیاز به ترکیب با بیومارکر و تصویربرداریه، بدون تشخیص زودهنگام عملاً کاربرد محدود میشه
مهدی
تو خانوادهمون سابقه آلزایمر داریم، میخوام بدونم کی میشه دسترسی پیدا کرد... اگه واقعاً جواب بده، بدون سوال زیرش میرم!
بیونیکس
کمی شک دارم، مدل موشی خیلی وقتا فریبنده ست. راهی هست بفهمیم همین مکانیزم تو مغز انسان هم برقرارِ؟ هنوز سوالای زیادی مونده
رودایکس
وای، اگر واقعاً NU-9 بتونه آستروسیتو اینجوری محافظت کنه... یعنی یه انقلاب تو پیشگیری آلزایمر؟ امیدوارم آزمایشای انسانی هم جواب بدن

ارسال نظر