8 دقیقه
تحقیق جدید دانشگاه مکگیل یک ایده مرکزی دربارهٔ دوپامین و حرکت را به چالش میکشد. بهجای اینکه دوپامین نقش کنترلگر لحظهبهلحظه برای تعیین سرعت یا نیروی هر حرکت را داشته باشد، ممکن است این انتقالدهنده وظیفهٔ فراهم کردن شرایط زمینهای و پایدار را بر عهده داشته باشد تا اساساً امکان حرکت فراهم شود — یافتهای که پیامدهای مستقیمی برای درمان بیماری پارکینسون دارد.
تغییری در نگاه به توان حرکتی
برای دههها، نوروساینتیستها دوپامین را به «توان حرکتی» (motor vigor) مرتبط دانستهاند — یعنی سرعت و نیروی اعمال ارادی. در بیماری پارکینسون، از دست رفتن پیشروندهٔ نورونهای تولیدکنندهٔ دوپامین با کندی حرکت، لرزش و مشکلات تعادل همراه است. در عمل بالینی، این ارتباط باعث شده درمانها بر بازگرداندن سیگنالدهی دوپامین متمرکز شوند؛ بهویژه لوودوپا که همچنان مؤثرترین درمان علامتی شناخته میشود.
با این حال، مطالعهٔ جدید که در Nature Neuroscience منتشر شده و توسط نیکولاس تریتش در مرکز تحقیقاتی داگلاس مکگیل هدایت شده است، نقش متفاوتی را پیشنهاد میکند. بهجای اینکه دوپامین بهعنوان یک «گاز» یا «تراتل» در زمان اجرا عمل کند و سرعت هر حرکت را تعیین نماید، ممکن است مثل روغن موتور باشد: برای کارکرد کلی سیستم ضروری است اما سیگنال لحظهای تعیینکنندهٔ شدت هر عمل نیست. تریتش میگوید: «یافتههای ما نشان میدهد که باید نقش دوپامین در حرکت را بازاندیشی کنیم. بازگرداندن سطح دوپامین به محدودهٔ طبیعی ممکن است برای بهبود حرکت کافی باشد؛ و این میتواند راهحل درمانی برای پارکینسون را سادهتر کند.»
این بازنگری دیدگاهِ مرسوم دربارهٔ دوپامین و رفتار حرکتی را تحت تأثیر قرار میدهد و پرسشهایی را دربارهٔ معیارهای سنجش عملکرد دوپامین در پژوهشها و بالین مطرح میکند. در عین حال، این دیدگاه جدید بر تمایز میان دو وضعیتی که در مطالعات سیستمهای عصبی از آنها یاد میشود — فازیک (phasic) و تونیک (tonic) — تأکید بیشتری میگذارد: سیگنالهای سریع و گذرا در مقابل سطح پایهٔ پایدار انتقالدهنده.
چگونه آزمایش نقش دوپامین را مورد آزمون قرار داد
تیم تحقیقاتی دینامیک دوپامین را در زمان واقعی ثبت کردند در حالیکه موشها یک کار حرکتی ساده انجام میدادند: فشار دادن یک اهرم با وزن مشخص. آنها ضبطهای بسیار حساس از آزادسازی دوپامین را با اپتوژنتیک ترکیب کردند؛ روشی مبتنی بر نور که میتواند سلولهای تولیدکنندهٔ دوپامین را در لحظات معین روشن یا خاموش کند تا اثرات کوتاهمدت دقیق بررسی شود.
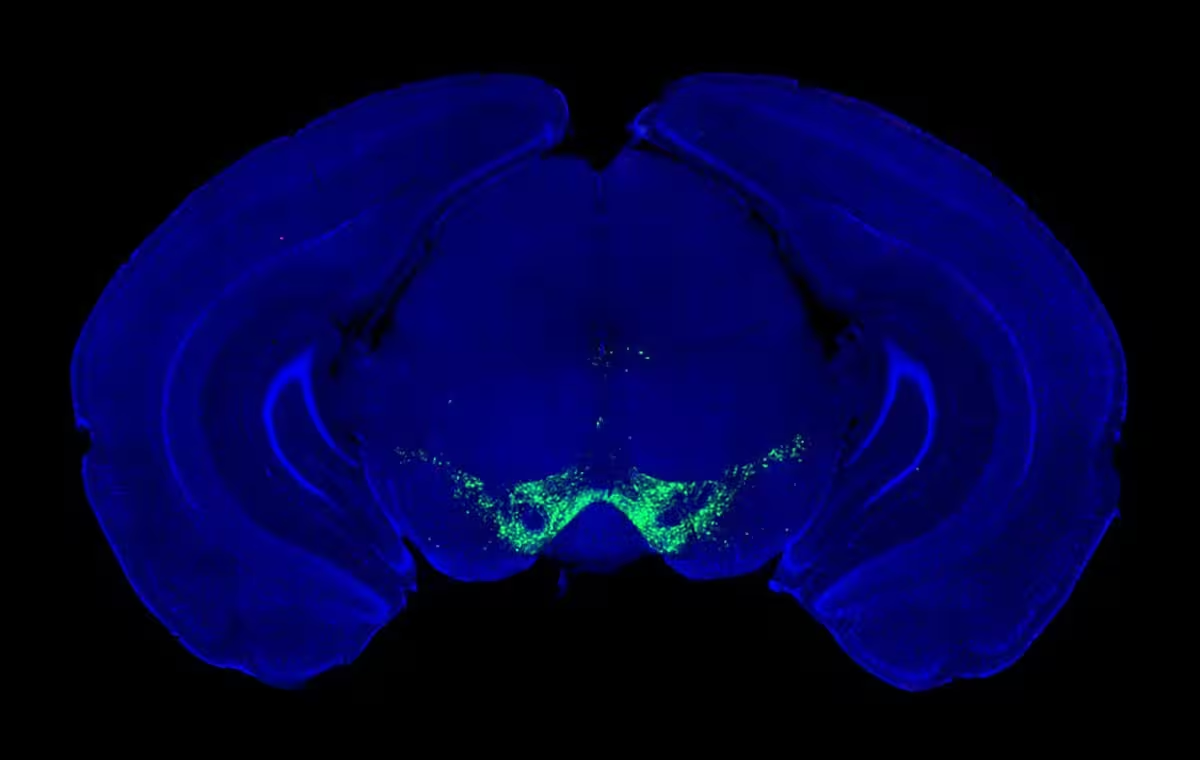
تصویر میکروسکوپی فلورسانس از نورونهای تولیدکنندهٔ دوپامین (سبز) در میانمغز یک موش.
فرض اولیه این بود که اگر جهشهای سریع دوپامین بهصورت مستقیم توان حرکتی را کنترل میکنند، دستکاری مصنوعی آن جهشها دقیقاً در لحظهٔ اجرا باید سرعت یا نیرو را تغییر دهد. متناقض با این انتظار، دستکاریهای کوتاهمدت نتایج پایدار و یکسانی روی شدت هر فشار نشان ندادند. در عوض پژوهشگران دریافتند که لوودوپا حرکت را با بالا بردن سطح پایهٔ کلی دوپامین مغز — همان سیگنال حالت پایدار — بهبود میدهد، بدون آنکه لزوماً پیکهای سریع مرتبط با حرکت را بازیابی کند.
برای تحلیل دقیقتر، پژوهشگران تفکیک زمانی سیگنالهای دوپامینی را بررسی کردند و تفاوت میان پاسخهای فازیک (که معمولاً با پاداش یا رویدادهای لحظهای ارتباط دارند) و تونیک یا زمینهای را تشریح نمودند. نتایج نشان میداد که توان حرکتی وابستگی بیشتری به سطح زمینهای و فراگیر دوپامین دارد تا به نوسانات کوتاهمدت.
این روششناسی ترکیبی — ثبت عصبی حساس، آزمایشهای رفتاری کنترلشده و دستکاری اپتوژنتیک — کیفیت شواهد را بالا میبرد و امکان تفکیک مکانی و زمانی عملکرد دوپامین در مسیرهای حرکتی میانمغزی و جسم سیاه (substantia nigra) را فراهم میسازد.
پیامدها برای درمان و پژوهش پارکینسون
این بازخوانیِ نقش دوپامین چند پرسش باز در پژوهش پارکینسون را بازسازی میکند. اگر دسترسی به دوپامین پایهای عامل مجازکنندهٔ اصلی برای حرکت باشد، درمانهایی که سطح تونیک دوپامین را تثبیت میکنند میتوانند به همان اندازه — یا حتی بیشتر — از مداخلاتی که میکوشند پیکهای فازیک را شبیهسازی کنند، اهمیت داشته باشند. این دیدگاه میتواند دلیل مؤثریت مداوم لوودوپا را توضیح دهد؛ لوودوپا سطح کلی در دسترس بودن دوپامین را افزایش میدهد و به همین ترتیب عملکرد حرکتی را بهبود میبخشد.
علاوه بر این، این یافته هدفی روشنتر برای توسعهٔ دارو ارائه میدهد. آگونیستهای گیرندهٔ دوپامینی قبلاً آزمایش شدهاند اما اغلب بهدلیل اثرات گسترده روی مدارهای مختلف مغزی باعث عوارض جانبی نامطلوب شدند. طراحی درمانهایی که سطح پایهٔ مناسب دوپامین را در مسیرهای حرکتی مشخص بازگردانند یا حفظ کنند میتواند هم اثرات درمانی را نگه دارد و هم عوارض جانبی را کاهش دهد.
در سطح بالینی، این دیدگاه میتواند نحوهٔ اندازهگیری پاسخ درمانی را نیز تغییر دهد: بهجای تمرکز صرف بر روی نوسانات کوتاهمدت یا معیارهای رفتاری یک تک عمل، اندازهگیری شاخصهایی که سطح پایهٔ دوپامین یا تنوس (tonicity) را منعکس میکنند ممکن است نشانگر بهتر و قابلاطمینانتری برای ارزیابی اثربخشی درمانها باشند. این شامل توسعهٔ بیومارکرهای تصویربرداری مولکولی، روشهای الکتروفیزیولوژیک یا حتی پروتکلهای آزمایشی رفتاری میشود که حساس به تغییرات تونیک هستند.
همچنین از منظر داروسازی، هدفگیری مسیرهای سلولی یا بیوشیمیایی خاص که سطح تونیک دوپامین را تنظیم میکنند (مانند تنظیمکنندههای سنتز، بازجذب و تجزیهٔ دوپامین) میتواند راهی برای ایجاد داروهایی با پنجرهٔ درمانی وسیعتر و عوارض کمتر فراهم کند. این رویکرد ممکن است شامل ترکیب داروها، تحویل موضعی یا فرمولاسیونهایی با آزادسازی طولانیمدت برای حفظ سطح ثابتی از انتقالدهنده در مدارهای حرکتی باشد.
گامهای بعدی برای پژوهشگران
کارهای آینده باید بررسی کنند که آیا همین اصول در پریماتها و انسانها نیز برقرار است و چگونه سطح پایهٔ دوپامین با دیگر نورومدولاتورها و تغییرات سطح مدار در بیماری پارکینسون تعامل دارد. بهویژه، باید نقش ترکیبی نوراپینفرین، سروتونین و آستروسیتها و میکروگلیا در پیکربندی سطح تونیک دوپامین و قابلیت حرکت مدنظر قرار گیرد.
برای محققان بنیادی، پرسشهایی مانند مکان دقیق تنظیم تونیک دوپامین، نقش گیرندههای زیرنوع D1 و D2 در سطوح پایه، و چگونگی تطبیق سیناپسها و شبکهها در پاسخ به کاهش دوپامین، از جمله موضوعات مهم هستند. از منظر ترجمهای، مطالعات طولی در بیماران تحت درمان با لوودوپا یا آگونیستها، همراه با نشانگرهای زیستی مولکولی و تصویربرداری فانکشنال، میتواند به درک بهتر رابطهٔ میان سطح پایه و کیفیت حرکت کمک کند.
بالینیها و توسعهدهندگان دارو نیز به دنبال بیومارکرهایی خواهند بود که بازتابدهندهٔ عملکرد دوپامین تونیک باشند؛ این بیومارکرها میتوانند در طراحی کارآزماییهای بالینی، تعیین دوز مناسب و شخصیسازی درمان مبتنی بر وضعیت پایهٔ دوپامین بیمار کمککننده باشند.
در نهایت، تحقیقات ترجمهای باید پیامدهای رفتاری و زندگی روزمره را مدنظر قرار دهند: چگونه تثبیت سطح پایهٔ دوپامین روی کیفیت حرکت، کاهش افتادن، توانایی در انجام فعالیتهای روزانه و پاسخ به تمرینات توانبخشی تأثیر میگذارد؟ پاسخ به این سوالات برای بهینهسازی درمانهای ترکیبی (دارویی و غیردارویی) اهمیت بالایی دارد.
نتیجهگیری
با تغییر تمرکز از پیکهای سریع دوپامین به نقش حمایتی سطح پایه، این مطالعه نحوهٔ فهم ما از کنترل حرکتی را بازتعریف میکند و راهبردهای دقیقتری را برای درمان بیماری پارکینسون پیشنهاد میدهد. نتیجه یک تصویر مکانیکی واضحتر و احتمالاً مسیری سادهتر بهسوی درمانهایی ایمنتر و مؤثرتر است.
این یافتهها نشان میدهد که نگاه همزمان به هر دو جنبهٔ دینامیک دوپامین — تونیک و فازیک — و درک تعامل آنها با شبکههای حرکتی و سایر نورومدولاتورها برای توسعهٔ درمانهای آینده حیاتی خواهد بود. به عبارت دیگر، بهجای تمرکز صرف بر افزایش واکنشهای لحظهای، باید راههایی برای حفظ و تنظیم سطوح پایهٔ دوپامین در مسیرهای کلیدی پیدا کنیم تا عملکرد حرکتی به شکل پایدارتر و قابلپیشبینیتر بازگردد.
همچنین این مطالعه فرصتی برای بازاندیشی معیارهای موفقیت در درمان پارکینسون فراهم میآورد: موفقیت ممکن است نه تنها در کاهش نوسانات کوتاهمدت بلکه در بازگرداندن تونیسیتهٔ مناسب دوپامین و بهبود کیفیت حرکت روزمره معنا پیدا کند. پژوهشهای آتی و توسعهٔ داروهایی که این هدف را دنبال کنند میتوانند تأثیر چشمگیری بر کیفیت زندگی بیماران پارکینسون داشته باشند.
منبع: scitechdaily
نظرات
پمپزون
خوبه ولی کمی اغراق داره، نباید فازیک رو کامل کنار بذاریم. بااینحال مسیر درمانی سادهتر جذابه.
ماکس_
تو کارهای بالینی دیدم بیمارا با لوودوپا بهتر میشن، ولی دلیلش همون تونیک بود؟ خاطرم نیمهکاره، اما حس میکنم ربط داره
آرمین
این واقعاً به انسان قابل تعمیمه؟ آزمایش روی موش خوبه ولی همیشه فرق میکنه... کسی دادههای بالینی هم داره؟
بیونیکس
منطقش خیلی میاد، تمرکز روی تونیک بهنظر معقولتره. ولی جزئیات مسیرها رو باید دید، زود قضاوت نشه.
دیتاپالس
وااای، یعنی دوپامین مثل روغنه نه تراتل؟ عجیب اما امیدوارکننده؛ اگه واقعاً سطح پایه کلید باشه، درمانها سادهتر میشه... امیدوارم روی انسان هم تایید بشه 🤞

ارسال نظر