8 دقیقه
پژوهشگران دانشگاه ورمانت یک «ترمز» مولکولی نامنتظره بر حسگرهای فشار در رگهای مغزی را شناسایی کردهاند — و بازیابی این ترمز میتواند راه جدیدی برای درمان کاهش جریان خون مغزی و برخی انواع زوال عقل باشد. این کشف نشان میدهد که یک فسفولیپید غشایی به نام PIP2 میتواند اهرمی درمانی برای نرمالسازی گردش خون و محافظت از عملکرد مغز باشد.
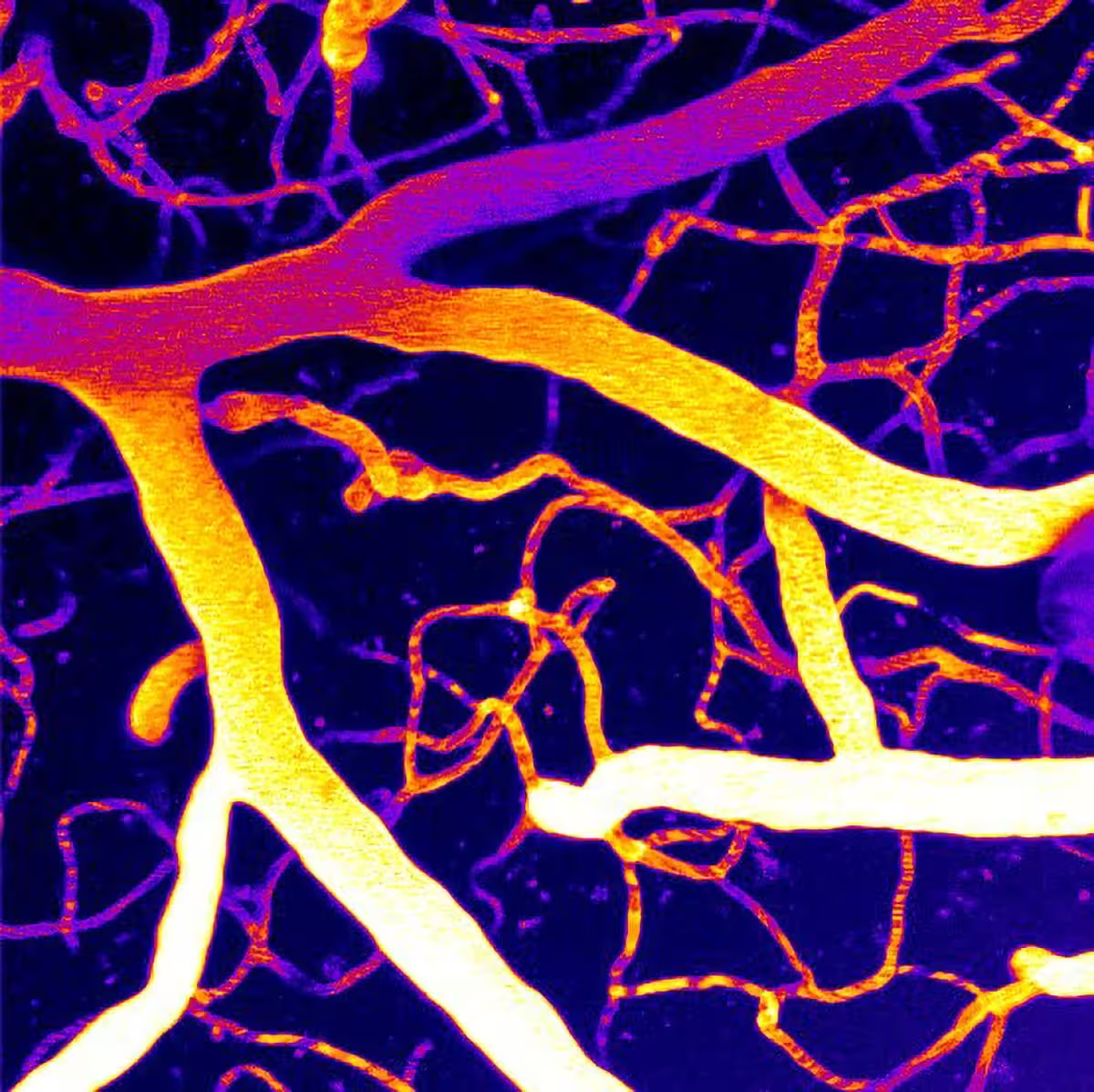
میکروسیرکولاسیون (شبکه ریزعروقی) مغز که با میکروسکوپ لیزر دو فوتونی تصویربرداری شده است.
چگونه یک لیپید غشایی جریان خون مغز را پایدار نگه میدارد
حفظ جریان خون پایدار در مغز نیازمند هماهنگی بسیار دقیق میان خون، دیواره رگها و بافت عصبی مجاور است. در مرکز این کنترل مکانیکی-سلولی کانال یونی حسگر فشار Piezo1 قرار دارد که در سلولهای عروقی بیان میشود. Piezo1 در پاسخ به نیروهای مکانیکی ناشی از جریان خون باز میشود و به رگها اجازه میدهد تا تن و قطر خود را تنظیم کنند؛ این سازوکار برای تامین اکسیژن و مواد مغذی به بافت عصبی و همچنین حفظ هموستاز محلی حیاتی است.
در کارهای پیشبالینی منتشرشده در نشریه Proceedings of the National Academy of Sciences، تیمی به سرپرستی اسامه حراز، دکترای علوم، در دانشکده پزشکی لارنر نشان دادند که فعالیت Piezo1 میتواند وقتی فسفولیپید غشایی فسفاتیدیلاینوزیتول 4,5-بیسفسفات (PIP2) کاهش مییابد، بدون کنترل شود. PIP2 نقش تنظیمکننده در بسیاری از کانالهای یونی و مسیرهای انتقال سیگنال دارد. در این مطالعه، PIP2 به مثابه یک مهارکننده طبیعی برای Piezo1 عمل میکند: هرگاه سطوح PIP2 افت کند، Piezo1 بیشفعّال شده و تعادل جریان خون مغزی را دچار اختلال میکند؛ نتیجهای که پیامدهای قابلتوجهی برای میکروسیرکولاسیون، پرفیوژن بافتی و سلامت نورونها دارد.
از ظرف آزمایش تا بازگرداندن گردش خون: بازیابی PIP2
حراز و همکارانش با استفاده از مدلهای حیوانی آزمایش کردند که آیا تأمین مجدد PIP2 میتواند فعالیت بیشازحد Piezo1 را مهار کرده و جریان خون طبیعی را بازگرداند یا خیر. نتایج آنها نشان داد بازیابی سطح PIP2 باعث سرکوب فعالیت مفرط Piezo1 شد و به تثبیت گردش خون میکروسکوئلار در مغز کمک کرد. این تغییرات بهطور معنیداری با بهبود شاخصهای پرفیوژن مغزی همراه بود؛ شاخصهایی که معمولاً در بیماران مبتلا به زوال عقل مختل میشوند و قابلاندازهگیری با روشهای تصویربرداری عملکردی مانند MRI پرفیوژن و تکنیکهای میکروسکوپی هستند.
این آزمایشهای پیشبالینی بر چند جنبه فنی و بیولوژیک تمرکز داشتند: اندازهگیری جریان خون موضعی، ثبت الکتروفیزیولوژیک فعالیت کانالهای یونی در سلولهای اندوتلیال و عضله صاف عروقی، و همچنین ارزیابی نشانگرهای نورولوژیک مرتبط با پرفیوژن. نتایج نشان داد که بازگرداندن PIP2 نه تنها فعالیت کانال Piezo1 را تعدیل میکند، بلکه اثرات مفیدی روی اکسیژنرسانی بافتی و پاکسازی متابولیک دارد؛ فرایندهایی که در حفظ عملکرد شناختی اهمیت دارند.
«این کشف گامی بزرگ در تلاشهای ما برای پیشگیری از زوال عقل و بیماریهای نورواسکولار است،» حراز گفت. «ما در حال آشکارسازی مکانیزمهای پیچیده این شرایط ناتوانکننده هستیم و اکنون میتوانیم درباره چگونگی ترجمه این زیستشناسی به درمانها فکر کنیم.»
چرا این موضوع برای آلزایمر و زوال عقل مرتبط اهمیت دارد
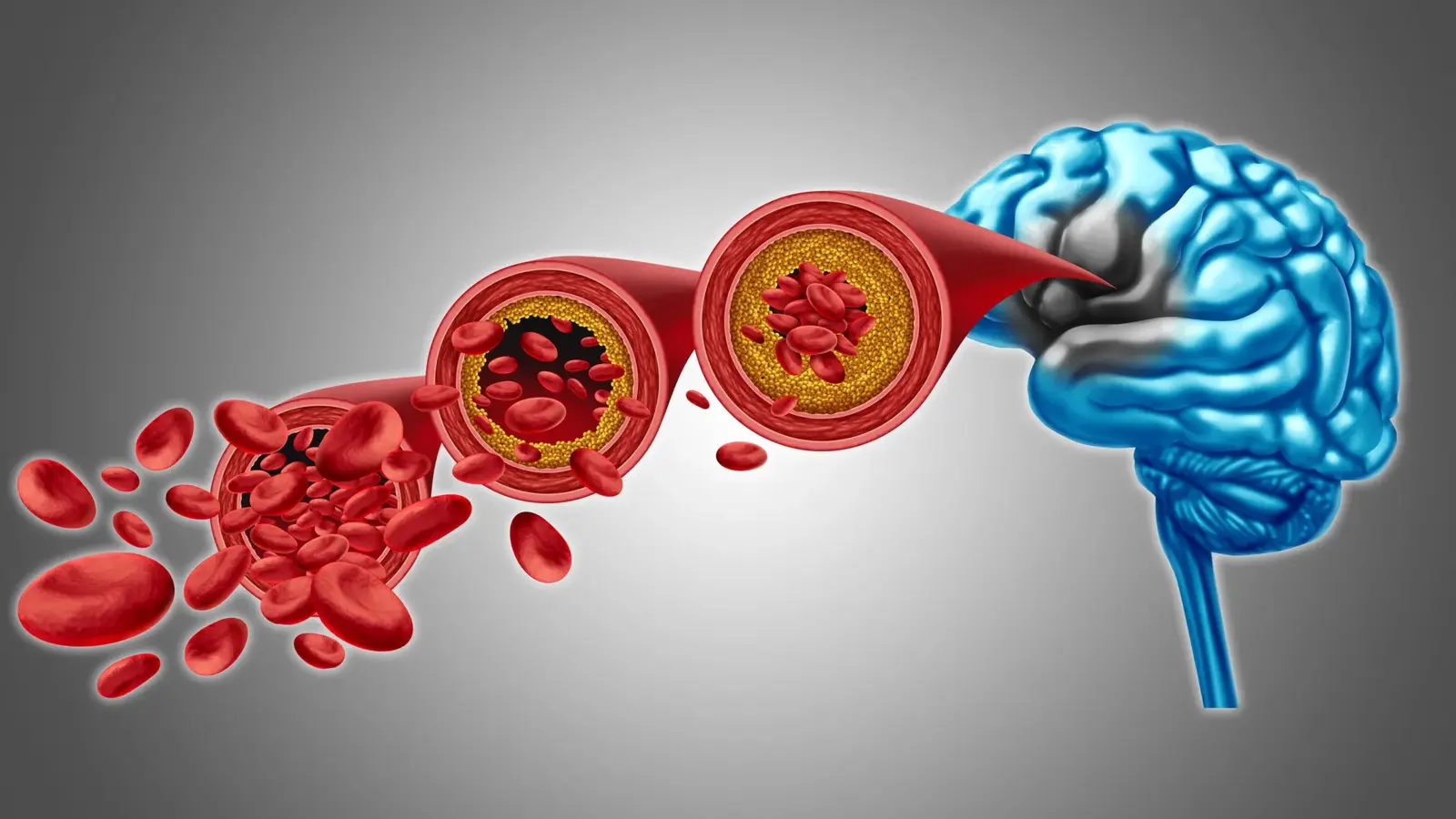
بیماری آلزایمر و دیگر انواع زوال عقل هماکنون دهها میلیون نفر را در سراسر جهان درگیر کردهاند، و نارسایی عروقی بهطور فزایندهای بهعنوان یک عامل مهم در کاهش شناختی شناخته میشود. کاهش جریان خون مغزی، اختلال در پاکسازی محصولات متابولیک و آسیب مزمن به ریزعروق همه میتوانند باعث تسریع در نارسایی نورونی شوند. بنابراین هر سازوکاری که بتواند پرفیوژن محلی را بازگرداند یا محافظت کند، پتانسیل قابلتوجهی برای کاهش یا کند کردن پیشرفت اختلالات شناختی دارد.
کار دانشگاه ورمانت یک زنجیره مکانیکی را نشان میدهد: کاهش PIP2 → فعالیت کنترلنشده Piezo1 در سلولهای رگهای مغزی → اختلال در جریان خون مغزی → تشدید احتمالی علائم زوال عقل. با هدفگذاری یکی از این حلقهها — یا احیای سطوح PIP2 و یا تعدیل عملکرد Piezo1 — پژوهشگران امیدوارند تنظیم عروقی را که بافت مغز را به اکسیژن و مواد مغذی تامین میکند، بازگردانند. این رویکرد میتواند مکمل درمانهای متمرکز بر آمیلوئید یا تاو باشد، بهویژه در بیمارانی که اجزای عروقی نقش بسطدهندهای در بیماریشان ایفا میکنند.
گامهای بعدی: سایتهای اتصال، فیزیک غشا و توسعه درمان
سؤالات کلیدی بدون پاسخ باقی ماندهاند. آزمایشگاه حراز قصد دارد بهطور دقیق مشخص کند که چگونه PIP2 فعالیت Piezo1 را محدود میکند: آیا PIP2 مستقیماً به مناطقی خاص از پروتئین کانال متصل میشود یا اینکه با تغییر خواص فیزیکی غشا (مانند کشش سطحی، ضخامت یا ترکیب لیپیدی محلی) باعث میشود حفره کانال کمتر در معرض باز شدن قرار گیرد؟ پاسخ دادن به این سؤالات ساختاری-عملکردی مسیرهای توسعه دارو را هدایت خواهد کرد — چه از طریق مولکولهایی که نقش PIP2 را تقلید میکنند، چه از طریق عوامل تقویتکننده تولید موضعی PIP2، یا مهارکنندههای انتخابی Piezo1 که برای رگهای مغزی بهینه شدهاند.
در زمینه توسعه درمان، چند گزینه دارویی و تحویلی قابل بررسی است: حاملهای نوین مانند لیپوزومها و نانوذرات هدفپذیر میتوانند مولکولهای آنالوگ PIP2 یا پیشسازهای آن را به سطوح میکروسری کولاسیون مغزی برسانند؛ یا داروهای کوچک و آنتاگونستهای کانال میتوانند فعالیت Piezo1 را مهار کنند. هر گزینه نیازمند ارزیابی دقیق ایمنی، پایداری بیوشیمیایی و توانایی عبور یا هدفگیری در عروق خونی مغز است.
مطالعات آینده همچنین بررسی خواهند کرد که فرآیندهای بیماریزا چگونه ابتدا باعث کاهش PIP2 میشوند. آیا از دست رفتن PIP2 پیامد التهاب مزمن، تغییرات در متابولیسم لیپیدها، یا دیگر آسیبشناسیهای شایع در مغزهای پیری است؟ درک علل بالادستی (upstream causes) این کاهش، گزینههای مداخلهای را گسترش میدهد و ممکن است نشانگرهای زیستی (بیومارکرها) را برای پیگیری پاسخ به درمان در کارآزماییهای بالینی معرفی کند.

اسامه حراز، دکترای علوم و دانشیار داروشناسی در دانشکده پزشکی لارنر، با میکروسکوپ فلورسانس وایدفیلد به شبکه عروقی مغز در آزمایشگاهش در دانشگاه ورمانت نگاه میکند. چنین تصویربرداریها و تکنیکهای بیوفیزیکی برای پیوند دادن فعالیت مولکولی به فیزیولوژی عروقی حیاتی هستند.
دیدگاه کارشناسان
«هدفگیری تعامل لیپید–کانال یک مرز نوظهور در پزشکی نورواسکولار است،» دکتر مایا سینگ، عصبیشناس که در این مطالعه مشارکت نداشت، میگوید. «اگر جایگزینی PIP2 یا تعدیل Piezo1 با ایمنی مناسب و تحویل به نواحی هدف مغزی ممکن شود، میتواند با حفظ حمایت عروقی مورد نیاز نورونها، مکمل درمانهای متمرکز بر آمیلوئید یا تاو باشد.»
این کشف قدمی اولیه اما امیدوارکننده است. تبدیل آن به درمانهای انسانی نیازمند کار مکانیکی تفصیلی، آزمایشهای ایمنی جامع و طراحی دقیق سامانههای تحویلی است تا میکروسیرکولاسیون مغزی را بدون اثرات جانبی سیستمیک هدفگیری کند. با این حال، با آشکارسازی یک نقطه کنترل مولکولی ملموس برای جریان خون، این پژوهش جهتی جدید برای مقابله با سهمهای عروقی در زوال عقل باز میکند و زمینه را برای ترکیب رویکردهای مولکولی، فیزیولوژیک و تصویربرداری پیشرفته فراهم میسازد.
بهعلاوه، یافتهها پیامدهای گستردهتری برای علوم اعصاب و داروشناسی دارند: ترکیب دادههای الکتروفیزیولوژی کانال، بیوشیمی لیپیدی غشا و مدلهای حیوانی رفتاری میتواند نشان دهد که چگونه تنظیم موضعی کانالهای مکانوسنسور نه تنها جریان خون بلکه فرایندهای نورونال مانند پلاستیسیته، پاکسازی پروتئینها و پاسخهای التهابی را تحت تاثیر قرار میدهد. از منظر بالینی، توسعه نشانگرهای تصویربرداری یا بیومارکرهای خون/مایعات مغزی-نخاعی که کاهش PIP2 یا فعالیت تغییر یافته Piezo1 را منعکس کنند، میتواند سلسلهمراتب مطالعاتی را از آزمایشگاه به کارآزماییهای فاز انسانی تسهیل نماید.
در نهایت، همکاریهای بینرشتهای — از بیوفیزیک و شیمی دارویی تا نورولوژی بالینی و تصویربرداری عملکردی — برای ترجمه این یافتهها به درمانهای مؤثر و ایمن ضروری خواهد بود. این مطالعه نمونهای از چگونگی کشف مولکولی میتواند مسیرهای درمانی جدیدی را برای بیماریهای پیچیده عصبی-عروقی فراهم آورد.
منبع: scitechdaily
نظرات
پمپزون
خیلی بزرگش کردن انگار، ایده جالبه اما نگران عوارض سیستمی ام، لیپوزوم و نانوذرات کلی چالش تحویلی دارن، باید محتاط بود
امیر._
یاد آزمایشگاه افتادم، وقتی ترکیب غشا عوض میشه کانالها واقعا تغییر میکنن، به شرطی که داروها امن باشن و هدفمند برسن سر ناحیه صحیح
رضا
این رو تو مدل حیوانی دیدن خوبه، اما آیا تو انسان هم تکرار میشه؟ کلی عوامل بالادستی هست، التهاب مزمن و متابولیسم لیپید میتونه قضیه رو پیچیده کنه
لابکور
معقول بنظر میاد، هدفگیری لیپید-کانال ایده جالبیه ولی راه زیادی تا درمان مونده، مخصوصا تحویل هدفمند و ایمنی باید ثابت بشه
دیتاپالس
نمیدونستم یه لیپید بتونه تا این حد تاثیر بذاره… جدی؟ اگه بشه PIP2 رو بازیابی کرد، خیلی چیزها عوض میشه! امیدوارم زودتر بررسیهای بالینی شروع شه

ارسال نظر