8 دقیقه
یک مطالعه آزمایشگاهی امیدوارکننده نشان میدهد که یک نامزد دارویی به نام P7C3-A20 میتواند تحلیل شناختی را در مدلهای موش با پاتولوژی پیشرفته شبیه آلزایمر معکوس کند. پژوهشگران گزارش میدهند که با بازگردانی شیمی انرژی سلولی و کاهش التهاب، مغز آسیبدیده میتواند عملکردهای مهمی را بازیابد حتی بدون پاکسازی تجمعات پروتئینی مشخصه بیماری مانند پلاکها و گرههای تاو. این یافتهها مسیر جدیدی در تحقیقات درمانی آلزایمر پیشنهاد میکنند که بر بازتوانی متابولیک و مقاومت متابولیک نورونها تأکید دارد.
How a single compound targets brain energy
محققان در دانشگاه Case Western Reserve و تیمهای همکار، ترکیب نوروپروتکتیو P7C3-A20 را ارزیابی کردند؛ ترکیبی که به بازیابی تعادل نیکوتینآمید آدنین دینوکلئوتید (NAD+) کمک میکند. NAD+ یک مولکول محوری در متابولیسم سلولی است: سلولها از آن برای تبدیل مواد مغذی به انرژی قابل استفاده، حمایت از تعمیر DNA و نگهداری پروتئینها بهره میبرند. کاهش سطح NAD+ با پیری و طیف وسیعی از بیماریهای نورودژنراتیو مرتبط است و به عنوان عامل مهمی در تحلیل عملکرد نورونها شناخته میشود.
در این مطالعه، موشهایی که علائم پیشرفته شبیه آلزایمر داشتند، به مدت شش ماه روزانه تزریق P7C3-A20 را دریافت کردند. درمان باعث بازگشت سطوح NAD+ به محدوده طبیعی، کاهش نشانگرهای التهابی و آسیب DNA و—به طور حیاتی—متوقف شدن تخریب سلولهای مغزی شد. این بهبود زیستشیمیایی در عملکرد مشاهده شد و به صورت افزایشهای قابل اندازهگیری در یادگیری و حافظه در هر دو خط آزمایشی موش ترجمه شد. نتایج رفتاری همراه با دادههای بافتشناسی و مولکولی نشان دهنده بازتوانی عملکردی و پاتولوژیک بود که فراتر از تغییرات موقتی عمل کرد.
Two different Alzheimer's models, one common outcome
تیم پژوهشی عمداً از دو مدل موشی با زمینه ژنتیکی متمایز استفاده کرد که هر یک نمایانگر یکی از دو پاتولوژی شاخص آلزایمر هستند: پلاکهای آمیلوئید-بتا و گرههای پروتئینی تاو. این پروتئینهای تجمعیافته در مغز بیماران آلزایمر انسانی به طور گسترده مشاهده میشوند، اما نقش دقیق آنها در ایجاد اختلالات شناختی پیچیده و محل بحث باقی مانده است. برخی شواهد نشان میدهد که خود تجمع پروتئینی مباشر علت نیست بلکه از طریق ایجاد اختلال در متابولیسم، التهاب و آسیب به شبکههای نورونی موجب نقص عملکرد میشود.
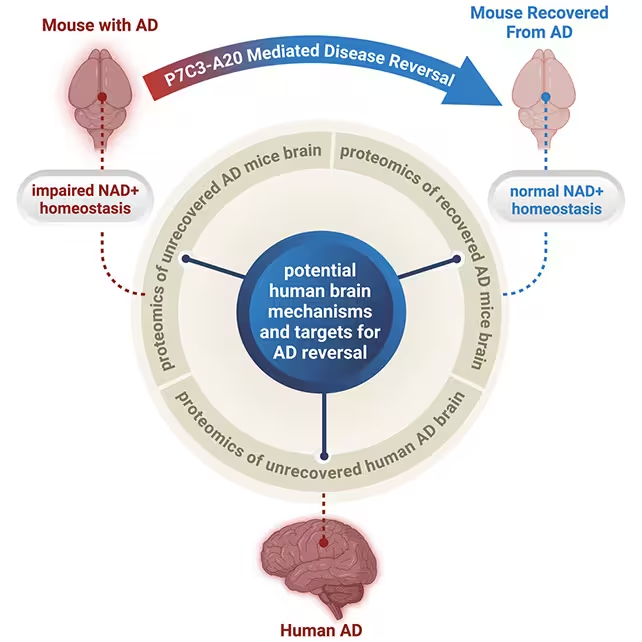
به طرز قابل توجهی، P7C3-A20 رفتار و نشانگرهای نوروبیولوژیک را در هر دو مدل بهبود بخشید بدون اینکه پلاکها یا گرههای تاو بهطور چشمگیر پاکسازی شوند. «بازگردانی تعادل انرژی مغز، بهبود پاتولوژیک و عملکردی را در هر دو خط موش با آلزایمر پیشرفته ایجاد کرد»، میگوید اندرو پیپر، عصبشناس و روانپزشک. این نتیجه نشان میدهد که اگر نورونها مقاومت متابولیک کافی را بازیابند، ممکن است بهتر بتوانند تجمع پروتئینها را تحمل کنند یا به نحوی جبران عملکرد کنند، یعنی به جای تمرکز صرف بر حذف پلاک آمیلوئید یا تاو، تقویت ظرفیت انرژی و تعمیر سلولی میتواند مسیر مؤثری باشد.
What the findings mean for Alzheimer's research
به نظر میرسد بازگردانی NAD+ مکانیزم محوری پشت این بازیابی باشد. پژوهشهای حیوانی قبلی نشان دادهاند که افزایشدهندههای NAD+ میتوانند نتایج بهتری پس از آسیب مغزی ایجاد کنند؛ این کار، این مشاهدات را به زمینه دژنراسیون عصبی مزمن گسترش میدهد. مقاله منتشرشده در Cell Reports Medicine گزارش داد که نشانگرهای التهاب و آسیب DNA در موشهای درمانشده کاهش یافت، که نشان میدهد سلولها ظرفیت بازگرداندن عملکرد طبیعی و مرمت مولکولی را بازیافتهاند. این شامل افزایش فعالیت مسیرهای مربوط به ترمیم DNA، بهبود عملکرد میتوکندریها و تنظیم پاسخ التهابی موضعی میشود.
با این حال، تیم پژوهشی هشدار میدهد که باید محتاط بود. ترجمه نتایج از مدلهای موشی به انسان بهطور شناختهشده دشوار است: دوزدهی، زمانبندی درمان، عوارض جانبی و ایمنی در بلندمدت باید در آزمایشهای بالینی کنترلشده اثبات شوند. پژوهشگران همچنین اشاره میکنند که فعالیت بیش از حد NAD+ در برخی زمینهها با افزایش خطر سرطان مرتبط شده است، بنابراین هر درمان انسانی نیاز به کالیبراسیون دقیق، پایش زیستی و مطالعات امنیتی گسترده دارد. علاوه بر این، تفاوتهای فارماکوکینتیک و فارماکودینامیک بین گونهها ممکن است نتایج میان انسان و موش را متفاوت سازد، بنابراین فازهای پیشبالینی تکمیلی و مدلهای غیرموشی (مثلاً اندامکهای مغزی انسانی و مدلهای بزرگتر) اهمیت دارند.
Why this doesn't mean an instant cure
آلزایمر یک بیماری چند عاملی است که شامل عوامل ژنتیکی، تجمع پروتئینها، التهاب مزمن، سلامت عروقی و عوامل سبک زندگی میشود. اثر P7C3-A20 پلاکها یا گرهها را از بین نمیبرد، اما ممکن است به نورونها اجازه دهد که علیرغم حضور این تجمعات به عملکرد ادامه دهند ــ یک تغییر مفهومی مهم که میتواند چارچوب جدیدی برای درمان ارائه دهد. «دیدن این اثر در دو مدل حیوانی بسیار متفاوت، که هر یک توسط علل ژنتیکی مختلف هدایت میشوند، ایده جدیدی را تقویت میکند که بازیابی از بیماری پیشرفته ممکن است در انسانها نیز وقتی تعادل NAD+ مغز بازگردانده شود، قابل حصول باشد»، پیپر میگوید.
این رویکرد نه بهعنوان درمانی که فوراً پلاکها را حذف میکند، بلکه بهعنوان استراتژیای برای افزایش مقاومت سلولی و بازیابی عملکرد شبکههای عصبی در نظر گرفته میشود. در عمل، این بدان معنی است که بیمارانی که در مراحل مختلف بیماری قرار دارند ممکن است از ترکیبی از اقدامات درمانی بهرهمند شوند: داروهایی برای کاهش بار پروتئینی، داروهایی برای تعدیل التهاب و در کنار آن بازتوانی متابولیک با هدف تقویت NAD+ و بهبود عملکرد میتوکندریها.
Potential paths forward: trials and safety checks
گامهای بعدی شامل کار پیشبالینی تکمیلی برای تعیین پنجرههای دوزدهی بهینه، اثرات بلندمدت و ایمنی در طیفهای سنی و زمینههای ژنتیکی مختلف است. اگر این مطالعات نتایج امیدوارکنندهای نشان دهند، آزمایشهای انسانی با طراحی دقیق میتواند آغاز شود ـ احتمالاً با مطالعههای فاز اول ایمنی در داوطلبان سالم و بیماران با آلزایمر خفیف تا متوسط. تعیین نشانگرهای زیستی (biomarkers) مناسب برای نظارت بر سطح NAD+ و پاسخ درمانی در خون و مایع مغزی-نخاعی بخش مهمی از این برنامه خواهد بود.
پژوهشگران همچنین بررسی خواهند کرد که آیا بازسازی NAD+ بهصورت تنها مؤثرتر است یا در ترکیب با درمانهایی که التهاب، سلامت عروقی و تجمع پروتئین را همزمان هدف میگیرند. با توجه به پیچیدگی آلزایمر، یک استراتژی درمانی چندوجهی منطقی به نظر میرسد؛ این میتواند شامل مهارکنندههای تجمع آمیلوئید، ضدالتهابهای هدفمند، تنظیمکنندههای میتوکندری و مداخلات سبک زندگی باشد. از منظر طراحی کارآزمایی بالینی، ترکیب شدن با درمانهای شناختهشده یا آزمایشی نیازمند طرحهای تصادفیسازی شده و نشانگرهای نتیجهگیری مشخص است تا اثربخشی و تعاملات ایمنی مشخص شوند.
Expert Insight
دکتر لنا مورالس، یک دانشمند ارشد عصبشناس خیالی اما واقعگرایانه در یک دانشگاه تحقیقاتی بزرگ، اظهار میدارد: «این مطالعه نحوه تفکر ما درباره مقاومت در مغز پیری را تغییر میدهد. بهجای تلاش برای حذف همه نشانگرهای پاتولوژیک، تقویت متابولیسم سلولی و سیستمهای تعمیر میتواند به نورونها اجازه دهد که عملکرد خود را بازیابند—دستکم برای مدتی. این رویکردی دلگرمکننده و عملی است که مکمل سایر استراتژیهای درمانی میباشد.»
اگرچه کار زیادی باقی مانده است، این مطالعه مسیری قابل آزمایش و امیدوارکننده پیشنهاد میدهد: با بازتنظیم اقتصاد انرژی مغز ممکن است حتی در مراحل پیشرفته بیماری امکان بازیابی عملکردی وجود داشته باشد. پژوهش در Cell Reports Medicine در سال 2025 منتشر شده است و تیم هدایتکننده بر انجام پیگیریهای دقیق و روشمند قبل از هر کاربرد انسانی تأکید میکند. برای افزایش اطمینان علمی، نیاز به دادههای مستقل، بازتولید نتایج در آزمایشگاههای دیگر، و مطالعات طولانیمدت روی ایمنی و اثربخشی وجود دارد تا مشخص شود که آیا نتایج موشی میتواند به مزیت بالینی قابل توجهی در بیماران آلزایمر منجر شود یا خیر.
منبع: sciencealert
نظرات
داوین
داییم آلزایمر داشت، این جور خبرها آدمو امیدوار میکنه. کاش زودتر فازهای بالینی شفاف و عمومی بشن 🙏
توربو
احتمالا زیاد بزرگش نکنیم، پلاک و تاو هم مهمن؛ این بیشتر یه رویکرد مکمله. امیدوارم عوارض نداشته باشه
آرمین
معقول به نظر میاد، بازتوانی متابولیکی میتونه کلید باشه. ولی باید صبر کنیم و دادههای بالینی ببینیم.
بیونیکس
امیدوره اما، آیا دوز و ایمنی طولانی مدت مشخصه؟ ترجمه از موش به انسان همیشه پر از سواله و پیچیدگی
رودایکس
وای، اگه واقعاً P7C3-A20 بتونه حافظه رو برگردونه، زندگی خیلیا زیر و رو میشه... ولی واقعاً توی انسان چطور جواب میده؟


ارسال نظر