8 دقیقه
تحقیقات جدید نشان میدهد که عدمتعادل در جمعیت باکتریهای روده میتواند سیمکشی عصبی مغز را بازسازی کند و رفتارهای شبیه افسردگی مرتبط با اختلال دوقطبی را تولید نماید — حداقل در مدلهای موشی. با پیوند میکروبیوتای مدفوعی از افراد در فاز افسردگی بیماری دوقطبی به جوندگان، پژوهشگران توانستند هم نشانههای رفتاری و هم ویژگیهای عصبی مرتبط با این اختلال را بازتولید کنند. این یافتهها اهمیت محور روده-مغز و نقش میکروبیوم روده در سلامت روان و اختلالات خلقی را برجسته میسازند و شواهدی ارائه میدهند که میتواند راهگشای رویکردهای درمانی مبتنی بر میکروبیوم در آینده باشد.
چگونگی آزمایش روی موشها — و چرا اهمیت دارد
محققان دانشگاه ژجیانگ نمونههای مدفوع داوطلبانی را که مبتلا به اختلال دوقطبی و در فاز افسردگی بودند، به موشهای آزمایشگاهی انتقال دادند. تیم تحقیقاتی از ترکیب آزمونهای رفتاری، تصویربرداری مغزی و توالییابی ژنتیکی برای دنبال کردن تغییرات پس از پیوند استفاده کرد. در مقایسه با موشهایی که با نمونههای باکتریایی اهداکنندگان سالم تیمار شدند، گیرندگان میکروبیوتای منبعشده از بیماران دوقطبی حرکت کمتری داشتند، علاقهی آنها به غذاهای تشویقی کاهش یافت و دیگر نشانههای کلاسیکی که در مدلهای حیوانی افسردگی بهکار میروند، در آنها پدیدار شد.
چرایی اهمیت این یافته ساده است: مدلهای حیوانی به دانشمندان اجازه میدهند یک متغیر را در هر زمان جدا کنند. در این مطالعه متغیر مداخلهای، میکروبیوتای روده بود. وقتی تغییرات رفتاری تنها در موشهایی دیده شد که با میکروبیوتای منشاء دوقطبی تیمار شده بودند، ارتباط بین ترکیب میکروبی روده و عملکرد مدارهای مغزی مرتبط با خلق و خو قویتر و قابلاستنادتر شد. این شیوه پژوهش کنترل شده، اعتبار شواهد را در زمینه ارتباط میکروبیوم روده و اختلالات خلقی افزایش میدهد و نشان میدهد که تغییرات میکروبی میتواند مستقیماً بر رفتار و نوروفیزیولوژی تاثیر بگذارد.
آنچه تصویربرداری مغزی و آزمایشهای سلولی نشان داد
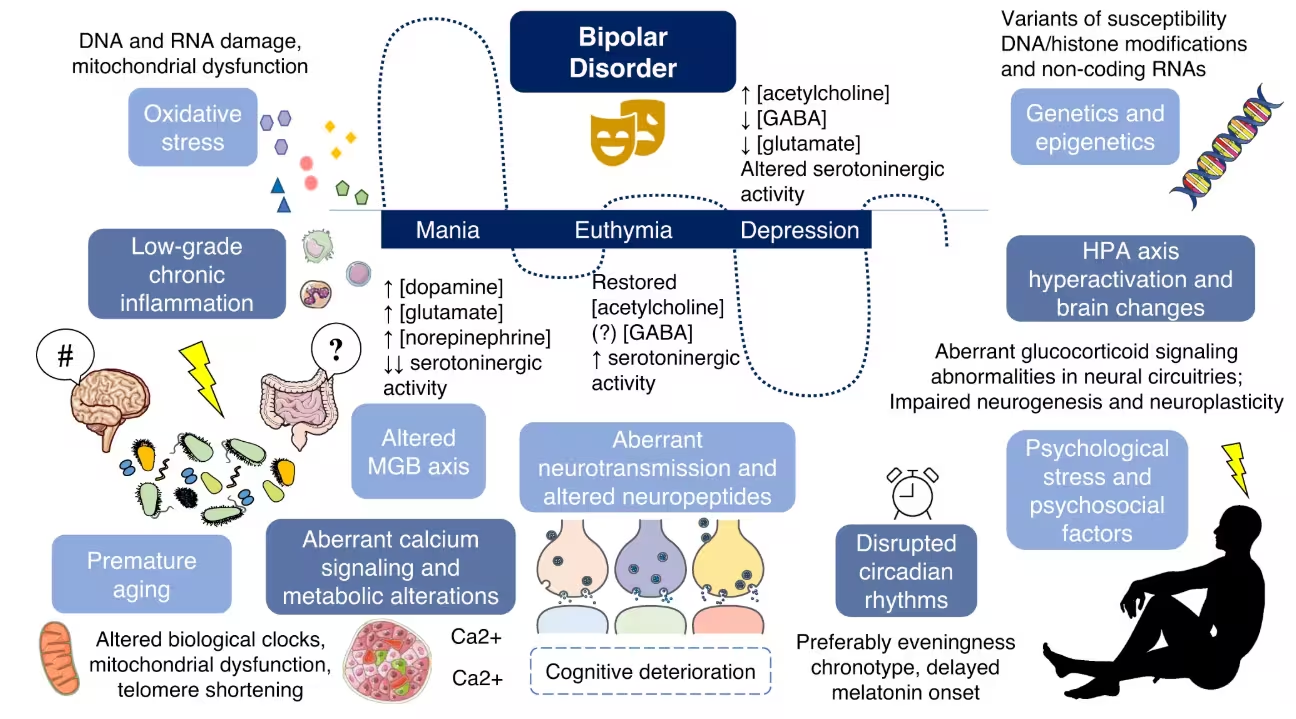
مغز موشهای تحت تاثیر تغییرات میکروبی نشاندهنده تغییرات اختصاصی در قشر پیشپیشانی میانی (mPFC) بود؛ ناحیهای که در تصمیمگیری، تنظیم عاطفی و پردازش پاداش نقش محوری دارد. مطالعه کاهش اتصال سیناپسی را گزارش کرد — که به معنای کاهش اتصالات فیزیکی میان نورونها است — و همچنین تضعیف اتصال بین mPFC و مدارهای پردازش پاداش. به طور خلاصه، مرکز پاداش مغز بهطور عملکردی بخشی مستقل یا کماثر به نظر میرسید که با جنبههای مرکزی رفتار افسرده مانند آنهدونیا (کاهش توانایی احساس لذت) تطابق دارد.
توالییابی ژنتیکی میکروبیوتای پیوندی نشاندهنده افزایش سطوح برخی جنسهای باکتریایی بود که قبلاً با پیامدهای نامطلوب سلامت مرتبط شدهاند، از جمله Klebsiella و Alistipes. این جنسها در مطالعات پیشین نیز بهعنوان عوامل بالقوه تأثیرگذار بر خلق و خو مطرح شدهاند، اگرچه نویسندگان تأکید میکنند که برای تعیین رابطه علیت-معلول در سطح گونهای نیاز به پژوهشهای دقیقتر و تحلیلیتر هست. علاوه بر نامهای جنس باکتری، تغییر در فراوانی متابولیتهای میکروبی، محصولات متابولیسمی و مسیرهای التهابی نیز میتواند واسطه تغییرات نورونی باشد؛ بنابراین تحلیل توالی، متابولومیکس و کارکرد ایمنی باید همزمان بررسی شوند تا مکانیسمهای مولکولی روشن شوند.
چرا لیتیوم، نه فلوکستین، بهبود ایجاد کرد
برای بررسی اینکه آیا افسردگی القا شده بیش از آنکه شبیه افسردگی تکقطبی باشد، شبیه افسردگی دوقطبی است یا خیر، پژوهشگران دو دارو را آزمایش کردند: فلوکستین (یک مهارکننده بازجذب سروتونین یا SSRI که معمولاً در افسردگی عمده استفاده میشود) و لیتیوم (یک تثبیتکننده خلق خط اول برای اختلال دوقطبی). فلوکستین رفتار طبیعی را بازنساخت نکرد، اما لیتیوم منجر به نجات قابلتوجهی در رفتار شد.
این الگو با تجربه بالینی همراستا است: اپیزودهای افسردگی در اختلال دوقطبی اغلب نسبت به داروهای ضدافسردگی پاسخ متفاوتی دارند تا افسردگی تکقطبی. اثرات شناختهشده لیتیوم بر سیگنالدهی دوپامین و الگوهای شلیک نورونها ممکن است به فعالسازی مجدد مسیرهای پاداش کمک کند که توسط میکروبیوم تغییر یافته دچار اختلال شده بودند. مکانیسمهای احتمالی شامل تنظیم مسیرهای کیناز درون سلولی، محافظت سیناپسی، کاهش استرس اکسیداتیو و تعدیل ایمنی مرکزی هستند که همگی میتوانند به بازگرداندن همبستگی مدارهای پاداش و رفتارهای انگیزشی کمک نمایند.
تصویر بزرگتر: میکروبهای روده بهعنوان بخشی از یک پازل پیچیده
نویسندگان و کارشناسان مستقل هشدار میدهند که بعید است باکتریهای روده تنها علت اختلال دوقطبی باشند. این بیماری از تلاقی عوامل ژنتیکی، محیطی و سبک زندگی ناشی میشود — و محور میکروبیوتا-روده-مغز (MGB) یکی از لایههای مشارکتکننده است. با این حال، این یافتهها از مدلی پشتیبانی میکنند که طی آن عدمتعادل میکروبی میتواند حساسیت به بیثباتی خلقی را افزایش دهد یا با تغییر اتصال عصبی شدت علائم را تشدید نماید. درک نقش میکروبیوتا به ما کمک میکند تصویر زیستپزشکی گستردهتری از اختلالات خلقی مانند اختلال دوقطبی بسازیم.
اگر این نتایج در مطالعات مستقل تکرار شوند و به انسان تعمیم یابند، پنجرههای درمانی جدیدی باز میشود: مداخلات هدفمند روی میکروبیوم، از جمله پروبیوتیکهای دقیق، پریبیوتیکها، تغییرات رژیمی هدفدار و بازسازی میکروبیوتا (مانند پیوند میکروبیوتای مدفوع با پروتکلهای کنترلشده) ممکن است روزی مکمل دارودرمانی و رواندرمانی شوند. البته پیش از کاربرد بالینی باید ایمنی، پایداری اثر و مناسبت هر مداخله برای بیماران دوقطبی ارزیابی شود. در حال حاضر این مطالعه نشان میدهد که تغییر در جوامع رودهای میتواند تاثیرات مستقیم و قابلاندازهگیری بر مدارهای مغزی مرتبط با افسردگی دوقطبی داشته باشد.
پیامدها برای تشخیص و پژوهشهای آینده
اشتباه در تشخیص اختلال دوقطبی شایع است، تا حدی به این دلیل که اپیزودهای افسردگی ممکن است شبیه افسردگی عمده به نظر برسند. شناسایی نشانههای زیستی — چه میکروبی، چه مولکولی یا سطح مدار عصبی — که افسردگی دوقطبی را از انواع دیگر متمایز میسازند میتواند تشخیص زودهنگام را بهبود بخشد و راهنمایی برای انتخاب درمان مناسب فراهم آورد. مطالعه منتشرشده در مجله Molecular Psychiatry خواستار تحقیقات بیشتر درباره باکتریهای مشخصی است که تغییرات عصبی را ایجاد میکنند و اینکه آیا الگوهای مشابه در انسانها مشاهده میشود یا خیر.
علاوه بر تحقیق علت و معلول، مطالعات آینده باید به موارد زیر بپردازند: طراحی آزمایشهای طولی در جمعیتهای انسانی، تحلیل همبسته بین تغییرات میکروبی و بیومارکرهای التهابی یا متابولیتی، ارزیابی پاسخ به مداخلات دارویی و میکروبی، و توسعه رویکردهای درمانی ترکیبی. همچنین باید به تنوع فردی میکروبیوم و اثرات عوامل محیطی مانند رژیم غذایی، مصرف آنتیبیوتیک، خواب و استرس توجه نمود، زیرا این عوامل میتوانند هم روی میکروبیوم و هم روی خطر ابتلا به اختلالات خلقی تاثیر بگذارند.
نکات فنی و تفسیر دادهها
برای خوانندگان تخصصیتر لازم است به برخی جزئیات فنی اشاره شود: مطالعه از توالییابی 16S rRNA برای شناسایی تغییرات جنسهای باکتریایی استفاده کرده است، که برای دید کلی از تغییرات ترکیبی مناسب است اما تفکیک گونهای و عملکردی محدودیتهایی دارد. برای تعیین نقش متابولیتهای باکتریایی و مسیرهای مولکولی واسطه، ادغام متابولومیکس، ترنسکریپتومیکس و پروتئومیکس توصیه میشود. همچنین ارزیابیهای عملکردی مانند تولید متابولیتهای کوتاهزنجیر اسید چرب (SCFA)، لیپوکالینها و تعامل با پاسخ ایمنی میزبان میتواند نشان دهد که چگونه میکروارگانیسمها مستقیماً یا غیرمستقیم بر نورونها تأثیر میگذارند.
از نظر تصویربرداری، ترکیب MRI ساختاری و عملکردی با تکنیکهای الکترونیک در سطح نورون (مثل ثبت تکسلولی و مطالعات الکتروفیزیولوژیک) امکان میدهد تا همبستگی بین تغییرات ساختاری-سایزی و عملکرد مدارها بهتر تبیین شود. در نهایت، مدلسازی شبکههای عصبی و شبیهسازیهای بیوفیزیکی میتواند به پیشبینی نتایج مداخلات میکروبی کمک کند و نشان دهد که کدام اهداف میکروبی بیشترین پتانسیل را برای اصلاح مدارهای پاداش دارند.
بینش تخصصی
«این مطالعه ایده ارتباط معنیدار بین روده و مغز را در زمینه اختلالات روانپزشکی تقویت میکند»، میگوید دکتر امیلی هارت، نوروساینتیست بالینی (شخصیت ساختگی) که روی اختلالات خلقی و میکروبیوم پژوهش میکند. «واکنشپذیری به لیتیوم خصوصاً قابلتوجه است: این امر نشان میدهد که سیگنال باکتریایی با سامانههای عصبیای تعامل میکند که بهطور شناختهشدهای در اختلال دوقطبی مرکزی هستند. گام بعدی انجام پژوهشهای انسانی دقیق است که گونه یا سویههای باکتریایی خاص را به تغییرات قابلاندازهگیری در مدارها پیوند دهد.»
پژوهشهای بعدی باید علیت را در انسانها تأیید کنند، اهداف میکروبی قابلعمل را شناسایی نمایند و ایمنی و اثربخشی مداخلات مبتنی بر میکروبیوم را بهعنوان همراهی برای درمانهای فعلی اختلال دوقطبی آزمایش کنند. تا آن زمان، این مطالعه یک پایه آزمایشی قوی فراهم میآورد که نشان میدهد تغییرات در جوامع میکروبی روده میتواند به طور مستقیم روی مدارهای مغزی تاثیر بگذارد و در شکلگیری یا تشدید علائم افسردگی نقش داشته باشد.
منبع: sciencealert
نظرات
نووا_ک
مطالعه فنی و جامعیه، بیشترین نکته اینه که باید ترکیب توالی، متابولوم و ایمونولوژی رو با هم ببینن... گام بعدی انسانیه.
پمپزون
تو خانوادهمون کسی با دوقطبی هست، بعضی رفتارها آشنا بود؛ خوشم اومد اما فکر نمیکنم فقط باکتری باشه 😕
مکس_
خوبه ولی کمی جار زده شده، هنوز راه درازیه تا درمان بالینی، مخصوصا ایمنی و پایداری اثر.
دیتاپالس
معقول به نظر میاد، میکروبیوم مهمه ولی نه تنها علت؛ باید چندرشتهای بررسی شه
آرش
واقعا؟ فقط موش بود، این یعنی ممکنه در انسان هم باشه یا نه؟ خیلی سوال پیش میاد، من شک دارم به تعمیمش.
بایونیکس
وای، باکتریها میتونن سیمکشی مغز رو بازتنظیم کنن... واقعاً امیدبخشه اما کلی تحقیق روی آدم لازم هست.

ارسال نظر