9 دقیقه
یک میکروب آشنا در دستگاه تنفسی در جایی کمتر انتظار میرود یافت شده است: در پشت چشم. پژوهشگران گزارش دادهاند که سطوح بالاتری از Chlamydia pneumoniae در شبکیه افراد مبتلا به بیماری آلزایمر مشاهده شده است؛ یافتهای که نحوه نگاه دانشمندان به عفونت، التهاب و نورودژنراسیون را بازتعریف میکند.
از ریه تا شبکیه: پژوهش چه کار کرد و چرا اهمیت دارد
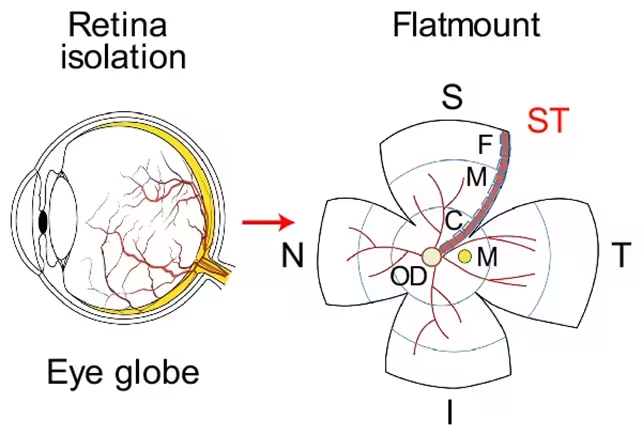
این کار که توسط تیمی در مرکز پزشکی Cedars-Sinai رهبری شد، بافتهای چشم و مغز 104 فرد فوتشده را بررسی کرد؛ نمونهها طیفی از افراد با شناخت طبیعی تا اختلال شناختی خفیف (MCI) و بیماران با تشخیص بالینی آلزایمر را شامل میشدند. پژوهشگران بر روی شبکیه تمرکز کردند — بافت عصبی نازکی که نور را به سیگنالهای الکتریکی تبدیل میکند و مغز از آن برای ساختن بینایی استفاده میکند — و به دنبال نشانههایی از C. pneumoniae گشتند، باکتریای که معمولاً با برونشیت، پنومونی و سینوزیت مرتبط است.
الگوی روشنی مشاهده شد: در افراد مبتلا به آلزایمر، مقدار باکتری هم در بافت شبکیه و هم در بافت مغز بیشتر بود، و بار بالاتر باکتری با افت شدیدتر شناختی همبستگی داشت. خطر ژنتیکی نیز نقش داشت: بافتهایی از اهداکنندگانی که حامل آللهای مرتبط با آلزایمر در ژن APOE بودند، مقدار بیشتری از باکتری را نسبت به بافت افرادی که آن آللها را نداشتند نشان داد. تفاوت میان گروه کنترل سالم و آنهایی که MCI داشتند کمتر آشکار بود، که نشان میدهد این نشانگر ممکن است با پیشرفت آسیبشناسی تقویت شود.
برای درک بهتر زمینهٔ بالینی و میکروبیولوژیک، نویسندگان روشهای آزمایشگاهی و تشخیصی را به تفصیل شرح دادند: تشخیص شامل تکنیکهایی مانند واکنش زنجیرهای پلیمراز (PCR) برای شناسایی ماده ژنتیکی باکتری، رنگآمیزی ایمنیتوزیعشده (immunohistochemistry) برای تعیین محل سلولی باکتری و تحلیل کمی بار میکروبی در نمونههای شبکیه و بافت مغزی بود. این جزئیات فنی باعث قوت تحلیل و قابلیت بازتولید نتایج در مطالعات بعدی میشود.
زمینه بیولوژیک C. pneumoniae نیز مورد توجه قرار گرفت: این میکروب یک پاتوژن داخلسلولی اجباری است که توانایی ایجاد عفونتهای تنفسی مزمن و پاسخ ایمنی پایدار را دارد. نقش بالقوهٔ آن در بافت عصبی، بهخصوص وقتی با زمینه التهابی یا خطر ژنتیکی ترکیب میشود، مسألهای است که این مطالعه در زمینه تشخیص و پژوهش استراتژیک برجسته میکند.
آزمایشهای آزمایشگاهی، مکانیزمها و محدودیتهای شواهد
همبستگی به تنهایی نمیتواند علت را اثبات کند و تیم پژوهشی این موضوع را تأیید کرد؛ بنابراین پژوهشگران وارد مدلهای سلولی و حیوانی شدند تا بررسی کنند این میکروب عملاً چه تأثیری میتواند داشته باشد. کشتهای عصبی آلوده و حیوانات آلوده واکنش التهابی بیشتری، از دست رفتن نورونهای بیشتر و رسوبهای بزرگتری از آمیلوئید-بتا — تکههای پروتئینی چسبنده که در مغز بیماران مبتلا به آلزایمر تجمع مییابند — نشان دادند. به عبارت سادهتر: ورود این باکتری فرآیندهایی را که پیش از این با نورودژنراسیون مرتبط بودند، تشدید کرد.
در سطح مولکولی، پژوهشگران به مسیرهای التهابی اشاره میکنند که C. pneumoniae هدف میگیرد و به نظر میرسد پاسخ ایمنی در بافت عصبی را تقویت میکند؛ این تقویت ممکن است سلولهایی را که از پیش آسیبپذیر هستند به سمت نارسایی و مرگ سوق دهد. مولکولهایی مانند سایتوکاینها (مانند TNF-α و IL-1β)، کارکرد میکروگلیا و گردش خون سلولی ایمنی محلی از جمله اجزای احتمالی این واکنش هستند که در مدلهای حیوانی و کشتهای سلولی مشاهده شدهاند.
نویسندگان با دقت بیان میکنند که این باکتری به عنوان یک «تقویتکننده» توصیف میشود نه محرک اولیه؛ یعنی احتمال دارد C. pneumoniae یکی از عوامل متعدد در یک بیماری چندعاملی باشد. این تفکیک مفهومی برای طراحی مطالعات درمانی و تشخیصی اهمیت دارد، زیرا نشان میدهد هدفگیری مستقیم باکتری ممکن است تنها بخشی از استراتژی درمانی باشد.
«چشم نمایندهای برای مغز است،» گفت مایا کورونیو-هماوئی، نوروساینتیست از Cedars-Sinai. «عفونت باکتریایی شبکیه و التهاب مزمن میتواند بازتابی از آسیبشناسی مغز باشد و وضعیت بیماری را پیشبینی کند، که از تصویربرداری شبکیه به عنوان روشی غیرتهاجمی برای شناسایی افراد در معرض خطر آلزایمر پشتیبانی میکند.»
با وجود این، سوالات مهمی باقی میمانند. آیا C. pneumoniae میتواند یک فرصتطلب باشد که بافتی را سکنی میدهد که قبلاً توسط فرآیندهای آلزایمری آسیبدیده است؟ آیا برخی افراد از نظر ژنتیکی یا ایمنی بیشتر مستعد کلونیزاسیون شبکیه هستند؟ پاسخ به این سوالات نیازمند مطالعات طولی (longitudinal) و مداخلهای انسانی خواهد بود تا بتوان قضاوتهای بالینی قابل اتکا ارائه کرد و قبل از تغییر راهکارهای درمانی، شواهد قویتری جمعآوری شود.
علاوه بر این، محدودیتهای فنی همچنان مطرحاند: نمونهگیری پس از مرگ ممکن است بازتاب دقیقی از فرایندهای زندهٔ بیماری ارائه ندهد و خطر آلودگی تقاطعی در نمونهگیریها همیشه باید مد نظر قرار گیرد. بنابراین، تأیید این یافتهها در مطالعات مستقل و نمونههای بالینی زنده با روشهای تشخیصی حساس و اختصاصی ضروری است.
پیامدها برای تشخیص و درمان
در اینجا جذابیت کاربردی وجود دارد. شبکیه در دسترس است: فناوریهای تصویربرداری چشم مانند توموگرافی انسجام نوری (OCT) و اسکنهای مولکولی پیشرفتهٔ شبکیه، بسیار کمتر تهاجمی از بیوپسی مغز یا برخی انواع تصویربرداری نورومتابولیک هستند. اگر عفونت شبکیه به طور قابلاعتمادی با آسیبشناسی مغز همراستا باشد، یک آزمایش غیرتهاجمی چشم ممکن است روزی افراد با خطر بالا را شناسایی کند و آنها را به سوی مداخلات زودهنگام هدایت کند.
از منظر درمانی، دو مسیر اصلی باز میشود. مسیر اول ضد میکروبی است: آیا آنتیبیوتیکهای هدفمند یا ایمونوتراپیهای متمرکز بر میکروب میتوانند بار باکتریایی را کاهش داده و التهاب ثانویه را مهار کنند؟ مسیر دوم ضدالتهابی است: اگر عفونت موجب پاسخ ایمنی بیشفعال شود که نورودژنراسیون را تسریع میکند، کاهش این پاسخ ممکن است پیشرفت بیماری را کندتر سازد. هیچیک از این رویکردها اثباتشده نیستند؛ هردو نیازمند آزمایشهای بالینی دقیقاند زیرا تغییر تعادل ایمنی یا جامعه میکروبی در بزرگسالان مسن با خطرات و پیامدهای جانبی همراه است.
در جستجوی گزینههای ضد میکروبی، لازم است بررسی کنیم که درمانهای آنتیبیوتیکی سیستمیک تا چه حد به بافت شبکیه و مغز نفوذ میکنند و آیا درمانهای محلی یا ایمنیسازی هدفمند میتوانند اثربخشی بالاتری داشته باشند. از سوی دیگر، مداخله در مسیرهای التهابی باید با دقت انجام شود تا عملکرد محافظتی ایمنی به مخاطره نیفتد؛ تنظیمکنندههایی که میکروگلیا را به وضعیت حمایتی سوق میدهند یا بلوکهکنندههای انتخابی مسیرهای التهابی میتوانند گزینههای پژوهشی مطرح باشند.
«این کشف امکان هدفگیری محور عفونت-التهاب برای درمان آلزایمر را مطرح میکند،» گفت تیموتی کروتر، دانشمند علوم زیستی در Cedars-Sinai.
در کنار مداخلات دارویی، این یافتهها بر ارزش توسعه نشانگرهای زیستی (بیومارکرها) متکی بر چشم تأکید میکنند: ترکیبی از تصویربرداری شبکیه، معیارهای مولکولی در مایع چشم یا خون و تحلیلهای ژنتیکی (مثل وضعیت APOE) میتواند یک پروفایل ریسک چندبعدی ایجاد کند که در تشخیص زودهنگام و طراحی کارآزماییهای مداخلهای به کار آید.
دیدگاه کارشناسی
دکتر سرِنا مالک، ایمنیشناس اعصاب که در مطالعه دخالتی نداشت، میگوید نتایج با تصویر فزایندهای همخوانی دارد که در آن عفونتهای محیطی و التهاب مزمن بر سلامت مغز تأثیر میگذارند. «ما میدانستیم که التهاب سیستمیک میتواند افت شناختی را تشدید کند،» او توضیح میدهد. «یافتن C. pneumoniae در شبکیه برای ما یک پل آناتومیکی ملموس فراهم میکند تا بررسی کنیم چگونه این سیگنال محیطی به مغز میرسد. این به معنای آن نیست که هر مورد آلزایمر منشاء عفونی دارد، اما فهرست عوامل قابل تغییر برای بررسی را گسترش میدهد.»
این مطالعه فوریت جدیدی به پژوهشهایی که چشم و مغز را به هم پیوند میدهند افزوده است. همچنین پیچیدگی را برجسته میکند: احتمالاً آلزایمر به یک درمان واحد پاسخ نخواهد داد. اما با آشکارسازی یک تقویتکنندهٔ میکروبی احتمالی در بافتی که به آسانی قابل بررسی است، این تحقیق به سوی استراتژیهای قابل آزمایش — مسیرهای جدید بیومارکری، درمانهای هدفمند و شاید آیندهای که در آن یک اسکن سادهٔ چشم به هدایت مراقبت و پیشگیری از زوال عقل کمک کند — اشاره میکند.
از منظر پژوهشی و بالینی، گامهای بعدی شامل تایید مستقل نتایج در مجموعهٔ دادههای بزرگتر، پیگیری طولی بیماران زنده برای تعیین توالی زمانی عفونت نسبت به شروع علائم شناختی، و آغاز کارآزماییهای بالینی کنترلشده برای ارزیابی ایمنی و کارایی مداخلات ضد میکروبی و ضدالتهابی است. در نهایت، تلفیق دادههای تصویربرداری شبکیه با نشانگرهای مایع مغزی-نخاعی (CSF)، تصویربرداری PET و بیومارکرهای خون میتواند چارچوبی جامع برای تشخیص و کاربست بالینی فراهم کند.
در مجموع، این یافته چشماندازی جدید و قابلپیگیری به ارتباط میان عفونتهای محیطی، التهاب مزمن و زوال شناختی اضافه میکند؛ موضوعی که ممکن است منجر به ابزارهای تشخیصی غیرتهاجمی و گزینههای درمانی تکمیلی در آینده شود.
منبع: sciencealert
نظرات
آرمین
جالب اما یه کم تیترها پرچالشاند؛ تا وقتی تو افراد زنده و پیگیری نشده نباید بگیم علت اصلیه. صبر لازم داریم، عجله نکنیم.
تریپلین
تحقیق قویه، PCR و مدلهای حیوانی ارزش دارن. ولی همبستگی با علت فرق داره، مرحله بعدی: مطالعات روی بیماران زنده و طولی.
بیونیکس
تو کارم دیدم عفونت مزمن راهها رو عوض میکنه؛ اینکه شبکیه هم درگیر باشه یعنی باید چشمپزشک و نورولوژیست با هم کار کنن، جدی بگیریم
توربو
واقعاً از نمونههای پس از مرگ میشه نتیجه گرفت؟ ممکنه آلودگی نمونه یا باکتری فرصتطلب باشه، منتظر مطالعات طولیام.
کوینپ
منطقیش اینه: التهاب+عفونت میتونه شتاب بده. اما آنتیبیوتیک؟ مراقب اثرات جانبی باشیم، ساده نیست.
روداکس
واییی، چشم هم؟ اینکه باکتری ریه تو شبکیه باشه و با آلزایمر ربط داشته باشه… هم ترسناک هم هیجانانگیز، واقعا آینده تشخیص رو عوض میکنه؟

ارسال نظر