8 دقیقه
تصور کنید یک کلید مولکولی کوچک داخل مغز استخوان وجود دارد که وقتی راه میروید، آهسته میدوید یا یک کیسه خرید را بلند میکنید، روشن میشود — و همین روشن شدن به تقویت استخوانهای شما کمک میکند. پژوهشگران اکنون میگویند چیزی شبیه به این یافتهاند: یک پروتئین که نیروی مکانیکی را حس میکند و سلولهای بنیادی را به سمت ساخت استخوان هدایت میکند تا به جای تبدیل شدن به سلولهای چربی.
این پروتئین که به نام Piezo1 (پیزو۱) شناخته میشود، در سلولهای بنیادی مزانشیمی مغز استخوان (BMMSCs) فعال است؛ همان پیشسازهای منعطفی که میتوانند به استئوبلاستها — سلولهایی که استخوان جدید میسازند — یا آدیپوسیتها، سلولهای چربی، تبدیل شوند. انتخاب سرنوشت این سلولهای بنیادی به سیگنالهای شیمیایی، هورمونها، التهاب و مهمتر از همه نیروهای مکانیکی بستگی دارد. برای دههها مشخص بود که ورزش تمایل BMMSCs را به سوی شکلگیری استخوان افزایش میدهد، اما جزئیات مولکولی نامشخص بود. مطالعه جدیدی به رهبری دانشگاه هنگکنگ پیزو۱ را بهعنوان حسگری مکانیکی اصلی در این فرایند معرفی میکند.
اگر پیزو۱ را در موشها حذف کنید، توازن تغییر میکند. استخوانها نازکتر میشوند، تعداد استئوبلاستهای تشکیلشده کاهش مییابد و سلولهای چربی در داخل مغز استخوان تجمع میکنند. در این حالت، ورزش هم دیگر افزایش معمول در چگالی استخوان را ایجاد نمیکند. مدلهای حیوانی بهکار رفته نشان میدهند پیزو۱ فقط نقشی حاشیهای یا کمرنگ ندارد؛ بلکه مستقیماً در سلسلهمراتب سیگنالدهی شرکت میکند و بر انتخاب سرنوشت سلولی تاثیر میگذارد.
پژوهشگران مسیرهای مولکولی پاییندستی پیزو۱ را دنبال کردند تا مسیرهای رابط بین کشش مکانیکی و تصمیمگیری سلولی را مشخص کنند. وقتی پیزو۱ فعال است، بهنظر میرسد سیگنالهای التهابی را که در غیر این صورت BMMSCs را به سوی تولید چربی منحرف میکنند، مهار میکند. در غیاب یا عدم فعالیت پیزو۱، سیگنالهای التهابی افزایش مییابند و محیط مغز استخوان پذیرای رسوب چربی میشود و به موازات آن ساخت استخوان کاهش مییابد. نکته مهم آنکه بازگرداندن فعالیت پیزو۱ یا اصلاح سیگنالهای پاییندستی موجب معکوس شدن این تغییرات در مدلهای موشی شد.
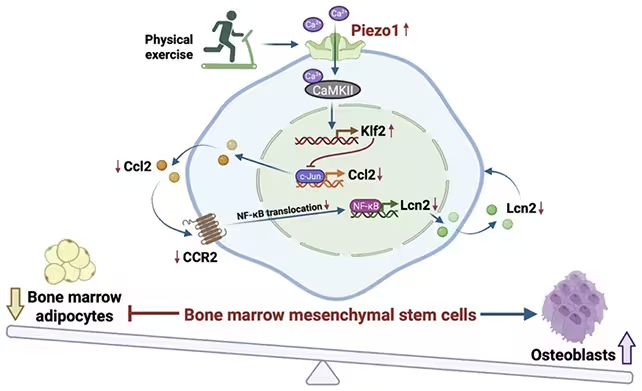
فعالسازی پیزو۱ یا مسیرهای پاییندستی آن میتواند تشکیل استخوان ناشی از ورزش را در موشها بازتولید کند.
این یافتهها یک احتمال تحریککننده را پیش مینهند: آیا روزی میتوانیم «مقلد ورزش» (exercise mimetic) بسازیم — دارویی که مغز استخوان را فریب دهد تا حتی در شرایط محدودیت حرکت، مانند زمانی که بدن تحت بار مکانیکی است، واکنش مناسب نشان دهد؟ برای سالمندان، بیماران ضعیف و افراد بستری، درمانی که بخشی از مزایای مولکولی ورزش را بازتولید کند میتواند تحولآفرین باشد. اما مسیر از مدلهای موشی تا داروی انسانی طولانی و پیچیده است.
آنچه آزمایشها نشان داد و چرا اهمیت دارد
تیم پژوهشی از دستکاریهای ژنتیکی برای حذف پیزو۱ در BMMSCs موشها استفاده کرد و ساختار استخوان، ترکیب سلولی و پاسخ به فعالیت فیزیکی را با حیوانات طبیعی مقایسه نمود. حذف پیزو۱ کاهشهای قابل اندازهگیری در چگالی معدنی استخوان و کاهش نشانگرهای تشکیل استخوان را به همراه داشت. همزمان، میکرو محیط مغز استخوان افزایش شمار آدیپوسیتها و بالا رفتن میانجیهای التهابی را نشان داد. هنگامی که پژوهشگران سیگنالدهی پیزو۱ را بازسازی کردند، هم ترکیب و هم پاسخ سازنده استخوان بازگشت.
این نتایج یک هدف مشخص برای پژوهشگران فراهم میآورد: پیزو۱ و اثرگران پاییندستی آن. با نقشهبرداری شبکه سیگنالدهی، مطالعه واژگان مولکولیای را فراهم کرد که توسعهدهندگان دارو برای طراحی مداخلات نیاز دارند. با این حال، پیزو۱ در بافتهای متعددی حضور دارد؛ در رگهای خونی، ریهها و سایر بافتها نیز در حسگری مکانیکی نقش ایفا میکند. بنابراین هر رویکرد دارویی باید دقیق باشد و توانایی تنظیم فعالیت پیزو۱ را تنها در بافت استخوان داشته باشد تا از اثرات ناخواسته در سایر اندامها جلوگیری کند.
این مطالعه که در مجله Signal Transduction and Targeted Therapy منتشر شده، در تقاطع مکانوبیولوژی و پزشکی بازساختی قرار میگیرد. همچنین اوستئوپروز (پوکی استخوان) را که اغلب بهعنوان مشکلی ناشی از عدم تعادل هورمونی و از دست دادن کلسیم دیده میشود، از منظر جدیدی بازتعریف میکند: بیماریای که در آن سیگنالینگ مکانیکی دچار اختلال میشود. این دیدگاه ابزارهای درمانی را گسترش میدهد و استراتژیهای مکملی را پیشنهاد میکند: داروهای هدفمند، بیومتریالهایی که نشانههای مکانیکی را منتقل میکنند یا تکنیکهای تحریک موضعی که فعالسازی پیزو۱ را تقویت میکنند.
از منظر تکنیکی، مطالعه جزئیات مهمی را شرح میدهد: ارتباط بین کانالهای یونی حساس به نیرو، تغییرات جریانهای کلسیمی موضعی و القای مسیرهای سیگنالینگ ضدالتهابی که سرنوشت تمایزی را تعیین میکنند. این فرایندها شامل تنظیم فاکتورهای رونویسی مرتبط با استئوژنز (مانند RUNX2) و مسیرهای التهابی شبیه NF-κB است که تمایل به آدیپوژنز را افزایش میدهند. نشان دادن اینکه پیزو۱ قادر است این شبکهها را تعدیل کند، اعتبار مولکولی برای مشاهده اثرات فیزیولوژیک ورزش بر بازسازی استخوان فراهم میآورد.
بینش کارشناسان
«این پژوهش نشان میدهد چگونه سیگنالهای مکانیکی به تصمیمهای سلولی در مغز استخوان تبدیل میشوند»، میگوید ژو آیمین (Xu Aimin)، یک دانشمند زیستپزشکی درگیر در این کار. «پیزو۱ مانند گوش مولکولی برای حرکت عمل میکند، و اکنون ما بخشی از زبانی را که آن صحبت میکند، میدانیم. این دانش برای بازتولید مزایای ورزش در سطح سلولی ضروری است.»
اریک اِنوره (Eric Honoré)، مکانوبیولوژیست و نویسنده ارشد مطالعه، دیدگاهی بالینی میافزاید: «اگر بتوانیم این مسیر را با ایمنی هدفگذاری کنیم، میتوانیم افراد ناتوان از ورزش را در برابر پیشرفت از دست دادن استخوان و شکستگیها محافظت کنیم. پتانسیل واقعی است، اما نیاز به احتیاط نیز وجود دارد — پیزو۱ نقشهای متعددی در سراسر بدن ایفا میکند و عوارض خارج هدف یک نگرانی جدی است.»
کار ترجمهای یا انتقالی نیاز به فارماکولوژی دقیق، روشهای ارسال اختصاصی بافت و در نهایت آزمایشهای انسانی دارد. تلاشهای مرحلهٔ اولیه ممکن است بر سیستمهای تحویل موضعی متمرکز شوند — برای مثال داروها یا بیومتریالهایی که در نزدیکی محل شکستگی یا ایمپلنتها اعمال میشوند تا تماس سیستمیک را کاهش دهند. راهکارهای دیگر شامل طراحی مولکولهایی است که تعاملات خاص پیزو۱ در بافت استخوان را تثبیت میکنند یا میانجیهای التهابی پاییندست را بدون دست زدن مستقیم به پیزو۱ تنظیم مینمایند.
از دید سلامت عمومی، پیام آشکار و مکرر همچنان پابرجاست: فعالیت بدنی برای سلامت استخوانها مفید است. اما در شرایطی که حرکت ممکن نیست، نقشهبرداری از مکانیک مولکولی ورزش یک مسیر جایگزین امیدوارکننده ارائه میدهد. کشف نقش مرکزی پیزو۱ مانند قطبنمایی است که به سمت درمانهایی اشاره میکند که ممکن است اسکلت پیر را محافظت کنند و خطر شکستگی را در جمعیتهای آسیبپذیر کاهش دهند.
با این وجود کار زیادی برای آزمایش وجود دارد. زیستشناسی انسانی به ندرت دقیقاً مشابه مدلهای موشی است. تفاوتهای بین گونهای در بیان پروتئینی، پاسخ ایمنی و فیزیولوژی استخوان میتواند موانعی جدی ایجاد کند. هنوز باید داروهای مناسب، محدوده دوز ایمن و کارآیی در جمعیتهای متنوع ارزیابی شود. مطالعات پیشبالینی بیشتر و سپس کارهای بالینی تدریجی ضروری خواهد بود.
آگاهی از مکان و مکانیسم تغییرات اما همه چیز را تغییر میدهد — و ممکن است نخستین گام باشد برای فراهم کردن توانایی «گفتوگو» بین استخوانها و حرکت، حتی زمانی که بدن قادر به انجام فعالیت فیزیکی نیست. در مسیر پژوهش ترجمهای، ترکیب دانش مکانوبیولوژی، مهندسی بافت و داروسازی هدفمند میتواند به راهحلهایی منجر شود که بهصورت همافزا عمل کنند: از داروهای موضعی و مواد کاشتنی هوشمند تا روشهای تحریک الکترو مکانیکی موضعی که پیزو۱ را در سایتهای هدف فعال میکنند.
در نهایت، تمرکز بر پیزو۱ به عنوان هدف تحقیقاتی نه تنها راه را برای توسعه درمانهای جدید باز میکند، بلکه چشماندازی تازه از پیشگیری و مدیریت اوستئوپروز ارائه میدهد؛ چشماندازی که فعالیت فیزیکی را بهعنوان یک محرک مکانیکی اساسی در نظر میگیرد و تلاش میکند از زبان مولکولی این محرک برای درمان استفاده کند. تا رسیدن به آن هدف، پیام ساده اما مهم باقی میماند: حرکت کنید، چون حرکت بافت استخوان را تغذیه میکند — و فهمیدن مولکولهایی مثل پیزو۱ به ما کمک میکند حتی زمانی که حرکت محدود است، راهکارهایی برای حفظ سلامت استخوان پیدا کنیم.
منبع: sciencealert
نظرات
مهران
ایده خوبه ولی نگرانی از اثرات جانبی(real) بزرگه، پیزو۱ تو ریه و رگ هم فعاله، باید خیلی دقیق و موضعی کار کنن
تریپمایند
خلاصه: حرکت مفیده، و «مقلد ورزش» وسوسهانگیزه. امیدوارم فازهای بالینی منطقی و ایمن باشن
بیونیکس
تو آزمایشگاهم دیدم محیط مکانیکی همه چیزو عوض میکنه، خوشحالم که حالا یک مولکول مشخص پیدا شده. اما ترجمه به بالین راه درازی داره
توربومک
این روی انسان هم همون اثر رو داره؟ مدل موش که خیلی فرق میکنه، اگه واقعیه که فوقالعادهست?
فینپالس
منطقیشه ولی دارو شدنش کلی چالش داره، زمان میبره و باید از عوارض خارج هدف هم بگن
دیتاپالس
وااای، یعنی یه پروتئین کوچیک میتونه اینقدر تعیینکننده باشه؟ فکرشم نمیکردم، امیدوارم تبدیلش به دارو عملی باشه…

ارسال نظر