8 دقیقه
داروی آلزایمر؛ امیدی برای رفتار اجتماعی در زیرمجموعهای از کودکان مبتلا به ASD
دارویی که ابتدا برای کند کردن زوال شناختی در بیماری آلزایمر توسعه یافته بود — ممانتین — ممکن است برای بهبود ارتباط اجتماعی و مشارکت اجتماعی در یک زیرگروه مشخص از کودکان مبتلا به اختلال طیف اتیسم (ASD) مفید باشد. یک کارآزمایی بالینی تصادفیشده که بهتازگی توسط پژوهشگرانی از بیمارستان عمومی ماساچوست و دانشگاه هاروارد هدایت شد، نشانههای امیدوارکنندهای نشان داد زمانی که دارو در دوزهای بالاتر و به طور هدفمند به بیمارانی با نمایههای خاص شیمی مغزی داده شد.
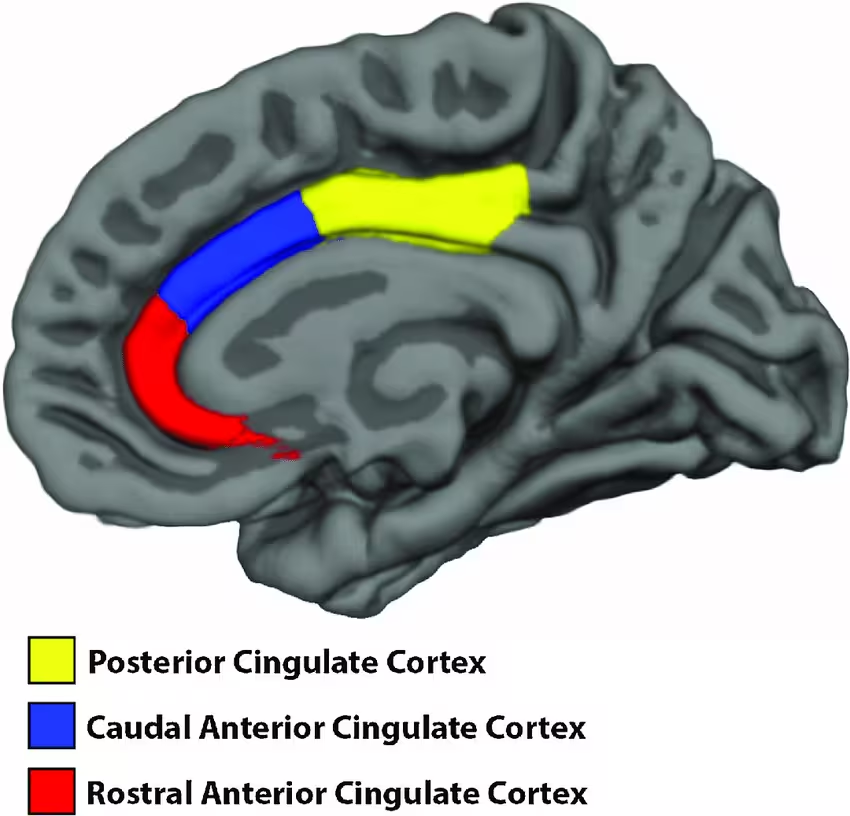
موقعیت قشر سینگولیت در مغز انسان. (Overbye et al., Dev. Cog. Neuro., 2019)
طراحی مطالعه و یافتههای اصلی
این کارآزمایی 33 کودک و نوجوان را در رده سنی 8 تا 17 سال بدون اختلال هوشیاری شدید ثبت کرد. شرکتکنندگان بهطور تصادفی برای دریافت 20 میلیگرم ممانتین روزانه یا دارونما به مدت 12 هفته تخصیص یافتند. در نگاه کلی، کل گروه نتایج یکپارچهای نشان نداد — که با مطالعات قبلی همخوانی دارد — اما وقتی پژوهشگران شرکتکنندگان را بر اساس سطح گلوتامات در یک ناحیه مغزی مرتبط با رفتار اجتماعی، یعنی قشر پیشجلویی سینگولیت (pregenual anterior cingulate cortex یا pgACC)، طبقهبندی کردند، الگوی روشنی پدیدار شد.
حدود نیمی از شرکتکنندگان دارای سطوح غیرطبیعی و بالای گلوتامات در pgACC بودند. در میان این کودکان، مراقبان و والدین گزارش کردند که مقیاسهای ارتباطی، تعامل بینفردی و مشارکت اجتماعی بهطور قابلتوجه و از نظر بالینی بهبود یافتهاند وقتی که ممانتین در مقایسه با دارونما تجویز شده بود. در مقابل، کودکانی که pgACC آنها دارای گلوتامات بالایی نبود، این نوع بهبودها را نشان ندادند.
نویسندگان تأکید میکنند که این نتایج مقدماتی است: مطالعه کوچک و کوتاهمدت بوده و برای تایید اثربخشی و ایمنی در جمعیتهای اطفال، نیاز به کارآزماییهای بزرگتر و بلندمدت وجود دارد. همچنین لازم است تفاوتهای احتمالی مربوط به سن، جنسیت و همراهی سایر شرایط عصبی یا پزشکی در تحلیلهای آینده مورد توجه قرار گیرد.
پیشزمینه علمی: گلوتامات، pgACC و ممانتین
گلوتامات بهعنوان اصلیترین ناقل عصبی تحریکی در مغز شناخته میشود و نقش محوری در یادگیری، حافظه و پلاستیسیتی سیناپسی دارد. در شرایطی که سیگنالدهی گلوتامات متعادل باشد، شبکههای عصبی میتوانند بهخوبی اطلاعات را پردازش کنند؛ اما افزایش بیش از حد فعالیت گلوتامات میتواند به اگزوکسیتیسیتی (excitatoxicity) منجر شود و پردازش عصبی را مختل سازد. قشر پیشجلویی سینگولیت (pgACC) دارای تراکم بالایی از گیرندههای مربوط به گلوتامات است و در عملکردهایی مانند شناخت اجتماعی، آگاهی احساسی و انگیزش نقش محوری ایفا میکند — حوزههایی که اغلب در ASD تحتتأثیر قرار میگیرند.
ممانتین بهعنوان یک آنتاگونیست گیرنده NMDA عمل میکند؛ این وضعیت باعث تنظیم سیگنالدهی گلوتامات میشود و از نورونها در برابر تحریک بیش از حد محافظت میکند. در بیماریهای تحلیلرونده عصبی، ممانتین میتواند با کاهش فعالیت گلوتامات پاتولوژیک، پیشرفت برخی علائم را کند کند. نتایج کارآزمایی جدید نشان میدهد که مکانیسم مشابهی ممکن است علائم اجتماعی را در کودکانی که pgACC آنها دارای گلوتامات بالاتری است، تعدیل کند.
در این مطالعه، سطح گلوتامات مغزی با استفاده از روشهای تصویربرداری عصبی که قادر به اندازهگیری غلظتهای ناقلین عصبی هستند مانند اسپکتروسکوپی تشدید مغناطیسی (magnetic resonance spectroscopy یا MRS) ارزیابی شد. چنین روشهایی امکان تفکیک زیرگروههایی را فراهم میکنند که به احتمال زیاد از مداخلات دارویی خاص بهرهمند میشوند. استفاده از MRS به عنوان یک بیومارکر، اگرچه فنآوریمحور و تا حدی پرهزینه است، امکان پیشبینی پاسخ دارویی را افزایش میدهد و بدین ترتیب میتواند به شخصیسازی درمان کمک کند.
پیامدها و گامهای بعدی
این یافتهها دو نکته کلیدی را برای پژوهشهای بالینی و پزشکی دقیق در اتیسم برجسته میکنند:
- تنوع زیستی مهم است: اختلال طیف اتیسم شامل پروفایلهای بیولوژیک متنوعی است، بنابراین درمانهایی که برای یک زیرگروه مؤثرند ممکن است برای گروههای دیگر مفید نباشند. کارآزماییهای قبلی که ASD را بهعنوان یک مجموعه همگن در نظر گرفتهاند احتمالاً منافع آنی برای زیربخشهای خاص را از دست دادهاند.
- درمان هدایتشده توسط بیومارکر: اندازهگیری گلوتامات مغزی میتواند راهی برای شخصیسازی درمان باشد و از در معرض قرار گرفتن غیرضروری کودکانی که احتمال پاسخدهی پایینی دارند، جلوگیری کند. این رویکرد میتواند هزینهها و ریسکهای جانبی را کاهش دهد و بهرهوری بالینی را افزایش دهد.
تیم پژوهشی خواستار انجام کارآزماییهای بزرگتر چندمرکزی با پیگیری طولانیتر، طیف سنی وسیعتر و نظارت دقیق بر ایمنی شد. اگر نتایج تکرار شوند، ممانتین میتواند به گزینهای برای درصد قابلتوجهی از کودکان مبتلا به ASD که دارای گلوتامات بالای pgACC هستند بدل شود، و انتظار میرود این امر منجر به بهبود نتایج اجتماعی با حداقل مواجهه برای افراد غیرپاسخگو گردد.
علاوه بر این، چند نکته عملیاتی و تحقیقاتی نیز نیازمند توجهند: دسترسی به اسپکتروسکوپی مغناطیسی در مراکز بالینی محدود است و استانداردسازی روشهای اندازهگیری گلوتامات برای مقایسه بین سایتها ضروری است. ایمنی طولانیمدت مصرف ممانتین در کودکان—بهویژه در دوزهای بالاتر—باید با دقت بررسی شود، زیرا اثرات بخصوص در دورههای رشد عصبی ممکن است متفاوت باشد. همچنین در مطالعات آینده میتوان اثرات ترکیبی ممانتین با مداخلات رفتاری متمرکز بر آموزش مهارتهای اجتماعی را مورد بررسی قرار داد تا آیا همافزایی درمانی وجود دارد یا خیر.
توضیحات فنی بیشتر درباره مکانیسم و شواهد پیشین
مکانیزم مولکولی ممانتین بهعنوان یک آنتاگونیست غیررقابتی NMDA و با خصوصیات وابسته به ولتاژ شناخته میشود؛ این ویژگی به آن اجازه میدهد تا در شرایطی که سیستم گلوتامات بیش از حد فعال است، اثر مهاری خود را اعمال کند اما عملکرد طبیعی سیناپسی را نسبتاً کمتر مختل سازد. این تمایز کلیدی باعث شده که ممانتین در بالین برای انواعی از بیماریها مورد بررسی قرار گیرد، از جمله اختلالات طیف اتیسم، اسکیزوفرنی، و برخی اختلالات نورودژنراتیو.
تحقیقات پیشین در ASD نتایج متناقضی نشان دادهاند؛ برخی مطالعات نشان دادهاند که ممانتین میتواند به کاهش برخی رفتارهای تکراری یا نقص اجتماعی کمک کند، در حالی که کارآزماییهای دیگر اثربخشی کلی را تایید نکردهاند. تفاوت در نتایج ممکن است به heterogeneity زیستی شرکتکنندگان، تفاوت در سنهای مورد مطالعه، دوزهای مختلف دارو و فقدان بیومارکرهای پیشبینیکننده مربوط باشد. کارآزمایی فعلی با هدف قرار دادن زیربخش مبتنی بر بیولوژی (یعنی سطح گلوتامات pgACC)، نمونهای از نحوه غلبه بر این چالشها است.
بهطور فیزیولوژیک، تعدیل مسیرهای گلوتاماترژیک میتواند بر اکسیتابیلیتی شبکههای اجتماعی میکروسیرکیتهای مغزی تأثیر بگذارد—بهویژه در نواحی همپوشانیدهنده میان عملکردهای احساسی و شناختی مانند pgACC، آمیگدالا و شبکه پیشفرض (default mode network). بنابراین اگر ممانتین بتواند سطح تحریکپذیری این شبکهها را در افراد دارای گلوتامات بالا تنظیم کند، انتظار میرود پردازش اطلاعات اجتماعی و پاسخهای رفتاری بهبود یابد.
ملاحظات ایمنی و اخلاقی
اگرچه ممانتین در بزرگسالان مبتلا به آلزایمر و در برخی شرایط دیگر نسبتاً ایمن در نظر گرفته شده است، استفاده در جمعیتهای کودکان نیاز به احتیاط، پایش دقیق و دادههای بلندمدت دارد. پژوهشگران باید عوارض جانبی بالقوه مانند تغییرات خواب، خستگی، تغییرات خلقی یا تداخلات دارویی را زیر نظر داشته باشند. بهعلاوه، هر تصمیم بالینی برای تجویز دارو باید تعادل میان منافع بالقوه و ریسکها را در هر کودک بهصورت جداگانه در نظر بگیرد و ترجیحات خانواده، شدت علائم و سایر درمانهای در دسترس را مدنظر قرار دهد.
از منظر اخلاقی، پژوهشگران باید به موضوع دسترسی عادلانه به ابزارهای تشخیصی (مثل MRS)، شفافیت در اطلاعرسانی به خانوادهها درباره عدم قطعیتهای فعلی و محافظت از دادههای زیستی حساس توجه کنند. همچنین ضروری است که مطالعات آینده نمایندهبودن جمعیتی را افزایش دهند تا نتایج برای گروههای متنوعتری قابلتعمیم باشد.
جمعبندی
یک کارآزمایی بالینی کوچک و هدفمند نشان میدهد که ممانتین ممکن است ارتباطات اجتماعی و مشارکت را در کودکانی از طیف اتیسم که سطح گلوتامات در pgACC آنها افزایش یافته است، بهبود بخشد. این نتایج بر نیاز به رویکردهای هدایتشده توسط بیومارکر در پژوهشهای اتیسم تأکید میکنند و تنوع زیستی زیستشناختی این اختلال را برجسته میسازند. با این حال، تأیید قوی در مطالعات بزرگتر، طولانیمدت و چندمرکزی ضروری است پیش از آنکه بتوان ممانتین را بهعنوان گزینه درمانی برای کودکان مبتلا به ASD توصیه کرد.
در نهایت، این پژوهش مسیر حرکت به سوی پزشکی دقیق در اتیسم را نشان میدهد: شناسایی زیرگروههای زیستی و تطبیق درمانها بر اساس مشخصات عصبیبیولوژیک میتواند اثربخشی درمانی را افزایش دهد و مداخلات را هدفمندتر و ایمنتر سازد. ادغام دادههای تصویربرداری عصبی، بررسیهای بالینی دقیق و پیگیری بلندمدت، لازمهٔ تبدیل این رویکرد از یافتههای تحقیقاتی به عمل بالینی روزمره است.
منبع: sciencealert


ارسال نظر