8 دقیقه
یک مطالعهٔ موردی تازه برخی مفروضات رایج دربارهٔ گروهی از ویروسهای پاپیلوما انسانی (HPV) را بههم زده است. پژوهشگران گزارش دادند که یک HPV از نوع بتا — که پیشتر بهعنوان یک فاکتور کماهمیت شناخته میشد و صرفاً آسیب ناشی از اشعهٔ فرابنفش (UV) را تشدید میکرد — در واقع در DNA تومور ادغام شده و باعث رشد کارسینومای سلول سنگفرشی پوستی (cSCC) تهاجمی در یک بیمار دارای نقص ایمنی شده است. این کشف نشان میدهد که فعالیت پنهان ویروسی و نواقص ایمنی میتواند تشخیص و راهبردهای درمانی را دگرگون کند و اهمیت آزمایشهای ویروژنتیکی و بررسی نقصهای ایمنی را برجسته میسازد.
از تومور مکرر پیشانی تا متهم ویروسی غیرمنتظره
ماجرا با زنی 34 ساله آغاز شد که سرطان پوست پیشانیاش علیرغم جراحیهای تکراری و ایمونوتراپی مکرراً عود میکرد. تشخیص او: کارسینومای سلول سنگفرشی پوستی (cSCC)، یکی از شایعترین انواع سرطان پوست. عوامل مرسوم مانند قرارگیری در معرض اشعهٔ UV و نقص در تعمیر DNA بررسی شدند، اما توالییابی ژنتیکی تومور یک عامل غیرمترقبه را آشکار کرد — توالیهای HPV بتا که در ژنوم تومور ادغام شده و فعالانه پروتئینهای ویروسی تولید میکردند.
تا کنون، ادغام HPV بتا در DNA انسانی بهعنوان عامل رشد مداوم سرطان بهطور مستند ثبت نشده بود. این تمایز، این مورد را از نقش اثباتشدهٔ انواع آلفا-HPV در سرطانهای دهانهٔ رحم و حلق تمایز میدهد، جایی که ادغام ویروسی و بیان آنکوژنها مکانیسمهای شناختهشدهای برای تومورزاییاند. گزارش حاضر نشان میدهد که الگوهای مولکولی و کلینیکی ممکن است در انواع مختلف HPV و در بسترهای ایمنی متغیر، متفاوت عمل کنند.
این یافته، فرصتهایی برای بازنگری در پروتکلهای تشخیصی و درمانی فراهم میآورد؛ بهویژه در بیمارانی که تومورهای پوستیشان رفتار غیرمعمول یا مقاوم به درمان نشان میدهد. ترکیب دادههای ویرولومیک، ژنومی و ایمنیشناسی میتواند تصویری کاملتر از علت بیماری ارائه دهد و به تصمیمگیری دقیقتر دربارهٔ درمانهای سیستمیک یا محلی کمک کند.
نقص ایمنی؛ بازکنندهٔ راه برای ویروس
این بیمار مبتلا به یک اختلال ایمنی ارثی بود که پاسخ سلولهای T او را مختل میکرد. بهطور مشخص، نقصهایی که بر پروتئین سیگنالدهی ZAP70 اثر میگذاشتند دخیل شناخته شدند — نارسایی مولکولی که مانع شناسایی مؤثر و حذف سلولهای آلوده به HPV توسط سلولهای T میشد. اگرچه سلولهای او قادر به تعمیر آسیب DNA ناشی از UV بودند، اما نظارت سازگاری ایمنی ضعیف اجازه داد HPV بتا وارد سلولهای پوستی شود و در آنجا پایدار بماند، و در نهایت این سلولها را به سمت تبدیل بدخیم سوق داد.
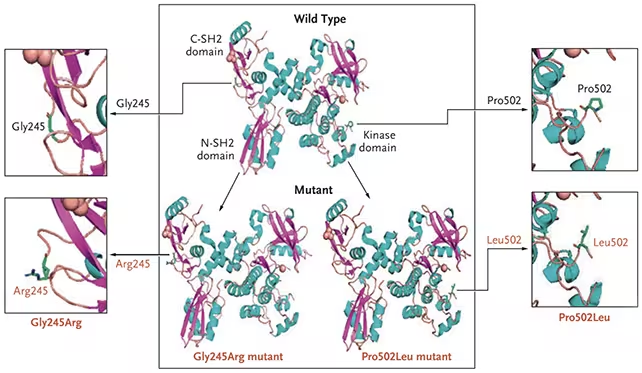
«این نشان میدهد که ممکن است افراد بیشتری با اشکال تهاجمی cSCC وجود داشته باشند که نقص ایمنی نهفتهای دارند و میتوانند از درمانهای هدفگیر ایمنی بهرهمند شوند»، میگوید آندریا لیسکو، ایمنشناس از مؤسسهٔ ملی آلرژی و بیماریهای عفونی آمریکا (NIAID). این دیدگاه، توجه ویژهای را به معاینهٔ ژنتیکی سیستم ایمنی و بررسی مسیرهای سیگنالدهی T-cell مانند ZAP70 جلب میکند.
بهعلاوه، این مورد بر اهمیت تحلیلهای مولکولی مانند توالییابی ژنومی و آنالیز بیان پروتئینی ویروسی تأکید میکند. روشهایی مانند PCR هدفمند، توالییابی نسل بعد (NGS) و آنالیز RNA میتوانند حضور و فعالیت ویروسی را در نمونههای توموری تایید کنند و نشان دهند آیا ادغام ویروسی رخ داده و ژنهای آنکوژنیک ویروسی بیان میشوند یا خیر.
چرخش درمانی: پیوند سلولهای بنیادی و بهبودی
وقتی تیم پزشکی ادغام ویروسی و نقص عملکرد سلول T را تشخیص داد، از درمانهای رایج سرطان پوست فراتر رفتند. بیمار تحت پیوند مغز استخوان و پیوند سلولهای بنیادی هماتوپویتیک قرار گرفت تا سلولهای ایمنی معیوب او با سلولهای T سالم مشتق از اهداکننده جایگزین شوند. پس از پیوند، هم cSCC مکرر و هم ضایعات دیگر مرتبط با HPV — از جمله زگیلهای پوستی و دهانی — برطرف شدند و در طول پیگیری سهساله عودی مشاهده نشد.
این نتیجه نه تنها یک موفقیت بالینی بود، بلکه نمونهای از پزشکی دقیق (precision medicine) را نشان داد که بر اساس تشخیص مولکولی و اصلاح سیستم ایمنی طراحی شده است. پیوند سلولهای بنیادی هماتوپویتیک میتواند در بیماران منتخب با نقص ایمنی زمینهای، یک راهکار بازساختی و درمانی فراهم کند که علاوه بر حذف تومور، زمینهٔ کنترل عفونتهای ویروسی مزمن را نیز ترمیم کند.
«این کشف و نتیجهٔ موفق بدون مشارکت ترکیبی ویروسشناسان، ایمنشناسان، انکولوژیستها و متخصصان پیوند که همه در یک تیم مشترک کار کردند، ممکن نبود»، لیسکو اضافه کرد. همکاری بینرشتهای در این مورد باعث شد تشخیص دقیقتر و انتخاب درمانهای سیستمیک اصلاحکنندهٔ ایمنی ممکن گردد.
چرا این یافته نحوهٔ نگرش ما به برخی سرطانهای پوستی را تغییر میدهد
این مورد، نقش مرکزی اشعهٔ فرابنفش در سرطان پوست را کماهمیت نمیکند، بلکه پیچیدگیها را نمایان میسازد: در برخی افراد دچار ضعف ایمنی، ویروسهایی که در شرایط عادی کمخطر تلقی میشوند، زمانی که نظارت ایمنی فرو میپاشد میتوانند به عوامل تومورزا تبدیل شوند. پیامدهای بالینی و جمعیتشناختی این نکته دوگانه است. از یک سو، پزشکان باید در مواجهه با cSCCهای غیرمعمول یا مقاوم به درمان، آزمایشهای ژنومی ویروسی و غربالگری ژنتیکی ایمنی را مدنظر قرار دهند. از سوی دیگر، درمانهای هدفگیر بازسازی ایمنی — از جمله پیوند سلولهای بنیادی یا ایمونوتراپیهای اختصاصی برای نقصهای مشخص بیمار — ممکن است از تکرار درمانهای موضعی ساده مؤثرتر باشند.
گزارش منتشرشده در نشریهٔ The New England Journal of Medicine (Ye و همکاران، 2025) همچنین بازتابدهندهٔ یک موفقیت بزرگ در بهداشت عمومی است: واکسیناسیون علیه انواع آلفا-HPV منجر به کاهش قابلتوجهی در بروز سرطانهای دهانهٔ رحم و حلق شده است. اگرچه واکسنهای اختصاصی برای HPV بتا هنوز تثبیت نشدهاند، این مورد ارزش بالقوهٔ پیشگیری مبتنی بر ویروس و پزشکی دقیق را تقویت میکند و انگیزهای برای توسعه واکسنها یا داروهای ضدویروسی هدفمند علیه انواع بتا فراهم میآورد.
پیامدهای بالینی و پژوهشی
- پروتکلهای تشخیصی: افزودن آنالیز ژنومی ویروسی در مواقعی که cSCC رفتار غیرطبیعی یا مقاومت به درمان نشان میدهد، ضروری است. از ترکیب توالییابی نسل جدید (NGS) با آنالیز بیان RNA میتوان برای تشخیص ادغام ویروسی و تعیین فعالیت ژنهای ویروسی استفاده کرد.
- غربالگری ژنتیکی: بررسی نقصهای سیگنالدهی در سلولهای T (مثلاً مسیرهای مرتبط با ZAP70) در موارد بازگشتپذیر یا تهاجمی میتواند بیماران مستعد را شناسایی کند و مسیر درمانی را تغییر دهد.
- راهبردهای درمانی: در بیمارانی با تومورهای تأییدشدهٔ ناشی از ویروس، باید رویکردهای بازسازی ایمنی — از جمله پیوند سلولهای بنیادی هماتوپویتیک — را در نظر گرفت. علاوه بر آن، توسعهٔ ایمونوتراپیهای هدفمند که نقص مولکولی خاص را اصلاح یا جبران کنند، از اولویتهای تحقیقاتی است.
- پایش و پیشگیری: پژوهشهای بیشتر برای تعیین فراوانی ادغام HPV بتا در جمعیتهای دارای نقص ایمنی لازم است تا مشخص شود آیا واکسنهای هدفمند یا ضدویروسها میتوانند خطر را کاهش دهند. مطالعات اپیدمیولوژیک، بررسیهای مولکولی و کارآزماییهای بالینی هماهنگ برای برنامهریزی سیاستهای پیشگیری ضروریاند.
افزون بر این، نیاز است پروتکلهای بالینی برای تشخیص و مدیریت مواردی که بین انکولوژی، ایمونولوژی و ویروسشناسی تلاقی دارند شکل بگیرند. ایجاد بانکهای دادهٔ مولکولی و ثبت موارد مشابه میتواند به درک بهتر شیوع، الگوهای ادغام ویروسی و تعیین معیارهای انتخاب بیماران برای درمانهای بازسازی ایمنی کمک کند.
دیدگاه کارشناسان
دکتر ماریا چن، ایمنشناس بالینی و پژوهشگر ترجمهای که در این مطالعه دخیل نبود، چنین اظهار میکند: «این گزارش یادآور قوی این نکته است که سرطان اغلب بیماری سیستمهای کنترلشدهٔ ناکام است — در اینجا، سیستم ایمنی. وقتی این سیستمهای کنترلی شکست میخورند، میکروبهایی که بهطور معمول بیضررند میتوانند پایگاهی برای ایجاد تغییرات بدخیم بیابند. از منظر بالینی، توالییابی و ایمونوفنوتایپینگ باید برای سرطانهای پوستی غیرمعمول یا مقاوم روتین شود.»
این مورد یک فراخوان برای یکپارچهسازی نزدیکتر ویروسشناسی، ایمنشناسی و انکولوژی است. برای بیمارانی که سرطانهایشان «رفتار نمیکنند»، نگاه فراتر از خود تومور — به ژنوم، ویروسهای حاضر در بافتها و سیمکشی ایمنی بیمار — میتواند علل قابلدرمانی و درمانهای پایداری را آشکار سازد. همچنین این رویکرد میتواند منجر به کاهش اعمال جراحی مکرر، عوارض مرتبط با درمانهای موضعی و هزینههای بلندمدت مراقبت شود.
در سطح تحقیقاتی، اولویتها شامل تعریف بیومارکرهای مولکولی برای تشخیص ادغام ویروسی فعال، توسعهٔ آزمایشهای بالینی برای غربالگری نقص ایمنی مرتبط با سلولهای T، و طراحی کارآزماییهای درمانی برای ارزیابی اثربخشی رویکردهای بازسازی ایمنی در بیماران دارای تومورهای هدایتشده توسط ویروس است. پاسخ به این پرسشها میتواند چشمانداز درمانی و پیشگیری سرطانهای پوستی را در جمعیتهای آسیبپذیر متحول کند.
منبع: sciencealert
نظرات
امیر
معقول میاد، نقص ZAP70 میتونه توضیح بده فرار ویروس از ایمنی و مقاومت درمانی. پیوند سلولی راه حل جسورانه اما منطقیه
تریپمند
حس میکنم یه مقدار بزرگنمایی شده، از طرفی کشف مهمه اما هنوز نمیشه گفت واکسن بتا واسه همه لازمه. مطالعات اپیدمی و تکرار نتایج لازمه، صبر کنید
بایونیکس
خیلی منطقیه؛ ترکیب ویرولومیک، ژنوم و ایمنولوژی تصویر کاملتری میده. پیشنهاد میکنم ژنوتایپ و ایمونوفنوتایپینگ برا موارد مقاوم روتین بشه
توربو
تو مطب دیدم بیمارای ایمنیضعیف زگیل و ضایعات دارن، اما تبدیل به سرطان و بعد بهبود با پیوند... اگه واقعی باشه، خیلی از پروندهها رو باید دوباره نگاه کنیم
کوینکس
آیا این واقعا ثابت شده؟ ادغام ویروسی بتا توی ژنوم و نقش مستقیم در تومور؟ جای زیادی برای تفسیر هست، دادهها باید تکرار بشن، نمونه های بیشتر لازمه
رودایکس
وااای، واقعاً سورپرایز شدم! یه HPV بتا که فکر میکردیم بیاهمیته وارد DNA تومور شده و باعث cSCC تهاجمی؟ پیوند سلول بنیادی همه چیزو تغییر داد... شگفتانگیز و تا حدی نگرانکننده

ارسال نظر