8 دقیقه
نسخهای قدیمی برای کنترل فشار خون، هیدرالازین، در آزمایشهای مولکولی یک عملکرد غیرمنتظره را نشان داده است که میتواند شیوه درمان فشار خون مرتبط با بارداری و حتی برخی تومورهای مغزی را بازتعریف کند. پژوهشگران میگویند این کشف درهای جدیدی به سوی توسعه درمانهای ایمنتر و هدفمندتر و شتاب در توسعه دارو از طریق بازمصرف یک ترکیب شناختهشده میگشاید.
نحوهای که یک داروی تثبیتشده مکانیسم پنهان را آشکار کرد
دانشمندان هنگام بررسی اینکه چرا هیدرالازین در درمان پرهاکلامپسی — افزایش خطرناک فشار خون در دوران بارداری — مؤثر است، یک مسیر مولکولی پیشتر ناشناخته را که این دارو بر آن اثر میگذارد کشف کردند. با ترسیم تعاملات بیوشیمیایی هیدرالازین، پژوهشگران اکنون میتوانند منافع بالینی آن را توضیح دهند و طراحی آنالوگهایی را آغاز کنند که کارایی را حفظ کرده و عوارض جانبی را کاهش دهند.
بهگفتهٔ شیمیدان مگان مَتوِز از دانشگاه پنسیلوانیا، درک هیدرالازین در سطح مولکولی یک نقشه راه برای ایجاد درمانهای ایمنتر و انتخابیتر برای فشار خون مرتبط با بارداری فراهم میآورد. این دید مکانیزمی همچنین به توسعهدهندگان دارو یک مزیت زمانی میدهد: هیدرالازین پیشتر تأیید شده و بهطور گسترده استفاده میشود، بنابراین مشتقات یا فرمولهسازیهای بهبودیافته آن میتوانند سریعتر از ترکیبات کاملاً جدید به بیماران برسند.
این کشف نه تنها به توضیح رفتار بالینی هیدرالازین کمک میکند، بلکه چارچوبی برای مطالعهٔ مکانیسمهای مولکولی مرتبط با فشار خون پرهاکلامپسی فراهم میآورد؛ از جمله ارتباطات بین عملکرد اندوتلیال، التهاب، استرس اکسیداتیو، و تغییرات در سینگالینگ سلولی. پژوهشگران با استفاده از تکنیکهای طیفبینی، کروماتوگرافی، و گونهای از آزمایشهای بیولوژیکی هدفمحور توانستند نشان دهند که هیدرالازین با مولکولهای کلیدی داخل سلول تعامل دارد و بهتدریج مسیرهایی را که قبلاً ناشناخته بودند، آشکار میکند.
چرا این یافته برای گلیوبلاستوما و درمانهای هدفمند اهمیت دارد
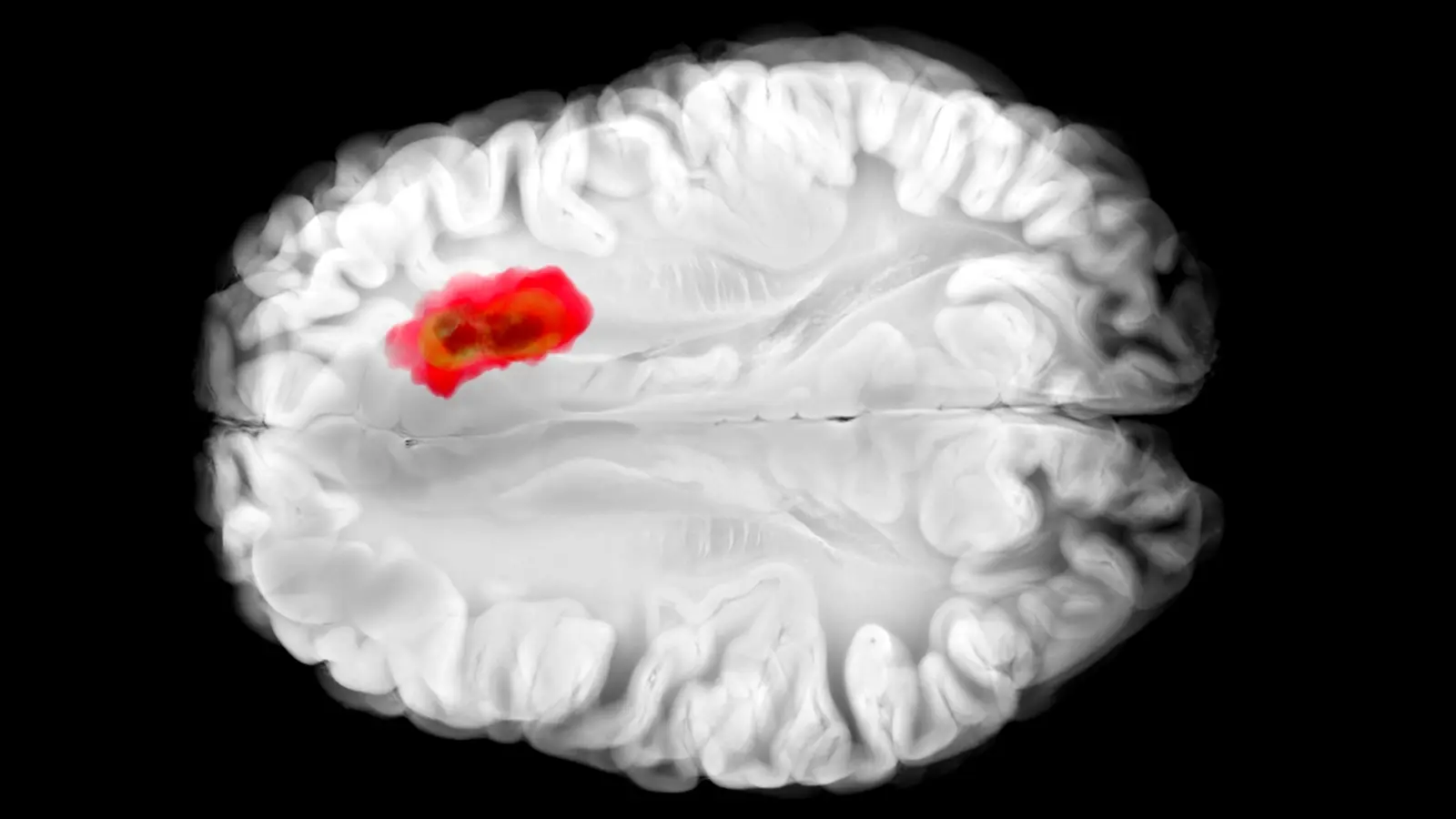
فراتر از حوزهٔ زنان و زایمان، یافتههای جدید نقاط ضعف بالقوهای در گلیوبلاستوما — یک تومور بدخیم و تهاجمی مغزی — را نشان میدهد. پژوهشها حاکی از آن است که هیدرالازین میتواند با مسیرهای سلولی که سلولهای گلیوبلاستومایی برای بقا از آنها استفاده میکنند تداخل کند. اگر دانشمندان بتوانند دارو را طوری تنظیم کنند که بهصورت انتخابی آن دفاعها را غیرفعال سازد، نتیجه میتواند مکمل مؤثری برای درمانهای موجود سرطان باشد.
گلیوبلاستوما بهدلیل تنوع ژنتیکی، مقاومت به دارو و محیط میکروی توموری پیچیده شناخته میشود. کشف اینکه یک داروی قلبی-عروقی قدیمی ممکن است برخی از مسیرهای حیاتی در سلولهای توموری را هدف قرار دهد، فرصتهایی برای توسعه رویکردهای ترکیبی فراهم میکند که هم مسیرهای متابولیک و هم مسیرهای سیگنالینگ را هدف میگیرند. چنین رویکردهایی میتوانند شامل ترکیب هیدرالازین مشتقشده با داروهای شیمیدرمانی، رادیوتراپی یا داروهای هدفمند مولکولی باشند تا حساسیت تومور به درمان افزایش یابد.
<figure class=\"image\"><img style=\"aspect-ratio:642/444;\" src=\"https://cdn.ding.news/files/post/content/2025/11/cancerdiagram.avif\" width=\"642\" height=\"444\">
تعادل بین قدرت اثر و ایمنی
یکی از مزایای بازمصرف داروها، پروفایل ایمنی نسبتاً شناختهشدهٔ آنها است. اما برای درمان سرطان مغز یا عوارض بارداری، پژوهشگران بر نیاز به تعادل میان هدفگیری سلولهای خاص و اجتناب از آسیب به بافتهای سالم تأکید میکنند. دستیابی به این تعادل احتمالاً نیازمند شیمی دارویی دقیق است تا آنالوگهای انتخابیتری از هیدرالازین ایجاد شود و همچنین آزمایشات بالینی دقیق برای ارزیابی تحملپذیری، اثربخشی و ایمنی طولانیمدت انجام گیرد.
طراحی آنالوگها میتواند شامل تغییرات ساختاری باشد که باعث افزایش اتصال به اهداف مولکولی خاص، کاهش نفوذ به بافتهای حساس، یا بهینهسازی متابولیسم دارو در بدن میشود. رویکردهای مدرن مانند طراحی دارو مبتنی بر ساختار (structure-based drug design)، شبیهسازیهای مولکولی، و استفاده از بانکهای دادهٔ ترکیبات میتوانند مسیر توسعهٔ این مواد را کوتاه کنند. همزمان، مطالعات پیشبالینی در مدلهای حیوانی و کشتهای سلولی چندسویه برای ارزیابی اثربخشی انتخابی و عوارض جانبی ضروری است.
در درمانهای نوروانکولوژیک، عبور از سد خونی-مغزی یکی از موانع عمده است. هرچند هیدرالازین در اصل برای کاربردهای قلبی-عروقی توسعه یافته است، اما اصلاح ساختار مولکولی ممکن است نفوذ به مغز را بهبود دهد یا بهعکس، آن را محدود کند تا فعالیت دارو به بافتهای هدف محدود شود. علاوه بر این، راهبردهای تحویل دارو مانند نانوحاملها، ایمونوکانژوگاتها، یا حاملهای قابل هدفگیری میتوانند به افزایش غلظت دارو در تومور و کاهش سمیت سیستمیک کمک کنند.
پیگیری بالینی: بیماران و پژوهشگران چه انتظاری دارند؟
تیم تحقیقاتی نتایج خود را در مجله Science Advances منتشر کرده است. گامهای بعدی شامل بهینهسازی انتخابیبودن ترکیب، آزمایشهای پیشبالینی متمرکز بر مدلهای گلیوبلاستوما، و کارآزماییهایی است که هدفشان بهبود نتایج برای زنان مبتلا به پرهاکلامپسی است. تصور کنید آیندهای را که در آن یک داروی قلبی-عروقی قدیمی، با بازمهندسی مبتنی بر بینش مولکولی مدرن، هم به مادران باردار و هم به بیماران مبتلا به تومورهای مغزی کمک میکند — یک راه میانبر کارآمد از میز آزمایش تا تخت بیمار.
این امر نادر است که یک داروی کلاسیک فشار خون راهبردهای جدیدی در نوروانکولوژی روشن کند، میگوید مَتوِز، و پژوهشگران امیدوارند این آغاز مجموعهای از پیشرفتهای بینرشتهای باشد که به درمانهای واقعی در میدان عمل ترجمه میشوند. برای حرکت از یافتههای آزمایشگاهی به درمان بالینی، مسیرهای تنظیمی، استانداردسازی فرمولاسیونها، و طراحی کارآزماییهای بالینی با معیارهای موفقیت روشن ضروریاند. علاوه بر این، همکاری میان گروههای بالینی، بیولوژیستهای مولکولی، شیمیدانان دارویی، و شرکتهای دارویی میتواند فرایند ترجمه را سرعت ببخشد.
چند حوزهٔ تحقیقاتی مشخص که در مراحل بعدی باید به آنها پرداخته شود عبارتاند از:
- تحلیلهای هدفمحور برای شناسایی پروتئینها یا مسیرهای دقیق تحت تأثیر هیدرالازین یا مشتقات آن.
- مطالعات توکسیکولوژی و فارماکوکینتیک در مدلهای حیوانی برای ارزیابی ایمنی و نحوه توزیع دارو در بافتها، بهخصوص عبور سد خونی-مغزی.
- توسعهٔ فرمولهسازیها و پلتفرمهای تحویل که میتوانند دارو را بهصورت محلی یا هدفمند عرضه کنند تا دوزهای سیستمیک کاهش یابد.
- طراحی کارآزماییهای بالینی فاز I/II برای تعیین دوز، تحملپذیری، و سیگنالهای اولیهٔ اثربخشی در بیماران مبتلا به پرهاکلامپسی و گلیوبلاستوما.
همچنین لازم است بیماران و جوامع پزشکی از مزایا و محدودیتهای بازمصرف داروها آگاه شوند. بازمصرف بهمعنای تضمین اثربخشی در یک شاخص بالینی جدید نیست؛ بلکه میتواند نقطه شروعی با ریسک کمتر از توسعهٔ ترکیبات کاملاً جدید باشد. شفافیت در گزارش نتایج، انتشار دادههای پیشبالینی، و همکاری با مراجع نظارتی برای تعریف مسیرهای توسعه و ارزیابی ریسک از اجزای ضروری فرآیند هستند.
در سطح عملی، شرکتهای دارویی و سازمانهای بودجهدهنده میتوانند با سرمایهگذاری هدفمند در مطالعات پیشبالینی و کارآزماییهای بالینی، شانس رسیدن به نتایج بالینی معنیدار را افزایش دهند. از نظر علمی، این کشف نشان میدهد که بازنگری در ترکیبات قدیمی با تکیه بر ابزارهای مولکولی مدرن میتواند میانبری مقرونبهصرفه و سریع برای یافتن درمانهای جدید فراهم آورد.
در پایان، اگرچه شواهد اولیه امیدوارکنندهاند، مسیر تبدیل یک کشف مولکولی به درمانهای ایمن و مؤثر طولانی و پیچیده است. نیاز به شواهد قوی در مدلهای بالینی، درک عمیقتر از هدفپذیری مولکولی، و طراحی هوشمندانهٔ کارآزماییها همچنان حیاتی است. اما این ایده که یک داروی قدیمی میتواند بهعنوان پلتفرمی برای درمانهای نوین در دو حوزهٔ متفاوت پزشکی — پرهاکلامپسی و گلیوبلاستوما — عمل کند، چشماندازی هیجانانگیز و اقتصادی برای آیندهٔ توسعه دارو ارائه میدهد.
منبع: sciencealert
نظرات
دانیکس
کمی اغراق شده به نظر میرسه، ولی مسیر علمی روشنه. اینکه هیدرالازین از اول ایمن بوده یعنی همه چی اوکی نیست، داده لازمه
پمپزون
تو کلینیک دیدم مواردی که فشار کنترل شده بودن، اما درمان تومور چیز دیگهس؛ ایدهٔ بازطراحی جذابه، امیدوارم مدلهای حیوانی سریع انجام بشه
رضان
این واقعا در گلیوبلاستوما اثر میکنه؟ کلی فاکتور هست، از سد خونی-مغزی تا سمیت... شک دارم تا وقتی کارآزمایی نباشه
رودایکس
منطقیشه tbh، بازمصرف داروها میتونن زمان رو کم کنن اما تستها مهمن، نباید عجله بشه
لابکور
وای، انتظار نداشتم هیدرالازین اینقدر کاربردی باشه... اگه واقعیت داشته باشه میتونه نجاتبخش باشه 😊 ولی امیدوارم عوارض بهتر بررسی بشه

ارسال نظر