8 دقیقه
دو کارآزمایی بالینی بزرگ نشان دادهاند که سمیگلوتاید — مؤلفه فعال در داروهای محبوبی مانند Ozempic و Wegovy و فرم خوراکی Rybelsus — توانایی کند کردن کاهش شناختی در افراد دارای اختلال شناختی خفیف یا مراحل اولیه بیماری آلزایمر را نشان نداد. این یافتهها خوشبینی اولیه نسبت به اینکه یک داروی دیابت و کاهش وزن ممکن است از مغز در برابر پیری محافظت کند را تعدیل میکنند و تصویر پیچیدهتری از مسیر توسعه درمانهای نورودژنراتیو ارائه میدهند.
What the trials tested and what they found
مطالعات evoke و evoke+ نزدیک به 3,800 شرکتکننده بین 55 تا 85 سال را جذب کردند که همگی مبتلا به اختلال شناختی خفیف (MCI) یا آلزایمر در مراحل ابتدایی بودند. در طراحی تصادفی و دوسوکور و کنترلشده با پلاسبو — استاندارد طلایی ارزیابی درمانها — داوطلبان به مدت دو سال روزانه یا سمیگلوتاید خوراکی (Rybelsus) مصرف کردند یا دارونما دریافت نمودند. این طراحی اجازه میدهد تا تأثیرات بالینی به شکلی موثقتر از تأثیرات تصادفی تفکیک شود و احتمال بایاس کمتری در نتایج وجود داشته باشد.
محققان عملکرد شناختی و توانایی انجام فعالیتهای روزمره را با استفاده از مقیاس Clinical Dementia Rating Sum of Boxes (CDR‑SB) اندازهگیری کردند؛ این نمره ترکیبی جنبههای تفکر و مهارتهای عملی زندگی روزمره را دربرمیگیرد. علاوه بر این، آزمونهای حافظه و رفتار اجرا شد و نمونهبرداری از مایع مغزینخاعی انجام گرفت تا سطوح پروتئینهای مرتبط با آلزایمر اندازهگیری شود. این مجموعه سنجهها امکان ارزیابی همزمان بیومارکرهای زیستی و علائم بالینی را فراهم میکرد.
با وجود اینکه بهبودهای کوچکی در برخی بیومارکرها مشاهده شد — که نشاندهنده اثرات زیستی سمیگلوتاید بر مسیرهای التهابی یا متابولیک بود — افراد دریافتکننده دارو در معیارهای اصلی بالینی مزیت معنیداری نشان ندادند: حافظه، عملکرد اجرایی و توانایی انجام وظایف روزمره در گروه سمیگلوتاید در طول 24 ماه به همان نرخ گروه پلاسبو کاهش یافت. این همراستا نبودن تغییرات بیولوژیک با نتایج بالینی، مسئلهای شناختهشده در تحقیقات دارویی نورودژنراتیو است.
Scientific background: why semaglutide seemed promising
سمیگلوتاید یک آگونیست گیرنده GLP‑1 (پپتید شبه گلوکاگون۱) است. GLP‑1 هورمونی است که پس از خوردن آزاد میشود و با تحریک ترشح انسولین، کاهش اشتها و کند کردن تخلیه معده به تنظیم قند خون کمک میکند. در مغز، فعالسازی گیرندههای GLP‑1 میتواند التهاب را کاهش دهد، متابولیسم انرژی نورونها را حمایت کند و سلولها را در برابر استرس محافظت نماید. این مجموعه اثرات موجب شد که داروهای مبتنی بر GLP‑1 بهعنوان نامزدهای احتمالی برای حفاظت نورونی بررسی شوند.
تحقیقات پیشبالینی — شامل کشتهای سلولی و مدلهای حیوانی — مکانیسمهای متعددی را مطرح کردند که سمیگلوتاید ممکن است از طریق آنها روندهای مرتبط با آلزایمر را تحت تأثیر قرار دهد: کاهش نورواینفلاسیون، بهبود سیگنالدهی انسولینی در بافت مغز، پشتیبانی از عملکرد میتوکندریها و کاهش تجمع پلاکهای آمیلوئید و گرههای تاو. علاوه بر این، مطالعات مشاهدهای در بیماران دیابتی نشان داد که مصرف داروهای GLP‑1 ممکن است با کاهش سرعت افت شناختی همراه باشد؛ اگرچه این مطالعات همواره علت و معلول را تعیین نمیکنند.
این شواهد آزمایشگاهی و اپیدمیولوژیک یک منطق علمی معقول برای آزمون سمیگلوتاید در افراد در مراحل ابتدایی بالینی آلزایمر فراهم آورد، زیرا هدفگذاری مسیرهای متابولیک و التهابی میتوانست موجب تغییر روند بیماری در مرحلهای شود که هنوز سلولهای زیادی قابل نجات باشند.
Why the trials may have come up negative
تفسیر نتیجه منفی چندین جنبه دارد. اول اینکه زمان مداخله اهمیت دارد: راهبردهای محافظت عصبی معمولاً بیشترین کارآیی را زمانی دارند که قبل از بروز علائم بالینی اعمال شوند. وقتی که پاتولوژی آمیلوئید و تاو تثبیت شده و نورونها از دست رفتهاند، مداخله صرف روی التهاب یا مسیرهای متابولیک ممکن است برای تغییر جهت بالینی بیماری کافی نباشد. بهعبارتی، پنجره درمانی برای تأثیرگذاری بر توالی آسیب عصبی ممکن است خیلی زودتر از مرحلهای باشد که شرکتکنندگان وارد مطالعه شدهاند.
دوم اینکه تغییرات در بیومارکرها لزوماً به مزایای عملکردی ترجمه نمیشوند. یک جابجایی کوچک در پروتئینهای مایع مغزینخاعی میتواند نشاندهنده تأثیر زیستی باشد، اما آن تأثیر ممکن است بسیار کوچک، گذرا یا بهطور مستقیم مرتبط با مدارهای عصبی تعیینکننده حافظه و عملکرد روزمره نباشد — بهخصوص در پنجره زمانی دو ساله مطالعه که برای آشکارسازی تغییرات بالینی بزرگ ممکن است کافی نباشد.
سوم اینکه آلزایمر بیماریای پیچیده و چند عاملی است. یک داروی واحد که مسیرهای GLP‑1 را هدف قرار میدهد ممکن است چند فرایند مرتبط را درگیر کند، اما همچنان ممکن است سایر محرکهای بحرانی کاهش شناختی را ندیده بگیرد. علاوه بر این، احتمال وجود زیرگروههایی از بیماران — تعریفشده براساس ژنتیک، بیماریهای عروق خونی همراه، وضعیت متابولیک یا مرحله پاتولوژی — وجود دارد که میتوانستند منفعتی کسب کنند؛ اما این اثرات در زمان تجمیع دادهها روی هزاران شرکتکننده ممکن است محو شوند و در نتایج کلی ناپدید بمانند.
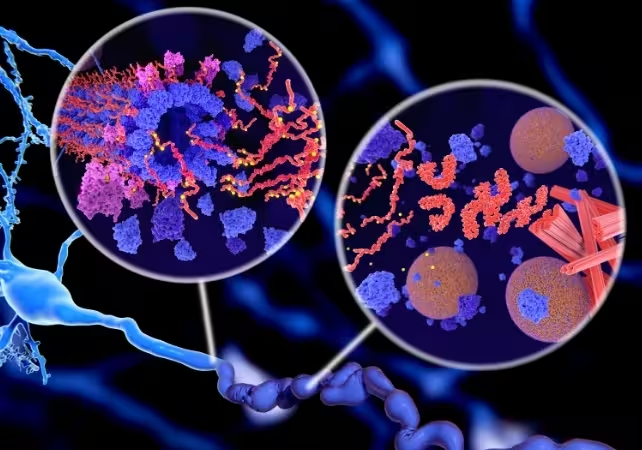
گیرههای پروتئینی تاو میتوانند مرگ نورونها را تحریک کرده و به بروز آلزایمر کمک کنند.
Trial rigor, safety and next steps
کارآزماییهای evoke در سطح جهانی، با تصادفیسازی و کنترلشده با پلاسبو انجام شدند و این ویژگیها اعتبار نتیجه کلی را افزایش میدهند. پروفایل ایمنی مشاهدهشده با آنچه پیشتر برای سمیگلوتاید در استفادههای دیابت و کاهش وزن شناخته شده بود سازگار بود — هیچ نشانه ایمنی جدیدی در طول مطالعه آشکار نشد. از آنجا که دارو در این مطالعه سود بالینی نشان نداد، شرکت نوو نوردیسک برنامههای خود برای تمدید طول مطالعه به مدت یک سال اضافی را لغو کرد.
دیتاستهای کامل و تحلیلهای زیرگروهی قرار است در کنفرانسهای پژوهشی آلزایمر در سال 2026 ارائه شوند. آن آنالیزهای عمیقتر اهمیت زیادی دارند: محققان خواهند بررسی کرد که آیا زیرمجموعههای مشخصی از بیماران بهطور جزیی بهبود شناختی داشتهاند یا خیر، آیا اثرات زیستی میان شرکتکنندگان یکنواخت بوده است و آیا آزمونهای ثانویه شناختی مزایای ظریفی را نشان میدهند که معیارهای اصلی نتوانستند ثبت کنند.
برای صنعت داروسازی، نتایج جاری بر نحوه طراحی کارآزماییهای آینده برای داروهای ضدچاقی و دیابت در زمینه بیماریهای نورودژنراتیو تأثیر خواهد گذاشت — بهویژه لزوم در نظر گرفتن مداخله زودتر، درمانهای ترکیبی یا انتخاب دقیقتر بیماران بر اساس مشخصات بیولوژیک و بالینی.
Expert Insight
«این کارآزماییها یادآور این نکتهاند که مکانیسمهای امیدوارکننده در آزمایشگاه همیشه به سود بالینی منجر نمیشوند»، دکتر النا مورالس، متخصص نورولوژی بالینی و پژوهشگر نورودرماتیک میگوید. «سمیگلوتاید چندین فرایند مرتبط با آلزایمر را فعال میکند، اما تغییر این مسیرها ممکن است وقتی علائم بالینی ظاهر شدهاند بهتنهایی کافی نباشد. گام بعدی این است که بررسی کنیم آیا استفاده زودتر، دوزهای متفاوت یا ترکیب آگونیستهای GLP‑1 با درمانهای ضدآمیلوئید یا ضدتاو میتواند منفعت قابلاندازهگیری ایجاد کند.»

پژوهشگران دیگر بر ارزش نتایج منفی تأکید میکنند: این نوع مطالعات محدوده پژوهشی را تنگتر میکنند و فرضیهها را تیزتر میسازند. درک اینکه چرا یک داروی فعال زیستی در عمل بالینی شکست میخورد به اولویتبندی مکانیسمهایی کمک میکند که باید دنبال شوند و گروههای بیمارانی که هدفگیری میشوند را مشخصتر میسازد. بهعلاوه، چنین نتایجی زمینه را برای طراحی کارآزماییهای آینده با معیارهای ورود دقیقتر، اندازهگیریهای زیستی پیشرفتهتر و استفاده از نشانگرهای پیشبینیکننده آماده میکنند.
Conclusion
نتایج evoke و evoke+ امیدها برای تبدیل سمیگلوتاید به درمانی برای آلزایمر را تعدیل میکنند. اگرچه این دارو چندین فرایند مرتبط با بیماری را تحت تأثیر قرار میدهد و تغییرات کوچکی در بیومارکرها ایجاد کرد، اما کاهش شناختی را کند نکرد و عملکرد روزمره را در افراد با بیماری علامتدار اولیه بهبود نداد. این نتیجه شکاف معمولا موجود بین مدلهای سلولی و زیستشناسی انسانی را برجسته میسازد و نیاز فوری به راهبردهای نوین — مداخله زودتر، درمانهای ترکیبی و انتخاب هدفمند بیماران — را نشان میدهد تا وعدههای بیولوژیک به منافع ملموس برای بیماران و خانوادههای درگیر آلزایمر تبدیل شود. در عین حال، تحقیقات متمرکز بر شناسایی زیرگروههای پاسخدهنده و کشف ترکیبات درمانی هدفمندتر ادامه خواهد یافت تا راههای درمانی مؤثرتری برای این بیماری پیچیده پیدا شود.
منبع: sciencealert
نظرات
اتو_ر
احساس میکنم کمی هیجان رسانهای بوده؛ بدون شک بیومارکرها مهمن اما ترجمه به عملکرد روزمره نشد 🤨 باید انتخاب بیمار هوشمندانهتر باشه.
شهرلاین
خودم خانوادگی تجربه مستقیم نداشتم ولی دیدم چطور وعدههای درمانی امید کاذب میدن، کاش مطالعات رو با بیماران دقیقتر و طولانیتر طراحی کنن
کیان
خلاصهی منطقی و متعادل؛ دیدن اثرات بیولوژیک ولی نه بالینی آشناست. احتمالا باید زودتر مداخله کنن یا ترکیبی از درمانها رو امتحان کنن.
بیونیکس
این نتایج واقعا منفی ان یا شاید زیرگروهها نشون بدن سودی بوده؟ دو سال ممکنه خیلی کوتاه باشه، جدی میگم، سوال برام بازه.
رودیکس
وااای، انتظار نداشتم انقدر ناامیدکننده باشه... کلی حرف و امید بود براش، حالا معلومه که مسیر درمانی آلزایمر خیلی پیچیده تره!

ارسال نظر