7 دقیقه
یک رویکرد جهانی بالقوه برای واکسیناسیون سرطان
پژوهشگران دانشگاه فلوریدا پیشرفتی پیشبالینی گزارش دادهاند که میتواند گسترهٔ واکسنهای درمانی سرطان را افزایش دهد. بهجای آموزش دستگاه ایمنی برای شناسایی یک هدف خاص تومور، واکسن جدید مبتنی بر mRNA یک هشدار ایمنی عمومی و قدرتمند ایجاد میکند که طیف وسیعی از سلولهای توموری — از جمله انواع مقاوم به درمان — را برای حملهٔ ایمنی قابلتشخیصتر میسازد. مطالعهای که در Nature Biomedical Engineering منتشر شده است نشان میدهد کنترل طولانیمدت تومور و پسرَفت کامل در برخی مدلهای موشی زمانی رخ میدهد که واکسن با بازدارندههای نقاط بازرسی ایمنی ترکیب شود.
پیشزمینه علمی و مکانیزم
هدف واکسنهای سرطان آموزش دستگاه ایمنی برای شناسایی و نابودی سلولهای بدخیم است. واکسنهای درمانی مرسوم معمولاً آنتیژنهای اختصاصی تومور را معرفی میکنند تا سلولهای T بتوانند یک نشانگر معین را تشخیص دهند. با این حال، بسیاری از سرطانها با تغییر آن نشانگرها یا ایجاد یک میکرومحیط مهارکنندهٔ ایمنی از تشخیص فرار میکنند.
استراتژی جدید از یک فرمولاسیون mRNA (که نویسندگان آن را uRNA نامیدهاند) استفاده میکند که بهجای آنتیژنهای اختصاصی تومور، پروتئینهای سیگنالدهندهٔ محرک ایمنی را رمزگذاری میکند. هنگام تزریق، این mRNA به سلولهای موضع تزریق دستور میدهد سایتوکاینها و سایر تنظیمکنندههای ایمنی را تولید کنند که مسیرهای ایمنی ذاتی و اکتسابی را فعال میکنند. تأثیر این فرمول بیدار کردن سلولهای ارائهدهندهٔ آنتیژن در حالت سکوت و جذب آنها در یک پاسخ ضدتوموری پایدار است.
نکتهٔ کلیدی این است که مولکولهای تولیدشده از mRNA واکسن متناسب با یک تومور مشخص نیستند. در عوض، آنها پاسخهای کلونهای ایمنی نسبتاً ساکن را تقویت کرده و شناسایی مجموعهٔ گستردهتری از ویژگیهای مرتبط با تومور را بالا میبرند. بهصورت استعاری، واکسن مانند یک آژیر جهانی عمل میکند که گشت مرزی بدن را هشدار میدهد — و نظارت را در انواع مختلف تومورها و پسزمینههای ژنتیکی افزایش میدهد.
مسدودسازی نقاط ایست (checkpoint) بهعنوان درمان همراه
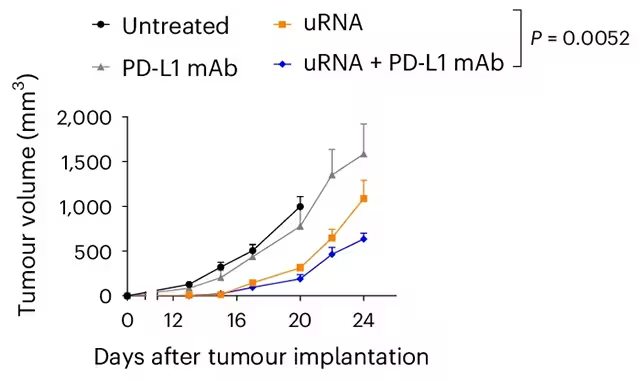
در این مطالعه واکسن mRNA با بازدارندههای نقاط بازرسی ایمنی (ICIs) — بهویژه آنتیبادیهای مونوکلونال هدفگیر PD-L1 (PD-L1 mAb) — ترکیب شد. بازدارندههای نقطهٔ بازرسی ترمزهای مولکولی را که فعالسازی سلولهای T را سرکوب میکنند برمیدارند، و وقتی با افزایش آمادهسازی ایمنیِ ایجادشده توسط واکسن همراه شوند، میتوانند اثر همافزایی ایجاد کنند.
بسیاری از تومورها با بار جهشی بالا یا مکانیسمهای مقاومت تطبیقی، فقط با ICIs فرار میکنند. در آزمایشهای موشی، ترکیب uRNA و PD-L1 mAb ایمنی ضدتوموری قویای ایجاد کرد، مقاومت را در چندین مدل تهاجمی معکوس کرد و برخی تومورها را بهطور کامل از بین برد. نویسندگان تأکید میکنند که در حالی که واکسن بهعنوان تکدرمانی در شرایطی فعالیت نشان داد، قویترین و قابلتکرارترین پاسخها هنگام ترکیب با مسدودسازی نقاط ایست بهدست آمد.
کشفهای کلیدی، پیامدها و گامهای بعدی
یافتههای کلیدی از کار پیشبالینی عبارتند از:
- حساسسازی گستردهٔ ایمنی: واکسن mRNA انواع مختلف سلولهای ایمنی را بهکار گرفت و تشخیص سلولهای توموری را که پیشتر توسط واکسنهای موجود هدفگیری نشده بودند، بهبود بخشید.
- غلبه بر مقاومت: تومورهایی که شناختهشدهبودند در برابر مسدودسازی نقاط ایست مقاوم باشند، زمانی که واکسن پیش یا همراه با درمان ICI داده شد حساس شدند.
- پسرَفتهای کامل: در یک زیرمجموعه از موشها پاکسازی کامل تومور مشاهده شد که نشاندهندهٔ اثرات بالقوهٔ درمانی در مدلهای خاص است.
پیامدها برای ایمونوتراپی سرطان قابلتوجه است. یک واکسن «آمادهٔ استفاده» با اثر گسترده میتواند نیاز به طراحی واکسنهای نوآنتیژن مخصوص هر بیمار را کاهش دهد و دسترسی به ایمونوتراپی را برای بیمارانی که تومورهایشان فاقد آنتیژنهای هدفپذیر واضح است، گسترش دهد. همانطور که الیاس سایور، سرطانشناس، در مطالعه اشاره میکند: این رویکرد یک اثبات مفهوم برای واکسنهای جهانی تجاریپذیر سرطان فراهم میآورد که سیستم ایمنی را برای حساسسازی علیه تومورهای فردی تقویت میکنند.
با این حال، یافتهها هنوز پیشبالینی هستند. گامهای بحرانی بعدی شامل بهینهسازی دوز، پروفایل ایمنی و کارآزماییهای انسانی طراحیشده با دقت برای ارزیابی اثربخشی و عوارض جانبی مربوط به ایمنی است. تیم در حال توسعهٔ فرمولاسیونهای جدید mRNA و برنامهریزی کارآزماییها برای ارزیابی هر دو سناریوی درمان و پیشگیری از عود است.
ایمنی، انتخاب بیمار و محدودیتها
تغییر در فعالسازی ایمنی خطرات شناختهشدهای دارد. تحریک بیشازحد یا نامناسب ایمنی میتواند موجب خودایمنی، سندرم آزادسازی سایتوکاین یا سمیتهای اختصاصی اعضا شود. تعیین پنجرهٔ درمانی و نشانگرهای انتخاب بیمار برای کاهش این خطرات ضروری خواهد بود. پژوهشگران همچنین بررسی میکنند آیا نشانگرهای ایمنی یا ژنتیکی خاص پیشبینیکنندهٔ پاسخ بهتر به رژیم واکسنبهعلاوه-ICI هستند یا خیر.
محدودیتهای اضافی کار کنونی شامل محدودیتهای ذاتی مدلهای موشی است که بهطور کامل پیچیدگی، ناهمگنی تومورهای انسانی، میکرومحیطهای آنها یا تنظیم طولانیمدت ایمنی را بازتولید نمیکنند. چالشهای انتقالی — تولید، پایداری و مسیرهای تصویب نظارتی برای یک محصول mRNA تنظیمکنندهٔ ایمنی جهانی — نیز نیاز به رسیدگی دارند.
دیدگاه کارشناسی
تفسیر یک مروج علم
«این مطالعه یک تغییر مفهومی مهم است: بهجای طراحی واکسنی که با تومور مطابقت داشته باشد، توانایی دستگاه ایمنی را برای دیدن تومور از ابتدا تقویت میکند،» دکتر آمینا پاتل، ایمنیشناس و مروج علم، میگوید. «اگر این رویکرد بهطور ایمن در انسان تکرار شود، میتواند سادهسازی نحوهٔ استفاده از ایمونوتراپی در انواع مختلف سرطان را ممکن سازد — اما پروفایل ایمنی و انتخاب دقیق بیماران تعیینکنندهٔ ارزش بالینی آن خواهد بود.»
افقهای آینده و فناوریهای مرتبط
این کار در تقاطع درمانهای mRNA، ایمنیشناسی تومور و توسعهٔ داروهای ایمونو-اونکولوژی قرار دارد. این مطالعه مکمل نوآوریهای دیگری مانند واکسنهای شخصیسازیشده نوآنتیژن، درمان CAR-T و رژیمهای ترکیبی شامل ویروسهای آنکولیتیک یا مولکولهای هدفدار کوچک است. پیشرفت در پلتفرمهای انتقال mRNA، طراحیهای بهتر ادجوانت و بیومارکرهای پیشبینیکنندهٔ پاسخ ایمنی، روند ترجمه را تسریع خواهد کرد.
پژوهشگران همچنین بررسی میکنند که آیا اصول مشابه واکسن میتواند از عود پس از جراحی جلوگیری کند و آیا اهداف نقطهٔ بازرسی متفاوت یا برنامهٔ دوزدهیهای دیگر نتایج را بهبود میبخشد یا خیر. همکاری میان گروههای دانشگاهی، شرکتهای بیوتکنولوژی و کنسرسیومهای بالینی برای پیشبرد این مفهوم به کارآزماییهای انسانی حیاتی خواهد بود.
نتیجهگیری
مطالعهٔ پیشبالینی به رهبری دانشگاه فلوریدا یک استراتژی واکسن mRNA را توصیف میکند که ایمنی ضدتوموری را بهطور گسترده فعال میکند و زمانی که با مسدودسازی PD-L1 ترکیب شود، تومورهای مقاوم به درمان را در موشها حذف میکند. نتایج از مفهوم واکسن جهانی سرطان که تشخیص ایمنی را در تومورهای متنوع بهبود میبخشد حمایت میکند. در حالی که امیدبخش است، این رویکرد نیاز به آزمایشهای بالینی دقیق برای ارزیابی ایمنی، ترکیبهای بهینه و شناسایی بیمارانی دارد که بیشترین سود را خواهند برد. این مطالعه که در Nature Biomedical Engineering منتشر شده است، گامی مهم در گسترش دامنهٔ ایمونوتراپی سرطان و نشانگر ادامهٔ وعدهٔ فناوری mRNA در انکولوژی است.
منبع: sciencealert

ارسال نظر