8 دقیقه
تصور کنید اتاق انتظار پیوندی که در آن گروه خونی دیگر تعیینکنندهٔ دریافت کلیه نیست. سریع. این وعدهای است که پشت یک دستاورد آزمایشگاهی اخیر قرار دارد: پژوهشگران کلیهٔ نوع A را به آنچه «کلیهٔ نوع O تبدیلشده با آنزیم» مینامند، تبدیل کردند — در واقع کلیهای که علامتهای قندی (آنتیژنها) که آن را بهعنوان نوع A قابلشناسایی میکردند، از سطح آن برداشته شدهاند. هدف ساده و در عین حال عظیم است: گسترش سازگاری تا بیماران بیشتری بتوانند زودتر پیوند دریافت کنند و مدت انتظار کوتاهتر شود.
نحوهٔ تبدیل و آزمایشی که دانشمندان انجام دادند
گروههای خونی بر پایهٔ مولکولهای قندی کوچکی هستند که به آنتیژنها معروفاند و سطح سلولها و بافتها را میپوشانند. دستگاه ایمنی بدن از آنتیبادیها برای خواندن این نشانههای مولکولی استفاده میکند. اگر سیستم ایمنی با نشانهای روبهرو شود که آن را غیرخودی تشخیص دهد، ممکن است پاسخ ایمنی و رد عضو رخ دهد. تیم پژوهشی از آنزیمها استفاده کرد — قیچیهای مولکولی مهندسیشده که میتوانند باقیماندههای قندی مشخصی را قطع کنند — تا بخشهای آنتیژنی زنجیرههای نوع A را بتراشند. وقتی آن قندها برداشته شوند، سطح عضو عملاً عاری از آنتیژنهای ABO میشود و شبیه پروفایل نوع O میشود.
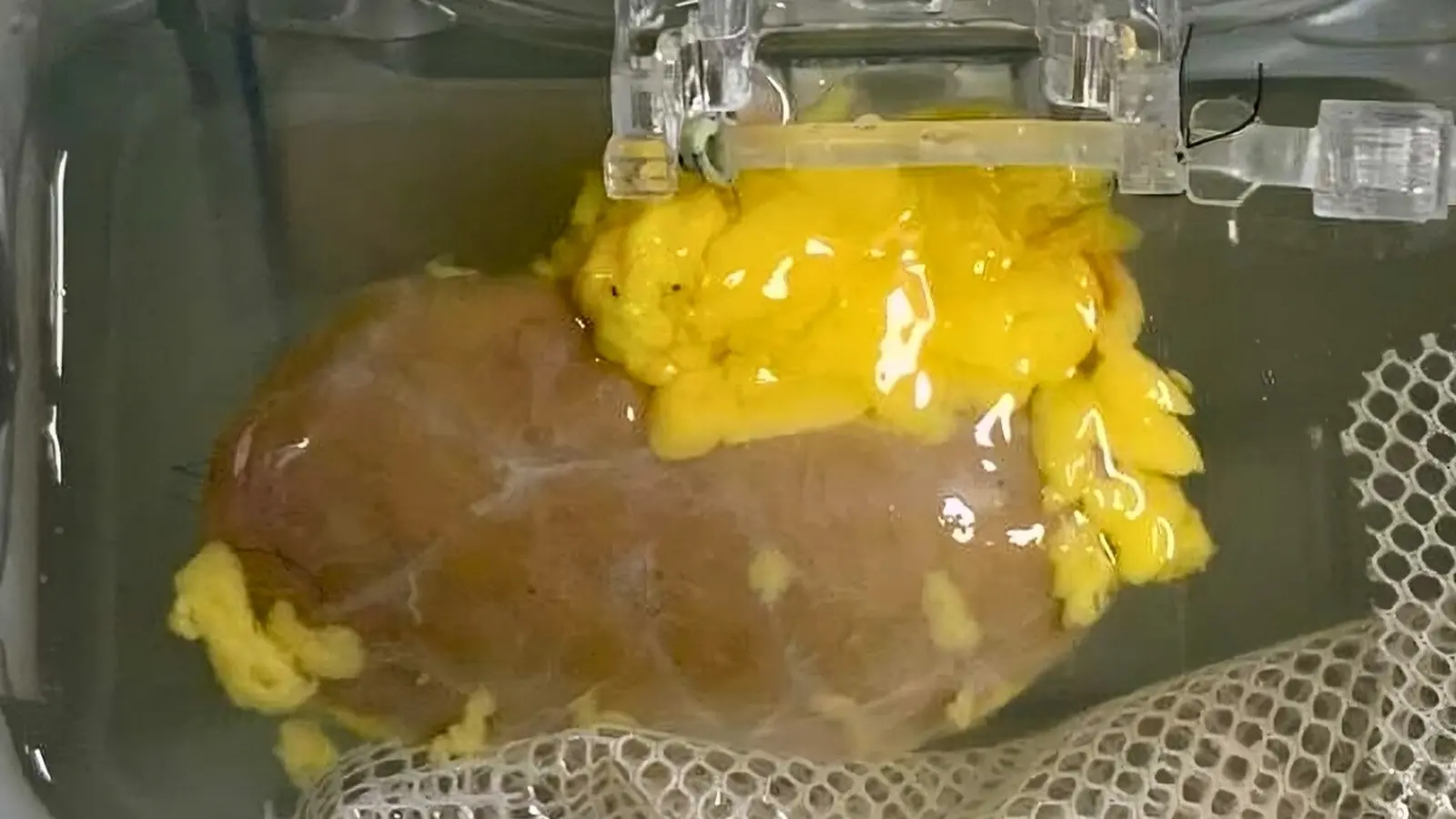
این یک تئوری صرف نیست. یک گروه همکاری از کانادا و چین یک کلیهٔ تبدیلشده با آنزیم به نوع O (ECO) را آماده کردند و آن را در بدن دهندهٔ مرگمغزی که برای تحقیق مجوز داده بود، پیوند زدند. این عضو برای چند روز عملکرد داشت. کامل نبود. تا روز سوم، ردپاهایی از نشانگرهای اصلی نوع A دوباره ظاهر شد و پاسخ ایمنی پدیدار شد. با این حال، واکنش از آنچه انتظار میرفت خفیفتر بود؛ این موضوع نشان میدهد روش ممکن است دستگاه ایمنی را بهسوی تحمل سوق دهد تا اینکه موجب رد کامل شود.
برای درک بهتر فرایند، باید به بیوشیمی گلیکوپroteinها و متابولیسم گلیکانها توجه کنیم. آنتیژنهای گروه خونی بر روی گلیکوپروتئینها و گلیکولیپیدها قرار دارند و گردش طبیعی سطحیِ این مولکولها (turnover) میتواند باعث بازسازی آنتیژنها پس از حذف شود. آنزیمهایی که در این مقاله استفاده شدهاند بهطور هدفمند باندهای اتصالِ قند خاصی را قطع میکنند؛ این کار نیازمند دقت بالا در انتخاب آنزیم و شرایط واکنش است تا ساختار بافتی کلیه حفظ شود و تغییرات ناخواستهٔ پروتئینها یا ماتریکس خارج سلولی رخ ندهد.
علاوه بر عملکرد آنی، تیم پژوهشی پارامترهای مرتبط با زمانبندی درمان آنزیمی، دوزها، دما و فرایند شستوشوی بافت را بهطور سیستماتیک بهینه کرد تا بالاترین حد حذف آنتیژن بهدست آید در حالی که آسیب مکانیکی یا شیمیایی به بافت محدود بماند. این بهبودها نشان میدهد که تبدیل آنزیمی فقط یک برش ساده نیست، بلکه فرایندی مهندسیشده است که نیازمند کنترل دقیق بیوشیمیایی و فیزیکی است.
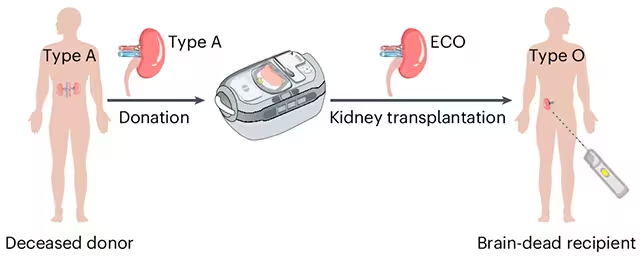
پژوهشگران یک کلیهٔ تبدیلشده به نوع O با آنزیم (ECO) آمادهٔ پیوند تولید کردند.
چرا این موضوع اهمیت دارد و مسیر پیش رو
بیماران با گروه خونی O طولانیترین انتظار را داشتهاند زیرا کلیههای نوع O بهعنوان دهندهٔ عمومی برای گلبولهای قرمز شناخته میشوند و در عمل کلیههای نوع O با دیگر گروههای خونی سازگارتر تلقی میشوند. این عدم تعادل مرگبار است. تنها در ایالات متحده، تقریباً 11 نفر هر روز در انتظار پیوند کلیه جان خود را از دست میدهند. بسیاری از آنها منتظر کلیههای نوع O هستند. بنابراین گسترش منابع قابلاستفادهٔ کلیه میتواند تأثیر مستقیم و بزرگی بر مرگومیر و کیفیت زندگی بیماران داشته باشد.
راهکارهای فعلی موجود هستند. پزشکان میتوانند گیرنده را حساسیتزدایی کنند یا پیش از پیوند بهصورت دقیق آنتیبادیها را حذف نمایند، اما این پروتکلها پیچیده، پرهزینه و پرخطر هستند — و معمولاً نیازمند یک دهندهٔ زنده و زمان برای آمادهسازی گیرندهاند. تبدیل مبتنی بر آنزیم روی کلیههای اهدایی میتواند محاسبات را تغییر دهد، زیرا با گسترش مجموعهٔ کلیههای قابلاستفاده از دهندههای فوتشده (deceased-donor)، نیاز به آمادهسازی طولانیمدت گیرنده کاهش مییابد و فرایند پیوند سریعتر و کارآمدتر خواهد شد.
با این وجود، چندین چالش علمی و بالینی باقی مانده است. بازظهور آنتیژنها پس از چند روز نشان میدهد که ممکن است برداشتن کامل انجام نشده باشد، یا گردش سطحی گلیکوپروتئینها باعث بازسازی آنتیژنها شود، یا سیستم ایمنی بهنحوی موجب بازسازی قندها گردد. پایداری بلندمدت تبدیل، عوارض جانبی بالقوهٔ آنزیمها و خطر تغییرات ناخواسته در بافت همه نیازمند مطالعهٔ نظاممند هستند. علاوه بر این، موانع مقرراتی و نیاز به آزمایشهای انسانی در مقیاس وسیعتر در پیش است تا بیمارستانها بتوانند این تکنیک را به شکل ایمن و کارآمد بپذیرند.
از منظر ایمنی زیستی، سوالاتی مانند ایمونولوژی آنتیژنهای نوظهور، پاسخهای ایمنی تطبیقی، و تعامل با داروهای سرکوبکنندهٔ ایمنی مطرحاند. آیا ترکیب تبدیل آنزیمی با پروتکلهای سرکوب ایمنی موجود میتواند طول عمر پیوند را افزایش دهد؟ آیا نیاز به رژیمهای سرکوب ایمنی جدید یا کمتر وجود دارد؟ پاسخ به این سوالات نیازمند آزمایشهای بالینی تصادفیشده و مطالعات مشاهدهای طولی خواهد بود.
.avif)
این تحقیق همچنین در کنار سایر استراتژیها برای کاهش کمبود عضو قرار دارد: پیوند بینگونهای با استفاده از کلیهٔ خوک (xenotransplantation)، آنتیبادیهای مهندسیشده برای کاهش رد، و بهبود رژیمهای سرکوب ایمنی. همهٔ این رویکردها بهطور همزمان یک حملهٔ چندجانبه به یک مشکل واحد را تشکیل میدهند — تعداد زیاد بیماران در برابر تعداد اندک اعضای پیوندی.
یک پژوهشگر در این پروژه گفت: «این لحظهای نادر است که دههها کار در زمینهٔ گلیکوبیولوژی مولکولی با نیازهای بالینی کنار هم میآیند.» این مشاهده توصیف میکند که چگونه شیمی پایهٔ آنزیمها سرانجام در یک مدل انسانی آزمایش میشود. نتایج هنوز اولیهاند، اما نشان میدهند که آیندهای ممکن است وجود داشته باشد که در آن سازگاری گروه خونی مهندسی میشود بهجای آنکه منتظر بمانیم تا گروه خونی مناسب فراهم شود.
اگر تبدیل آنزیمی بتواند در مقیاس وسیع دوامپذیر و ایمن شود، تأثیر آن بر لیستهای انتظار میتواند چشمگیر باشد: کلیههای قابلاستفادهٔ بیشتر، انتظارهای کوتاهتر و مرگومیرهای قابلپیشگیری کمتر. این کار یادآور این است که راهحلهای بحرانهای بالینی اغلب از ویرایشهای کوچک و دقیق در سطح مولکولی سرچشمه میگیرند — یک برش کوچک در یک مولکول، یک زندگی نجاتیافته.
برای بیماران و پزشکان، چند سال آینده حیاتی خواهد بود: آزمایشهای بزرگتر، ارزیابیهای کامل ایمنی، و پایش دقیق تا مشخص شود آیا این ترفند مولکولی میتواند به مزیت بالینی پایدار ترجمه شود یا خیر. هرچند روش اولیه است، اما بهعنوان یک اثبات مفهوم امیدوارکننده ایستاده است — هر بار با یک برش آنزیمی.
در نهایت، اتخاذ چنین تکنیکی نیازمند یک زنجیرهٔ تأمین دقیق، شامل تولید آنزیم تحت شرایط GMP، استانداردسازی فرایندهای تبدیل و تضمین کیفیت بافت پس از تبدیل است. رفتار آنزیمها در مقیاس بالینی، احتمال واکنشهای آلرژیک یا سیستمیک و تعامل با داروهای ضدفشار خون یا ایمونوساپرسانتها باید بهطور جدی مورد بررسی قرار گیرد. همچنین اطلاعرسانی و آموزش به تیمهای جراحی و پرستاری برای اجرای ایمن این فرایند ضروری است.
از منظر نظامهای بهداشتی، تحلیل هزینه-فایده نیز مهم است: هزینهٔ فرایند تبدیل آنزیمی در مقایسه با هزینههای فعلی حساسیتزدایی یا نگهداری در لیست انتظار چگونه است؟ پاسخ به این سوالات میتواند سیاستگذاری و تخصیص منابع را در سطح ملی و بینالمللی تحت تأثیر قرار دهد.
در مقیاس جهانی، دسترسی برابر به این تکنولوژی نیز چالشی جدی است. کشورهای با منابع محدود ممکن است بهسادگی نتوانند زیرساختهای لازم برای تولید یا اجرای تبدیل آنزیمی را فراهم کنند؛ بنابراین راهکارهای مقرونبهصرفه و انتقال فناوری باید در دستور کار محققان و سازمانهای بینالمللی قرار گیرد تا نابرابریهای موجود در دسترسی به پیوند کاهش یابد.
بهصورت خلاصه، تبدیل آنزیمی گروه خونی کلیهها یک راهبرد نوظهور و امیدوارکننده برای افزایش سازگاری پیوند کلیه است. اما پیش از آنکه بتوان آن را بهطور گسترده به کار گرفت، مطالعات دقیقتر، استانداردسازی فرایند، و توجه به پیامدهای اجتماعی و اقتصادی لازم است. اگر این موانع رفع شوند، این تکنولوژی میتواند تغییری بنیادین در مسیر درمان بیماریهای کلیوی و مدیریت لیستهای انتظار ایجاد کند و زندگی هزاران بیمار را نجات دهد.
منبع: sciencealert
نظرات
کوینکس
خوبه اما مقیاسبندی و GMP و هزینهها رو جدی نگیرن؛ و واکنش ایمنی با داروها چی میشه؟ 🤔
سفرحال
یه دوست تو انتظار پیوند بود، میگفت روزها و ماهها عذابن... اگه این جواب بده زندگیها عوض میشه، اما امیدوارم عوارضو جدی بگیرن
روداکس
ایدهاش خوبه ولی تا وقتی بازسازی آنتیژن کنترل نشه، فایدهاش محدود میمونه. نباید شتابزده وارد بالین بشن
امیر
این واقعاً تو بدن انسان پیوند شد؟ دو سه روز عملکرد یعنی خیلی کوتاه، نکنه فقط اثبات مفهوم باشه و نه راهکار عملی ؟
بیوانیکس
وای اگر واقعا بشه این یعنی کلی تغییر! ولی چرا آنتیژنها بعد چند روز برمیگردن؟ کلی سوال تو سرمه، کنجکاوم

ارسال نظر