10 دقیقه
افسردگی سالها قبل از بروز علائم حرکتی ظاهر شد و پس از تشخیص نیز ادامه یافت. این الگو از یک مطالعه بزرگ ثبتنامی در دانمارک به رهبری پژوهشگر بالینی کریستوفر رود و همکارانش در دانشگاه آرهوس بیرون آمد. با مقایسه افرادی که بعداً دچار بیماری پارکینسون یا دمانسِ لوی بادی شدند با بیمارانی که با بیماریهای مزمن جدی دیگر زندگی میکردند، تیم تحقیق تلاش کرد دریابد آیا تغییرات خلقی زنگ هشدار اختصاصی زوال عصبی هستند یا صرفاً واکنشی به بیماری مزمن طولانیمدت.
آنچه سوابق نشان داد
پژوهشگران دادههای سلامت را از سال 2007 تا 2019 دنبال کردند و 17,711 فرد را شناسایی کردند که در آن دوره تشخیص بیماری پارکینسون یا دمانس لوی بادی دریافت کرده بودند. این گروه مورد بررسی در برابر گروههای مقایسهای بزرگی مطابقت داده شد: 19,556 نفر مبتلا به آرتریت روماتوئید، 40,842 نفر با بیماری مزمن کلیه و 47,809 نفر با پوکی استخوان. بزرگی نمونه اهمیت دارد؛ با داشتن دهها هزار کنترل، تفاوتهای ظریف قابلتشخیصتر میشوند و قدرت آماری مطالعه افزایش مییابد.
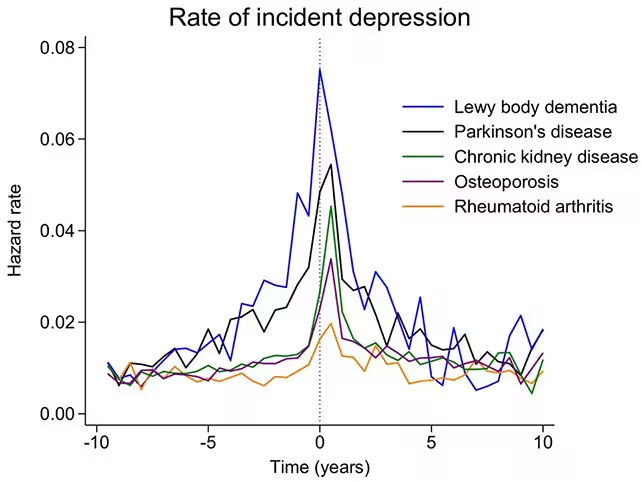
افسردگی تنها کمی در میان افرادی که بعداً دچار این اختلالات عصبی شدند شایعتر نبود؛ شیوع آن به طور معناداری افزایش یافت. نرخ ثبتشدهٔ علائم افسردگی از حدود هشت سال قبل از تشخیص رسمی عصبی شروع به صعود کرد. و این افزایش پس از تشخیص نیز ناپدید نشد—در حداقل پنج سال پس از تشخیص همچنان بالاتر باقی ماند.
در میان دو اختلال مغزی مورد مطالعه، همبستگی قویتر برای دمانس لوی بادی مشاهده شد. نویسندگان پیشنهاد میکنند این امر ممکن است بازتاب تأثیر این بیماری بر سیستمهای مغزی تنظیمکنندهٔ خلق و همچنین این واقعیت باشد که دمانس لوی بادی معمولاً پیشرفت تهاجمیتری نسبت به بیماری پارکینسون دارد.
تفسیر پیوند افسردگی و زوال عصبی
چه چیز میتواند توجیه کند که افسردگی اینقدر زود ظاهر میشود؟ سادهترین توضیح این است که افسردگی در بسیاری از موارد نشاندهندهٔ تغییرات بیولوژیکِ ابتدایی در مغز است—نقص در تعادل شیمیایی، از دست رفتن نورونهایی که ناقلهای عصبی مانند دوپامین تولید میکنند، یا گسترش تجمعهای پروتئینی شناختهشده بهعنوان «لوی بادی» که مدارهای مربوط به خلق و شناخت را مختل میکنند. به عبارت دیگر، علائم افسردگی ممکن است یکی از نخستین نشانههای قابلمشاهدهٔ آغاز فرآیندهای بیماری در سطح نورونها باشند.
با این حال احتیاط لازم است. این یک مطالعه مشاهدهای است؛ همبستگی مساوی با علت نیست. عوامل دیگری که با زوال عصبی همراهاند—اختلالات مداوم خواب، نقصان رو به رشد شناختی، التهاب سیستمیک یا موضعی، عوارض دارویی—ممکن است بهطور مستقل علائم خلقی را تحریک کنند بدون آنکه هستهٔ بیماری عصبی بهطور مستقیم مسئول باشد. پژوهشگران این موضوع را تصدیق میکنند و تأکید میکنند که انتخاب گروههای مقایسهای مبتلا به بیماریهای مزمن بهمنظور کاهش احتمال این بود که افسردگی صرفاً بازتاب بار روانی ناشی از زندگی با یک بیماری طولانیمدت باشد، انجام شده است.
میانگین میانسالِ تشخیص برای بیماری پارکینسون یا دمانس لوی بادی در این گروه 75 سال بوده است. این جزئیات برای پزشکان اهمیت دارد: وقتی فردی برای نخستینبار در اواخر عمر مبتلا به افسردگی تشخیص داده میشود، محتاطانه است که بیماریهای نورودژنراتیو در مرحلهٔ اولیه را در تشخیص افتراقی در نظر بگیرند و پیگیریهایی مانند غربالگری شناختی، ارزیابی اختلالات خواب یا ارجاع به نورولوژی را انجام دهند.
پیامدهای بالینی و پژوهشی
این یافتهها جنبهٔ عملی مهمی دارند. اگر علائم افسردگی بتوانند سالها پیش از تحلیل حرکتی، نشانههایی از تکامل اختلالات پارکینسونی را پرچمگذاری کنند، فرصتهایی پدید میآیند. بیماران میتوانند پشتیبانی زودهنگامتر برای خلق روانی، توانبخشی شناختی یا مداخلات سبک زندگی که به حفظ عملکرد کمک میکنند دریافت کنند. برای پژوهشگران، شناسایی زودهنگام پنجرهٔ زمانی مطالعهٔ مکانیسمهای بیماری و آزمایش درمانهای احتمالی تغییردهندهٔ سیر بیماری را در مراحلی که مداخلهها ممکن است مؤثرتر باشند، گسترش میدهد.
نویسندگان برای انجامِ غربالگری نظاممند سلامت روان در بیماران مبتلا به پارکینسون و دمانس لوی بادی استدلال میکنند. آنها مینویسند که مراقبت مستمر نسبت به افسردگی ممکن است به پزشکان کمک کند درمان ضدافسردگی یا مداخلات دیگر را زودتر آغاز کنند و احتمالاً عوارض مرتبط با وخامت خلق و شناخت را کندتر سازند.
با این وجود پرسشهای بیپاسخ باقی ماندهاند. کدام بیومارکرها یا نشانگرهای تصویربرداری بهترین پیشبینیکنندهٔ کسانی هستند که با افسردگی آغازینِ اواخر عمر نهایتاً دچار زوال عصبی میشوند؟ آیا درمان هدفمند افسردگی میتواند مسیر این بیماریهای مغزی را تغییر دهد؟ و چه مقدار از همبستگی مشاهدهشده توسط اختلالات خواب مثل اختلال رفتاری در خواب REM میانجیگری میشود که در برخی افراد پیشدرآمد سندرمهای پارکینسونی شناخته شده است؟
بینش کارشناسی
«این مطالعه آنچه پزشکان مدتها حدس میزدند را تقویت میکند: تغییرات خلقی میتوانند فصل ابتدایی یک داستان نورودژنراتیو باشند،» میگوید دکتر امیلی کارتر، نورولوژیست متخصص اختلالات حرکت. «شناسایی افسردگی بهعنوان چیزی فراتر از یک تشخیص روانپزشکی در سالمندان—گاه بهعنوان یک پرچم قرمز عصبی—مدیریت را تغییر میدهد. این موضوع باعث میشود غربالگری شناختی انجام شود، مرور دقیق داروها صورت گیرد و دربارهٔ پیشآگهی و نیازهای حمایتی با بیماران و خانوادهها گفتگو شود.»
دکتر کارتر اضافه میکند که پژوهشها اکنون باید بر یکپارچهسازی ارزیابیهای خلقی با بیومارکرها—تصویربرداری، بررسی مایع مغزینخاعی و پایش با دستگاههای پوشیدنی—تمرکز کنند تا مدلهای پیشبینیکنندهٔ بالینیکارآمد ساخته شود.
برای بیماران و پزشکان، پیامِ عملی منطقیتر از نومیدکننده است. افسردگی با شروع دیرهنگام نباید بهعنوان یک رویداد روانپزشکی منزوی رد شود. ممکن است زودترین سرنخ شنیداری باشد که چیزی در مغز در حال تغییر است. عمل بهموقع براساس این سرنخ—از طریق غربالگری، مراقبت چندرشتهای و پژوهش هدفمند—زمان بیشتری برای دسترسی افراد به درمانها، خدمات و کارآزماییهای بالینی میدهد، در دورههایی که هنوز مداخله میتواند تفاوتساز باشد.
جنبههای فنی و پیشنهادات کاربردی
برای تبدیل یافتههای این مطالعه به گفتمان بالینی مفید لازم است چند نکته فنی و عملی لحاظ شود. نخست اینکه پزشکان باید از ابزارهای غربالگری استاندارد برای افسردگی و اختلالات شناختی استفاده کنند؛ ابزارهایی مانند پرسشنامهٔ کوتاه افسردگی (PHQ-9) برای افسردگی و تستهایی مانند MoCA یا MMSE برای ارزیابی شناختی. ثبت دقیق زمان شروع علائم خلقی، شدت و پاسخ به درمان در پروندهٔ الکترونیک سلامت میتواند در مطالعات آینده به شناسایی الگوهای کمک کند.
دوم، ارزیابی خواب باید بهعنوان یک بخش ثابت در بیمارانی که با افسردگیِ دیررس مراجعه میکنند در نظر گرفته شود. اختلال رفتاری REM (RBD) بهعنوان یکی از پیشدرآمدهای شناختهشدهٔ پارکینسونی بودن یا طیف بیماریهای مرتبط با لِوی شناخته میشود؛ پرسش در مورد خواب دیدن خشونتآمیز، تکان خوردن در خواب یا آسیب به شریک خواب میتواند نشانههای عملی مهمی فراهم کند.
سوم، در سطح پژوهشی، ترکیب دادههای ثبتشده با نمونهبرداریهای زیستی (مثل نمونههای خون و مایع مغزینخاعی) و تصویربرداری عصبی (MRI ساختاری و عملکردی، PET برای پروتئینهای هدف) میتواند به کشف بیومارکرهای زمینهای کمک کند که همبستگی علائم خلقی و زوال عصبی را توضیح دهند. تحلیلهای طولی (Longitudinal) و مدلسازی پیشبینیکننده با استفاده از یادگیری ماشین ممکن است الگوهای پیچیدهتر را آشکار سازند.
چهارم، مداخلات بالینی برای افسردگی در سالمندان—شامل رواندرمانیهای رفتاری-شناختی، داروهای ضدافسردگی مناسب با بررسی تداخلات دارویی و مداخلات غیردارویی مانند ورزش منظم، بهینهسازی خواب و حمایت اجتماعی—باید بهصورت سیستماتیک ارزیابی شوند تا مشخص شود آیا این اقدامات میتوانند بر سیر بیماریهای پارکینسونی یا دمانس لوی بادی تأثیر بگذارند یا صرفاً کیفیت زندگی را بهبود بخشند.
چالشها و محدودیتهای مطالعه
مهم است محدودیتهای روششناختی را در نظر بگیریم. دادههای ثبتشده در پایگاههای بزرگ اغلب به تشخیصهای کدگذاریشده متکی هستند که ممکن است نسبت به ارزیابی بالینی مستقیم دارای سوگیری باشد. همچنین شدت علائم افسردگی، پاسخ به درمان و ویژگیهای دقیق بالینی معمولاً در این دیتابیسها ثبت نمیشود، که تحلیلهای جزئیتر را دشوار میسازد. سرانجام، جمعیت دانمارکی مطالعه ممکن است از نظر ساختار جمعیتی، دسترسی به خدمات سلامت و الگوهای تجویز دارو با سایر کشورها متفاوت باشد، که اهمیت تکرار مطالعات در جمعیتهای متنوعتر را افزایش میدهد.
نکات کلیدی برای پزشکان، پژوهشگران و بیماران
- افزایش شیوع افسردگی میتواند تا هشت سال قبل از تشخیص پارکینسون یا دمانس لوی بادی شروع شود؛ این میتواند یک علامت زودهنگام مهم باشد.
- افسردگی دیررس در سالمندان باید بهطور جدی ارزیابی شود و در تشخیص افتراقیِ زوال عصبی مد نظر قرار گیرد.
- غربالگری شناختی، پرسشگری خواب و در صورت نیاز ارجاع به نورولوژی باید بخشی از پیگیری بالینی بیماران مبتلا به افسردگیِ دیررس باشد.
- مطالعات آتی باید بیومارکرها، نمونههای زیستی و تصویربرداری عصبی را ترکیب کنند تا مکانیسمهای عامل و نشانگرهای پیشبینیکننده را شناسایی کنند.
- مداخله زودهنگام میتواند با فراهم آوردن فرصت برای توانبخشی شناختی، حمایت روانی و شرکت در کارآزماییهای درمانی، نتایج را بهبود بخشد.
جمعبندی و چشمانداز آینده
نتایج این مطالعه نشان میدهد افسردگی ممکن است پیشدرآمد مهمی برای برخی از اختلالات نورودژنراتیو مانند پارکینسون و دمانس لوی بادی باشد و این یافته پیامدهای بالینی و پژوهشی قابلتوجهی دارد. این مطالعات بر اهمیت یک نگاه یکپارچه میان روانپزشکی و نورولوژی تأکید میکنند و ضرورت توسعه مسیرهای تشخیصی و درمانی مشترک را نشان میدهند. با سرمایهگذاری در غربالگری نظاممند، تکمیل پروفایلهای بالینی-بیولوژیک و طراحی مطالعات مداخلهای طولی، میتوان امیدوار بود پنجرهٔ اقدام زودهنگام را بهگونهای باز کنیم که درمانها و حمایتهای مفیدی را در زمان مناسب برای بیماران فراهم سازد.
در نهایت، پیامِ کاری و خوشبینانه این است که شناسایی و واکنش به افسردگی با شروع دیررس، نه تنها میتواند کیفیت زندگی را بهبود دهد، بلکه ممکن است به تشخیص زودهنگام بیماریهای نورودژنراتیو کمک کند و فرصتهای جدیدی برای مداخلات بالینی و آزمایشی فراهم کند. این موضوع به معنای ارتباط نزدیکتر میان پزشکان عمومی، روانپزشکان، روانشناسان و نورولوژیستها و نیز مشارکت فعال بیماران و خانوادهها در فرایند تشخیصی و درمانی است.
منبع: sciencealert
نظرات
نووا_ای
این یعنی افسردگی رو جدی بگیریم... اما آیا درمانش مسیر بیماری رو عوض میکنه؟ شک دارم، ولی امیدوارم.
پمپزون
خیلی خوشبینانه نشه، مطالعه قویِ ولی دادههای ثبتشده محدودن. تکرار در جمعیتهای مختلف لازمه.
مسافر
نقش خواب و RBD جالبه، ترکیب با تصویربرداری واقعاً میتونه مسیر بیماری رو روشن کنه.
کوینکاپ
منطقیشه افسردگی دیررس میتونه هشدار باشه باید غربالگری کنن
آرمین
دیدم پدربزرگی افسرده شد بعد چند سال پارکینسون گرفت، حالا دلیلش مشخصتر شده. پیگیر شدم، سوالات زیاد...
لابکور
آیا دادههای ثبتشده خطا ندارن؟ شدت افسردگی و پاسخ به درمان هم ثبت شده؟ بدون اینا نمیشه قطعیت داد.
دیتاویو
وای، یعنی افسردگی میتونه ۸ سال قبل ظاهر بشه؟ عجیب و ترسناک... واقعاً باید بیشتر دنبال کنن!


ارسال نظر