5 دقیقه
پیشزمینه: چرا این برای دیابت نوع ۱ اهمیت دارد
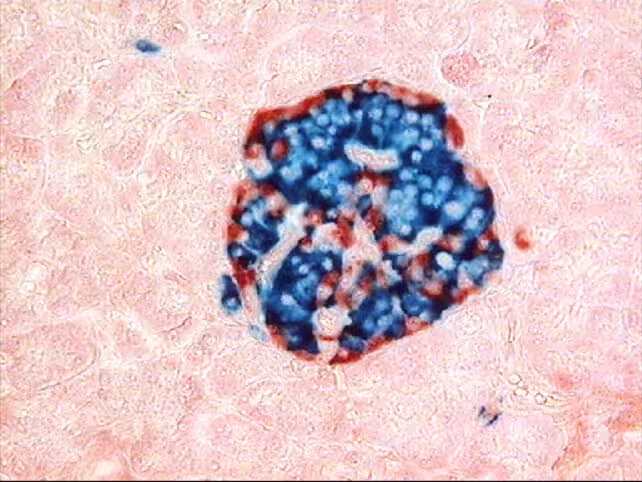
دیابت نوع ۱ یک بیماری خودایمنی است که در آن دستگاه ایمنی بدن، سلولهای جزایر لانگرهانس پانکراس را که مسئول تولید انسولین هستند نابود میکند. درمان مرسوم نیازمند تزریق مادامالعمر انسولین و مدیریت دقیق قند خون است. جایگزین کردن سلولهای آسیبدیده با سلولهای دهندهٔ عملکردی — که به آن پیوند ایزول گفته میشود — سالها بهعنوان روشی برای بازگرداندن ترشح فیزیولوژیک انسولین مورد بررسی قرار گرفته است. با این حال، سلولهای پیوندی معمولاً توسط سیستم ایمنی گیرنده بهعنوان جسم خارجی شناسایی میشوند و این موضوع مصرف داروهای سرکوبکنندهٔ ایمنی را لازم میسازد که خود با خطرات جدی عفونت و بدخیمی همراهاند.
پیوند انسانی نمونهٔ اولیه با استفاده از ایزولهای ویرایششدهٔ ژنتیکی
در یک مطالعهٔ نمونهٔ اولیهٔ برجسته، مردی ۴۲ ساله که از پنج سالگی مبتلا به دیابت نوع ۱ بود، سلولهای جزایر پانکراسی دهنده را دریافت کرد که پیش از پیوند با ویرایش ژنتیکی طوری تغییر یافته بودند که از شناسایی ایمنی فرار کنند. این سلولها از طریق چندین تزریق در بافت عضلانی ناحیهٔ ساعد کاشته شدند. طی دوازده هفتهٔ بعد، ایزولهای پیوندی شروع به تولید انسولین در پاسخ به افزایش قند خون — مثلاً بعد از غذا — کردند و نکتهٔ کلیدی این بود که بیمار نیازی به درمان سیستمیک با سرکوبکنندههای ایمنی نداشت.
استراتژی ویرایش ژنتیکی
محققان از ابزار CRISPR برای اعمال سه تغییر بر سلولهای ایزول دهنده پیش از پیوند بهره بردند. دو ویرایش باعث کاهش بیان آنتیژنهایی شدند که توسط سلولهای T سازگاری برای شناسایی و حمله به بافت غیرخودی استفاده میشوند، و ویرایش سوم تولید پروتئینی سطحسلولی به نام CD47 را افزایش داد که پاسخهای ایمنی ذاتی را مهار میکند. رویکرد سهگانه برای تضعیف هم شاخهٔ سازگاری (سلولهای T) و هم شاخهٔ ذاتی (سلولهای کشندهٔ طبیعی و ماکروفاژها) طراحی شده بود بدون اینکه ایمنی کلی گیرنده را سرکوب کند.
همهٔ سلولهای موجود در پیوند ویرایششده نبودند. این تنوع داخلی حکم شاهد داخلی را داشت: سلولهای ویرایشنشده به سرعت توسط سلولهای T حذف شدند، سلولهایی که فقط ویرایشهای کاهش آنتیژن را داشتند همچنان توسط سلولهای کشندهٔ طبیعی و ماکروفاژها هدف قرار گرفتند، و تنها سلولهایی که هر سه ویرایش موفق را داشتند برای مدت کافی زنده ماندند تا عملکردشان حفظ شود. وجود شمار کافی از ایزولهای سهویرایشی در پیوند باعث پایدار ماندن تولید انسولین در طول دورهٔ مشاهده شد.
نتایج کلیدی و پیامدها
این نخستین مورد انسانی گزارششده است که در آن سلولهای ایزول ویرایششدهٔ ژنتیکی بدون استفاده از سرکوبکنندههای سیستمیک ایمنی در یک دریافتکننده عملکرد نشان دادند. مطالعات پیشبالینی روی پریماتها و جوندگان نشان داده بودند که این روش میتواند کارا باشد، اما پیوندهای ایزول انسانی موفق پیشین معمولاً نیازمند سرکوب ایمنی بودند. اجتناب از داروهای سرکوبکنندهٔ ایمنی مادامالعمر میتواند ریسکهای طولانیمدت سلامت را برای گیرندگان پیوند بهشدت کاهش دهد و دامنهٔ کاربرد بالینی درمانهای سلولی را گسترش دهد.
فراتر از دیابت، این تکنیک پیشنهادگر یک سکوی عمومی است برای کمقابلرویت کردن دیگر سلولها و بافتهای دهنده در مقابل سیستم ایمنی میزبان. اگر در آزمایشهای وسیعتر قابل تکرار و ایمن باشد، مهندسی فرار از ایمنی با CRISPR میتواند نیاز به سرکوب ایمنی را در طیفی از پیوندهای آلوژنیک کاهش دهد یا حتی از میان بردارد.
تحولات مرتبط و زمینهٔ کلی
پیشرفتهای موازی شامل رویکردهای خودگیرنده است که اساساً ناسازگاری ایمنی را حذف میکنند: برای مثال، یک مورد اخیر در چین گزارش کرد زنی جوان که سلولهای تولیدکنندهٔ انسولین مشتق از سلولهای بنیادی خودش را دریافت کرد و بدون موانع ایمنی وابسته به دهنده، کنترل پایداری روی قند خون بهدست آورد. هر دو مسیر درمانی — سلولدرمانی خودگیرنده و پیوندهای آلوژنیک با فرار از ایمنی — جهتهای تحقیق فعالی هستند که هرکدام مزایا و چالشهای فنی متمایزی دارند.
دیدگاه کارشناس
«این نتیجه یک اثبات مفهوم محوری است»، دکتر النا مارتین، ایمونولوژیستی ساختگی که با ایمنیشناسی پیوند آشنایی دارد، میگوید. «ترکیب کاهش آنتیژن و افزایش CD47 هر دو شاخهٔ ایمنی سازگاری و ذاتی را مورد هدف قرار میدهد — این نوآوری کلیدی است. اما ما به آزمایشهای تصادفی و بزرگتر نیاز داریم تا پایداری را تأیید کنیم، اثرات خارجهدف و ایمنی بلندمدت را بررسی کنیم.» کارشناسان بر رصد دقیق برای احتمال پیامدهای ناخواسته تأکید دارند، مانند تغییر رفتار پیوند یا عوارض نادر ایمنی.
نتیجهگیری
مورد گزارششده گامی بزرگ بهسوی درمانهای مبتنی بر سلول برای دیابت نوع ۱ محسوب میشود و نشان میدهد که ایزولهای ویرایششده با CRISPR میتوانند در بدن انسان عملکرد داشته باشند بدون نیاز به سرکوب سیستمیک ایمنی. اگرچه نتایج مقدماتیاند، این پیشرفت راههای نوینی برای درمانهای سلولی ایمنتر و کاربردپذیرتر باز میکند و ضرورت ادامهٔ آزمایشهای بالینی برای ارزیابی اثربخشی، ایمنی و پیامدهای درازمدت را برجسته میسازد.
منبع: nejm


ارسال نظر